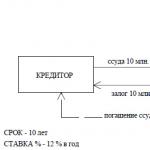
ชุดพันธุกรรมของโลหะและสารประกอบของพวกมัน ความสัมพันธ์ทางพันธุกรรมระหว่างกลุ่มหลักของสารอนินทรีย์
การทำซ้ำ การเชื่อมต่อทางพันธุกรรมของคลาสไม่ได้ สารประกอบอินทรีย์
บทนำ
หัวข้อของบทเรียนนี้คือ “การทำซ้ำ การเชื่อมต่อทางพันธุกรรมของชั้นเรียน สารประกอบอนินทรีย์". คุณจะทำซ้ำว่าสารอนินทรีย์ถูกแบ่งออกอย่างไร คุณจะสรุปได้ว่าสารประกอบอนินทรีย์อีกประเภทหนึ่งสามารถหาได้จากชั้นหนึ่งได้อย่างไร จากข้อมูลที่ได้รับ คุณจะพบว่าความเชื่อมโยงทางพันธุกรรมของคลาสดังกล่าวคืออะไร สองวิธีหลักในการเชื่อมต่อดังกล่าว
เรื่อง: บทนำ
บทเรียน: การทำซ้ำ ความสัมพันธ์ทางพันธุกรรมของคลาสของสารประกอบอนินทรีย์
เคมีเป็นศาสตร์แห่งสสาร คุณสมบัติ และการเปลี่ยนแปลงซึ่งกันและกัน
ข้าว. 1. การเชื่อมต่อทางพันธุกรรมของคลาสของสารประกอบอนินทรีย์
สารอนินทรีย์ทั้งหมดสามารถแบ่งออกเป็น:
สารง่ายๆ
สารที่ซับซ้อน
สารง่าย ๆ แบ่งออกเป็น:
โลหะ
อโลหะ
สารประกอบสามารถแบ่งออกเป็น:
ฐานราก
กรด
เกลือ. ดูรูปที่ 1
เหล่านี้เป็นสารประกอบไบนารีที่ประกอบด้วยสององค์ประกอบ ซึ่งหนึ่งในนั้นคือออกซิเจนในสถานะออกซิเดชัน -2 รูปที่ 2
ตัวอย่างเช่น แคลเซียมออกไซด์: Ca +2 O -2, ฟอสฟอรัสออกไซด์ (V) P 2 O 5., ไนตริกออกไซด์ (IV) -« หางจิ้งจอก"

ข้าว. 2. ออกไซด์
แบ่งออกเป็น:
หลัก
กรด
ออกไซด์พื้นฐานสอดคล้อง บริเวณ.
กรดออกไซด์สอดคล้อง กรด.
เกลือประกอบด้วย ไอออนบวกของโลหะและ แอนไอออนตกค้างของกรด.

ข้าว. 3. เส้นทางความสัมพันธ์ทางพันธุกรรมระหว่างสาร
ดังนั้น: จากสารประกอบอนินทรีย์ชั้นหนึ่งสามารถหาอีกชั้นหนึ่งได้
ดังนั้น ทั้งหมด ประเภทของสารอนินทรีย์เชื่อมต่อถึงกัน.
การเชื่อมต่อคลาสสารประกอบอนินทรีย์มักถูกเรียกว่า พันธุกรรมรูปที่ 3
ปฐมกาลในภาษากรีกหมายถึง "ต้นกำเนิด" เหล่านั้น. ความเชื่อมโยงทางพันธุกรรมแสดงให้เห็นความสัมพันธ์ระหว่างการเปลี่ยนแปลงของสารและที่มาของสารจากสารตัวเดียว
มีสองวิธีหลักในความสัมพันธ์ทางพันธุกรรมระหว่างสาร หนึ่งในนั้นเริ่มต้นด้วยโลหะ อีกอันเริ่มต้นด้วยอโลหะ
ชุดพันธุกรรมโลหะแสดง:
โลหะ → ออกไซด์พื้นฐาน → เกลือ → เบส → เกลือใหม่
ชุดพันธุกรรมของอโลหะสะท้อนการเปลี่ยนแปลงต่อไปนี้:
อโลหะ → กรดออกไซด์ → กรด → เกลือ
สำหรับชุดพันธุกรรมใด ๆ เราสามารถเขียนสมการปฏิกิริยาที่แสดง การแปรสภาพของสารหนึ่งไปเป็นอีกสารหนึ่ง.
ในการเริ่มต้น มีความจำเป็นต้องพิจารณาว่าสารอนินทรีย์แต่ละกลุ่มอยู่ในกลุ่มพันธุกรรมประเภทใด
คิด ทำอย่างไรให้สารยืนอยู่ข้างหลังจากสารที่ยืนอยู่หน้าลูกศร
ตัวอย่าง # 1 ชุดพันธุกรรมของโลหะ

เริ่มแถว สารง่าย ๆโลหะทองแดง ในการเปลี่ยนแปลงครั้งแรก คุณต้องเผาทองแดงในบรรยากาศที่มีออกซิเจน
2Cu +O 2 →2CuO
การเปลี่ยนแปลงที่สอง: คุณต้องได้รับเกลือ CuCl 2 มันถูกสร้างขึ้นโดยกรดไฮโดรคลอริก HCl เพราะเกลือของกรดไฮโดรคลอริกเรียกว่าคลอไรด์
CuO +2 HCl → CuCl 2 + H 2 O
ขั้นตอนที่สาม: เพื่อให้ได้เบสที่ไม่ละลายน้ำ คุณต้องเติมด่างลงในเกลือที่ละลายน้ำได้
CuCl 2 + 2NaOH → Cu(OH) 2 ↓ + 2NaCl
ในการแปลงคอปเปอร์ (II) ไฮดรอกไซด์เป็นคอปเปอร์ (II) ซัลเฟต ให้เติมลงไป กรดซัลฟูริก H2SO4.
Cu(OH) 2 ↓ + H 2 SO 4 → CuSO 4 + 2H 2 O
ตัวอย่าง # 2 ชุดพันธุกรรมของอโลหะ

ซีรีส์นี้เริ่มต้นด้วยสารธรรมดาที่ไม่ใช่คาร์บอน ในการเปลี่ยนแปลงครั้งแรก คุณต้องเผาคาร์บอนในบรรยากาศที่มีออกซิเจน
C + O 2 → CO 2
เมื่อเติมน้ำในกรดออกไซด์ จะได้กรดซึ่งเรียกว่ากรดคาร์บอนิก
CO 2 + H 2 O → H 2 CO 3
เพื่อรับเกลือ กรดคาร์บอนิก- แคลเซียมคาร์บอเนต คุณต้องเพิ่มสารประกอบแคลเซียมลงในกรด เช่น แคลเซียมไฮดรอกไซด์ Ca (OH) 2
H 2 CO 3 + Ca (OH) 2 → CaCO 3 + 2H 2 O
องค์ประกอบของชุดพันธุกรรมใด ๆ รวมถึงสาร คลาสต่างๆสารประกอบอนินทรีย์
แต่สารเหล่านี้จำเป็นต้องมีองค์ประกอบเดียวกัน เมื่อทราบคุณสมบัติทางเคมีของคลาสของสารประกอบ คุณสามารถเลือกสมการปฏิกิริยาที่สามารถทำการเปลี่ยนแปลงเหล่านี้ได้ การเปลี่ยนแปลงเหล่านี้ยังใช้ในการผลิต เพื่อเลือกวิธีการที่สมเหตุสมผลที่สุดในการได้มาซึ่งสารบางชนิด
คุณพูดซ้ำว่าสารอนินทรีย์ทั้งหมดถูกแบ่งออกอย่างไร สรุปว่าสารประกอบอนินทรีย์อีกประเภทหนึ่งสามารถหาได้จากชั้นหนึ่งได้อย่างไร จากข้อมูลที่ได้รับ เราได้เรียนรู้ว่าความสัมพันธ์ทางพันธุกรรมของคลาสดังกล่าวคืออะไร สองวิธีหลักของความสัมพันธ์ดังกล่าว .
1. Rudzitis G.E. เคมีอนินทรีย์และอินทรีย์ ชั้นประถมศึกษาปีที่ 8: ตำราเรียนสำหรับ สถาบันการศึกษา: ระดับพื้นฐาน / G. E. Rudzitis, F.G. Feldman.M.: การตรัสรู้ 2554 176 หน้า: ป่วย
2. Popel P.P. Chemistry: 8th class หนังสือเรียนสำหรับสถานศึกษาทั่วไป / ป.ป.ช. Popel, L.S. Krivlya. -K.: IC "Academy", 2008.-240 p.: ill.
3. Gabrielyan O.S. เคมี. เกรด 9 หนังสือเรียน. สำนักพิมพ์: Drofa.: 2001. 224 วินาที
1. No. 10-a, 10z (p. 112) Rudzitis G.E. เคมีอนินทรีย์และอินทรีย์ ชั้นประถมศึกษาปีที่ 8: ตำราเรียนสำหรับสถาบันการศึกษา: ระดับพื้นฐาน / G. E. Rudzitis, F.G. Feldman.M.: การตรัสรู้ 2554 176: ป่วย
2. วิธีการรับแคลเซียมซัลเฟตจากแคลเซียมออกไซด์ในสองวิธี?
3. สร้างชุดพันธุกรรมเพื่อให้ได้แบเรียมซัลเฟตจากกำมะถัน เขียนสมการปฏิกิริยา
หัวข้อ: ความสัมพันธ์ทางพันธุกรรมระหว่างโลหะกับอโลหะและสารประกอบของพวกมัน ชั้นประถมศึกษาปีที่ 9
วัตถุประสงค์: เพื่อการศึกษา: เพื่อรวบรวมแนวคิดของ "อนุกรมทางพันธุกรรม", "การเชื่อมต่อทางพันธุกรรม"; เพื่อสอนวิธีการวาดชุดองค์ประกอบทางพันธุกรรม (โลหะและอโลหะ) เพื่อวาดสมการของปฏิกิริยาที่สอดคล้องกับชุดพันธุกรรม ตรวจสอบวิธีการเรียนรู้ความรู้เกี่ยวกับ คุณสมบัติทางเคมีออกไซด์ กรด เกลือ เบส การพัฒนา: พัฒนาความสามารถในการวิเคราะห์ เปรียบเทียบ สรุป และสรุป วาดสมการ ปฏิกริยาเคมี; การศึกษา: เพื่อส่งเสริมการก่อตัวของโลกทัศน์ทางวิทยาศาสตร์
รับรองบทเรียน: ตาราง " ระบบธาตุ”, “ตารางการละลาย”, “ชุดกิจกรรมของโลหะ”, คำแนะนำสำหรับนักเรียน, งานทดสอบความรู้
ความคืบหน้าของงาน : 1) อ. ช่วงเวลา
2) กำลังตรวจสอบ d / z
3) การเรียนรู้เนื้อหาใหม่
4) แก้ไข
5) ด/จ
1) องค์กร ช่วงเวลา. ทักทาย.
2) การตรวจสอบ d / z

การเชื่อมโยงทางพันธุกรรมคือการเชื่อมโยงระหว่างคลาสต่างๆ ตามการเปลี่ยนแปลงร่วมกัน
เมื่อทราบประเภทของสารอนินทรีย์แล้ว ก็สามารถประกอบชุดพันธุกรรมของโลหะและอโลหะได้ แถวเหล่านี้อิงตามองค์ประกอบเดียวกัน
ในบรรดาโลหะนั้น ซีรีย์สองประเภทสามารถแยกแยะได้:
1 . ชุดพันธุกรรมที่ด่างทำหน้าที่เป็นฐาน ชุดนี้สามารถแสดงได้โดยใช้การแปลงต่อไปนี้:
โลหะ→ออกไซด์พื้นฐาน→ด่าง→เกลือ
ตัวอย่างเช่น K→K 2 O→KOH→KCl
2 . อนุกรมทางพันธุกรรม โดยที่เบสที่ไม่ละลายน้ำทำหน้าที่เป็นเบส จากนั้นอนุกรมนี้สามารถแทนด้วยสายโซ่แห่งการเปลี่ยนแปลง:
โลหะ→ออกไซด์พื้นฐาน→เกลือ→เบสที่ไม่ละลายน้ำ→
→ออกไซด์พื้นฐาน→โลหะ
ตัวอย่างเช่น Cu→CuO→CuCl 2 →ลูกบาศ์ก(OH) 2 →CuO→Cu
1 . ชุดพันธุกรรมของอโลหะ ซึ่งกรดที่ละลายได้ทำหน้าที่เป็นตัวเชื่อมในชุด ห่วงโซ่ของการเปลี่ยนแปลงสามารถแสดงได้ดังนี้:
อโลหะ→กรดออกไซด์→กรดที่ละลายน้ำได้→เกลือ
ตัวอย่างเช่น P→P 2 โอ 5 →ฮ 3 ป 4 →นะ 3 ป 4
2 . ชุดพันธุกรรมของอโลหะ ซึ่งกรดที่ไม่ละลายน้ำทำหน้าที่เป็นตัวเชื่อมในซีรีส์:
อโลหะ→กรดออกไซด์→เกลือ→กรด→
→กรดออกไซด์→อโลหะ
ตัวอย่างเช่น,ซิ→ SiO 2 → นา 2 SiO 3 → ชม 2 SiO 3 → SiO 2 → ซิ

การอภิปรายด้านหน้าเกี่ยวกับ:
การเชื่อมโยงทางพันธุกรรมคืออะไร การเชื่อมโยงทางพันธุกรรม เป็นความเชื่อมโยงระหว่างชั้นต่าง ๆ ตามการเปลี่ยนแปลงร่วมกัน ชุดพันธุกรรมคืออะไร?
ชุดพันธุกรรม - สารจำนวนหนึ่ง - ตัวแทน คลาสต่างๆซึ่งเป็นสารประกอบของหนึ่ง องค์ประกอบทางเคมีเชื่อมโยงกันด้วยการเปลี่ยนแปลงร่วมกันและสะท้อนถึงการเปลี่ยนแปลงของสารเหล่านี้ แถวเหล่านี้อิงตามองค์ประกอบเดียวกัน
อนุกรมทางพันธุกรรมประเภทใดที่มักจะแยกแยะ ระหว่างโลหะ อนุกรมสองประเภทสามารถแยกแยะได้:
ก) ชุดพันธุกรรมที่ด่างทำหน้าที่เป็นฐาน ชุดนี้สามารถแสดงได้โดยใช้การแปลงต่อไปนี้:
โลหะ → ออกไซด์พื้นฐาน → ด่าง → เกลือ
ตัวอย่างเช่น ชุดพันธุกรรมโพแทสเซียม K → K 2 O → เกาะ → KCl
b) อนุกรมทางพันธุกรรม โดยที่เบสที่ไม่ละลายน้ำทำหน้าที่เป็นเบส จากนั้นอนุกรมนี้สามารถแทนด้วยสายโซ่แห่งการเปลี่ยนแปลง:
โลหะ → ออกไซด์พื้นฐาน → เกลือ → เบสที่ไม่ละลายน้ำ → ออกไซด์พื้นฐาน → โลหะ
เช่น Cu → CuO → CuCl 2 → ลูกบาศ์ก(OH) 2 → CuO → Cu
ในบรรดาอโลหะนั้น ซีรีส์สองประเภทสามารถแยกแยะได้:
ก) ชุดพันธุกรรมของอโลหะ ซึ่งกรดที่ละลายได้ทำหน้าที่เป็นตัวเชื่อมในชุด ห่วงโซ่ของการเปลี่ยนแปลงสามารถแสดงได้ดังนี้: อโลหะ → กรดออกไซด์ → กรดที่ละลายน้ำได้ → เกลือ
ตัวอย่างเช่น: P → P 2 โอ 5 → ฮ 3 ป 4 →นะ 3 ป 4
b) ชุดพันธุกรรมของอโลหะ ซึ่งกรดที่ไม่ละลายน้ำทำหน้าที่เป็นตัวเชื่อมในอนุกรมต่อไปนี้ อโลหะ → กรดออกไซด์ → เกลือ → กรด → กรดออกไซด์ → อโลหะ
ตัวอย่างเช่น Si → SiO 2 → นา 2 SiO 3 → ฮ 2 SiO 3 → SiO 2 → ซี
ทำงานให้เสร็จตามตัวเลือก:
1. เลือกสูตรของออกไซด์ในเวอร์ชันของคุณ อธิบายตัวเลือกของคุณ ตามความรู้เกี่ยวกับคุณลักษณะขององค์ประกอบ ชั้นเรียนนี้การเชื่อมต่อ ตั้งชื่อพวกเขา
2. ในคอลัมน์ของสูตรที่คุณเลือก ให้ค้นหาสูตรของกรดและอธิบายตัวเลือกของคุณตามการวิเคราะห์องค์ประกอบของสารประกอบเหล่านี้
3. กำหนดความจุของกรดตกค้างในองค์ประกอบของกรด
4. เลือกสูตรเกลือและตั้งชื่อ
5. ทำสูตรเกลือที่สามารถสร้างได้จากแมกนีเซียมและกรดที่คุณเลือก เขียนชื่อพวกเขา
6. ในคอลัมน์สูตรที่คุณเลือก ค้นหาสูตรพื้นฐานและอธิบายตัวเลือกของคุณตามการวิเคราะห์องค์ประกอบของสารประกอบเหล่านี้
7. ในเวอร์ชันของคุณ ให้เลือกสูตรของสารที่สารละลายของกรดฟอสฟอริก (ไฮโดรคลอริก ซัลฟิวริก) สามารถทำปฏิกิริยาได้ เขียนสมการปฏิกิริยาที่เหมาะสม
9. ในบรรดาสูตรที่คุณเลือก ให้เลือกสูตรของสารที่สามารถโต้ตอบกันได้ เขียนสมการปฏิกิริยาที่เหมาะสม
10. สร้างห่วงโซ่ของพันธะทางพันธุกรรมของสารประกอบอนินทรีย์ซึ่งจะรวมถึงสารที่มีสูตรในเวอร์ชันของคุณเป็นอันดับหนึ่ง
ตัวเลือกที่ 1
ตัวเลือก 2
CaO
HNO 3
เฟ(OH) 3
นู๋ 2 โอ
สังกะสี(NO 3 ) 2
Cr(OH) 3
ชม 2 ดังนั้น 3
ชม 2 ส
PbO
LiOH
Ag 3 ป 4
พี 2 โอ 5
NaOH
ZnO
CO 2
BaCl 2
HCl
ชม 2 CO 3
ชม 2 ดังนั้น 4
CuSO 4
จากสารเหล่านี้สร้างชุดพันธุกรรมโดยใช้สูตรทั้งหมด เขียนสมการปฏิกิริยาซึ่งคุณสามารถดำเนินการเปลี่ยนรูปแบบนี้:
ฉันตัวเลือก: ZnSO 4, Zn, ZnO, Zn, Zn(OH) 2 : IIตัวเลือก:นา 2 ดังนั้น 4, NaOH, นา, นา 2 โอ 2 , นา 2 โอ
4) แก้ไข1.อัล→ อัล 2 โอ 3 → AlCl 3 → อัล( โอ้) 3 → อัล 2 โอ 3
2. พี→ พี 2 โอ 5 → ชม 3 ป 4 → นา 3 ป 4 → Ca 3 ( ป 4 ) 2
3. Zn→ZnCl 2 →สังกะสี (OH) 2 →ZnO→Zn(NO 3 ) 2
4.Cu→CuO→CuCl 2 →ลูกบาศ์ก(OH) 2 →CuO→Cu
5.น 2 โอ 5 →HNO 3 →เฟ(NO 3 ) 2 →เฟ(OH) 2 →FeS→FeSO 4
5)การบ้าน: แผนภูมิ การเปลี่ยนแปลงอย่างค่อยเป็นค่อยไปจากแคลเซียมเป็นแคลเซียมคาร์บอเนตและจัดทำรายงานการใช้เกลือทางการแพทย์ (โดยใช้เอกสารประกอบ)
คำแนะนำสำหรับนักเรียนในหลักสูตรโต้ตอบ "เคมีทั่วไปสำหรับเกรด 12" 1. ประเภทของนักเรียน: เอกสารสำหรับการนำเสนอนี้สำหรับนักเรียน การศึกษาด้วยตนเองหัวข้อ "สารและคุณสมบัติ" จากหลักสูตรเคมีทั่วไปเกรด 12 2. เนื้อหาหลักสูตร: ประกอบด้วยการนำเสนอหัวข้อ 5 หัวข้อ แต่ละหัวข้อการเรียนรู้มีโครงสร้างที่ชัดเจน สื่อการศึกษาในหัวข้อเฉพาะ สไลด์สุดท้ายคือการทดสอบการควบคุม - งานเพื่อการควบคุมตนเอง 3. ระยะเวลาการศึกษาสำหรับหลักสูตรนี้: ตั้งแต่หนึ่งสัปดาห์ถึงสองเดือน (กำหนดเป็นรายบุคคล) 4. การควบคุมความรู้: นักเรียนจัดทำรายงานความคืบหน้า รายการทดสอบ- แผ่นงานพร้อมตัวเลือกสำหรับงานที่ระบุหัวข้อ 5. การประเมินผลลัพธ์: "3" - 50% ของงานที่ทำเสร็จแล้ว "4" - 75%, "5"% ของงาน 6. ผลการเรียนรู้: ผ่าน (ล้มเหลว) ของหัวข้อที่ศึกษา


สมการปฏิกิริยา: 1. 2Cu + o 2 2CuO copper (II) ออกไซด์ 2. CuO + 2 HCl CuCl 2 + H 2 O copper (II) คลอไรด์ 3. CuCl NaOH Cu (OH) Na Cl copper (II) ไฮดรอกไซด์ 4. Cu (OH) 2 + H 2 SO 4 CuSO 4 + 2H 2 O คอปเปอร์ (II) ซัลเฟต



ชุดพันธุกรรมของสารประกอบอินทรีย์ หากเป็นพื้นฐานของชุดพันธุกรรม ไม่ เคมีอินทรีย์เป็นสารที่เกิดจากองค์ประกอบทางเคมีหนึ่งชนิด จากนั้นพื้นฐานของชุดพันธุกรรมในเคมีอินทรีย์จะประกอบด้วยสารที่มี เบอร์เดียวกันอะตอมของคาร์บอนในโมเลกุล

รูปแบบปฏิกิริยา: แต่ละหมายเลขเหนือลูกศรสอดคล้องกับสมการปฏิกิริยาเฉพาะ: เอทานอล เอทานอล เอเธน อีเทน คลอโรอีเทน เอธิน กรดอะซิติก (เอทาโนอิก)

สมการปฏิกิริยา: 1. C 2 H 5 Cl + H 2 O C 2 H 5 OH + HCl 2. C 2 H 5 OH + O CH 3 CH O + H 2 O 3. CH 3 CH O + H 2 C 2 H 5 OH 4. C 2 H 5 OH + HCl C 2 H 5 Cl + H 2 O 5. C 2 H 5 Cl C 2 H 4 + HCl 6. C 2 H 4 C 2 H 2 + H 2 7. C 2 H 2 + H 2 O CH 3 CH O 8. CH 3 CH O + Ag 2 O CH 3 COOH + Ag

ความเชื่อมโยงทางพันธุกรรมเป็นความสัมพันธ์ระหว่างสารที่อยู่ในจำพวกต่างๆ
คุณสมบัติหลักของชุดพันธุกรรม:
1. สารทั้งหมดในชุดเดียวกันต้องเกิดจากองค์ประกอบทางเคมีเดียว
2. สารที่เกิดจากองค์ประกอบเดียวกันจะต้องอยู่ในกลุ่มสารเคมีที่ต่างกัน
3. สารที่ก่อตัวเป็นอนุกรมทางพันธุกรรมขององค์ประกอบต้องเชื่อมโยงถึงกันด้วยการเปลี่ยนแปลงร่วมกัน
ทางนี้, พันธุกรรมระบุชื่อสารจำนวนหนึ่งซึ่งเป็นตัวแทนของสารประกอบอนินทรีย์ประเภทต่างๆ เป็นสารประกอบที่มีองค์ประกอบทางเคมีเดียวกัน เชื่อมต่อกันด้วยการแปลงระหว่างกัน และสะท้อนถึงต้นกำเนิดทั่วไปของสารเหล่านี้
สำหรับโลหะ สารที่เกี่ยวกับพันธุกรรมสามแถวมีความโดดเด่น สำหรับอโลหะ - หนึ่งแถว
1. ชุดพันธุกรรมของโลหะที่มีไฮดรอกไซด์เป็นเบส (อัลคาลิส):
โลหะ→ออกไซด์พื้นฐาน→ฐาน (ด่าง)→เกลือ.
ตัวอย่างเช่น ชุดพันธุกรรมของแคลเซียม:
Ca → CaO → Ca(OH) 2 → CaCl 2
2. ชุดพันธุกรรมของโลหะที่ก่อตัวเป็นแอมโฟเทอริกไฮดรอกไซด์:
เกลือ
โลหะ→แอมโฟเทอริกออกไซด์→(เกลือ)→แอมโฟเทอริกไฮดรอกไซด์
ตัวอย่างเช่น: ZnCl 2
Zn → ZnO → ZnSO 4 → Zn(OH) 2
(H 2 ZnO 2) ↓
นา 2 ZnO 2
ซิงค์ออกไซด์ไม่ทำปฏิกิริยากับน้ำดังนั้นก่อนอื่นจะได้เกลือจากนั้นจึงซิงค์ไฮดรอกไซด์ ทำเช่นเดียวกันหากโลหะตรงกับฐานที่ไม่ละลายน้ำ
3. ชุดพันธุกรรมของอโลหะ (อโลหะมีเฉพาะออกไซด์ที่เป็นกรด):
อโลหะ→กรดออกไซด์→กรด→เกลือ
ตัวอย่างเช่น ชุดพันธุกรรมของฟอสฟอรัส:
P → P 2 O 5 → H 3 PO 4 → K 3 PO 4
การเปลี่ยนจากสารหนึ่งไปยังอีกสารหนึ่งทำได้โดยใช้ปฏิกิริยาเคมี