Пригнічення агрегації тромбоцитів що це. Лікарські препарати, що впливають на судинно-тромбоцитарний гемостаз Агрегацію тромбоцитів гальмує блокатор ca2
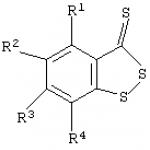
Винахід відноситься до фізіології, фармакології та медичної хімії, зокрема до вдосконаленого способу інгібування агрегації тромбоцитів. Поставлена мета досягається описаним удосконаленим способом інгібування агрегації тромбоцитів з використанням серовмісних гетероциклічних сполук, що полягає в тому, що в якості сірковмісних гетероциклічних сполук використовують відомі бензо-1,2-дитіол-3-тіон (БДТТ) або його вироби
 де R 1 -R 4 =Н або 1-4 -алкіл. Технічний результат: дозволяє більш ефективно інгібувати агрегацію тромбоцитів в умовах in vitro. Винахід відноситься до фізіології, фармакології та медичної хімії, зокрема, до вдосконаленого способу інгібування агрегації тромбоцитів. багатьох серцево-судинних захворювань (напр., таких як артеріальні тромбози, інфаркт міокарда, нестабільна стенокардія). З'єднання, здатні запобігати активації тромбоцитів, яка може бути викликана ендогенними індукторами (напр., аденозин-5'-дифосфатом /АДФ/), в даний час знаходять широке застосування для ефективного впливу на патологічні зміни системи гемостазу (Б.А.Сидоренко, Д .В.Преображенський. Клінічне застосування антитромботичних препаратів. - М., 1998). ,5,6,7-тетрагідротієнопіридин (тіклопідін) формули I
де R 1 -R 4 =Н або 1-4 -алкіл. Технічний результат: дозволяє більш ефективно інгібувати агрегацію тромбоцитів в умовах in vitro. Винахід відноситься до фізіології, фармакології та медичної хімії, зокрема, до вдосконаленого способу інгібування агрегації тромбоцитів. багатьох серцево-судинних захворювань (напр., таких як артеріальні тромбози, інфаркт міокарда, нестабільна стенокардія). З'єднання, здатні запобігати активації тромбоцитів, яка може бути викликана ендогенними індукторами (напр., аденозин-5'-дифосфатом /АДФ/), в даний час знаходять широке застосування для ефективного впливу на патологічні зміни системи гемостазу (Б.А.Сидоренко, Д .В.Преображенський. Клінічне застосування антитромботичних препаратів. - М., 1998). ,5,6,7-тетрагідротієнопіридин (тіклопідін) формули I  є антагоністом Р 2T рецепторів АДФ тромбоцитів (патент США №4963559, кл. 514-301, oп. 1990). Показано також, що блокатор кальцієвих каналів - D-цис-3-ацетокси-2,3-дигідро-5- -(2-метоксифеніл)-1,5-бензотіазепін-4(5Н)-вона гідрохлорид (дилтіазем) формули II
є антагоністом Р 2T рецепторів АДФ тромбоцитів (патент США №4963559, кл. 514-301, oп. 1990). Показано також, що блокатор кальцієвих каналів - D-цис-3-ацетокси-2,3-дигідро-5- -(2-метоксифеніл)-1,5-бензотіазепін-4(5Н)-вона гідрохлорид (дилтіазем) формули II  має антитромботичну дію (A.R.Dehpour, T.Samadian et al. "Effects of diltiazem and verapamil on ADP-induced rabbit platelet shape change and aggregation" Gen. Pharmacol, 1995, v.26, №6, p.1295-129 Вищевказані сполуки в умовах in vitro інгібували агрегацію тромбоцитів, спричинену АДФ, при концентрації >300 мкМ.
має антитромботичну дію (A.R.Dehpour, T.Samadian et al. "Effects of diltiazem and verapamil on ADP-induced rabbit platelet shape change and aggregation" Gen. Pharmacol, 1995, v.26, №6, p.1295-129 Вищевказані сполуки в умовах in vitro інгібували агрегацію тромбоцитів, спричинену АДФ, при концентрації >300 мкМ.  де R 1 R 4 =H або C 1-6 -алкіл, бензоїл, (заміщена) аміносульфонільна група та ін., як продукти органічного синтезу (Європейський патент №0043936, oп. 1981 ). .Найближчим до описуваного є відомий спосіб інгібування агрегації тромбоцитів шляхом введення в середу, що містить дані клітини, серусодержащих гетероциклічних сполук - заміщених 3,4-дигідро-1,2-дитиин-2-оксидів. Зокрема, зазначений спосіб приводив до зниження тромбоцитів при використанні 3,4-дигідро-3-вініл-1,2-дитиин-2-оксиду формули IV
де R 1 R 4 =H або C 1-6 -алкіл, бензоїл, (заміщена) аміносульфонільна група та ін., як продукти органічного синтезу (Європейський патент №0043936, oп. 1981 ). .Найближчим до описуваного є відомий спосіб інгібування агрегації тромбоцитів шляхом введення в середу, що містить дані клітини, серусодержащих гетероциклічних сполук - заміщених 3,4-дигідро-1,2-дитиин-2-оксидів. Зокрема, зазначений спосіб приводив до зниження тромбоцитів при використанні 3,4-дигідро-3-вініл-1,2-дитиин-2-оксиду формули IV  при порівняно високих концентраціях (напр., в умовах in vitro для даної сполуки IС 50 =100 мкМ) (патент Японії 02204487, C 07 D 339/08, оп. 1991, Chem. Abstr., 1991, v. 114, p. 6523s - прототип).Целью изобретения является разработка более эффективного способа ингибирования агрегации тромбоцитов.Поставленная цель достигается описываемым способом ингибирования агрегации тромбоцитов путем введения в среду, содержащую данные клетки, серусодержащих гетероциклических соединений, отличающимся тем, что в качестве полисернистых гетероциклических соединений используют известные БДТТ или його похідні вищевказаної загальної формули III, де R 1 -R 4 мають наведені значення. Сполуки загальної формули III були отримані відомим способом - взаємодією відповідного незаміщеного або заміщеного о-хлор- або о-бромбензилхлориду або броміду з сіркою при температурі 50-20 моноалкілового ефіру гліколю в присутності алкоголю лужного металу .Описуваний винахід ілюструється наступними прикладами.Приклад 1. Інгібування агрегації тромбоцитів людини під дією БДТТ і її похідних.Вплив продуктів цього винаходу на агрегацію тромбоцитів Для цього венозну кров, взяту о 8 годині ранку у здорових донорів, центрифугували при 450 g при кімнатній температурі в пластиковому посуді протягом 10 хв, використовуючи як антикоагулянт цитрат натрію. Супернатант, тобто багату на тромбоцити плазму, відбирали і центрифугували при 650 g протягом 30 хв, отримуючи бідну на тромбоцити плазму. Концентрацію тромбоцитів доводили в багатій на тромбоцити плазмі до 2,510 8 клітин/мл за допомогою розведення бідної на тромбоцити плазмою і приливали отриману суспензію в кювету об'ємом 0,5 мл. Агрегацію індукували додаванням АДФ до концентрації 20 мкМ. Концентрацію АДФ підбирали у кожному експерименті так, щоб агрегація була оборотною, і максимум припадав на 2 хв після додавання АДФ, не перевищуючи 50%. Світлорозсіювання суспензії тромбоцитів вимірювали за допомогою агрегометра, розробленого на біологічному факультеті МДУ ім. М.В. Ломоносова. Досліджувану сполуку (у вигляді водного розчину, при необхідності, що містить ДМСО до 0,2%) додавали в пробу до внесення індуктора агрегації (АДФ). ефективна дія спостерігалася при концентрації<30 мкМ. В частности, значение концентрации, при которой достигалось полумаксимальное ингибирование, (IC 50) для БДТТ составляло 6,4 мкМ. Согласно данным прототипа, для известного аналога (3,4-дигидро-3-винил-1,2-дитиин-2-оксида) в условиях in vitro IC 50 имела значение 100 мкМ.Пример 2. Острая токсичность БДТТ и его производных.Острую токсичность соединений настоящего изобретения определяли известным способом по ЛД 50 с использованием беспородных мышей обоего пола средней массой 21 г при комнатной температуре; стандартное питание и воду давали ad libitum в течение всего эксперимента; подвижность животных не ограничивали. Растворы соединений в ДМСО вводили с помощью стерильного шприца внутрибрюшинно. После инъекции за животными вели наблюдение в течение 48 ч по истечении этого времени за мышами наблюдали дополнительно в течение 72 ч (ни одно из животных не погибло в течение дополнительного промежутка времени). Полученные результаты свидетельствуют о том, что значение ЛД 50 для БДТТ составляет >100 мг/кг, а для його похідних не нижче 50 мг/кг.Дані, наведені в прикладі 1, показують, що описуваний спосіб дозволяє інгібувати агрегацію тромбоцитів в умовах in vitro більш ефективно порівняно з відомим способом.
при порівняно високих концентраціях (напр., в умовах in vitro для даної сполуки IС 50 =100 мкМ) (патент Японії 02204487, C 07 D 339/08, оп. 1991, Chem. Abstr., 1991, v. 114, p. 6523s - прототип).Целью изобретения является разработка более эффективного способа ингибирования агрегации тромбоцитов.Поставленная цель достигается описываемым способом ингибирования агрегации тромбоцитов путем введения в среду, содержащую данные клетки, серусодержащих гетероциклических соединений, отличающимся тем, что в качестве полисернистых гетероциклических соединений используют известные БДТТ или його похідні вищевказаної загальної формули III, де R 1 -R 4 мають наведені значення. Сполуки загальної формули III були отримані відомим способом - взаємодією відповідного незаміщеного або заміщеного о-хлор- або о-бромбензилхлориду або броміду з сіркою при температурі 50-20 моноалкілового ефіру гліколю в присутності алкоголю лужного металу .Описуваний винахід ілюструється наступними прикладами.Приклад 1. Інгібування агрегації тромбоцитів людини під дією БДТТ і її похідних.Вплив продуктів цього винаходу на агрегацію тромбоцитів Для цього венозну кров, взяту о 8 годині ранку у здорових донорів, центрифугували при 450 g при кімнатній температурі в пластиковому посуді протягом 10 хв, використовуючи як антикоагулянт цитрат натрію. Супернатант, тобто багату на тромбоцити плазму, відбирали і центрифугували при 650 g протягом 30 хв, отримуючи бідну на тромбоцити плазму. Концентрацію тромбоцитів доводили в багатій на тромбоцити плазмі до 2,510 8 клітин/мл за допомогою розведення бідної на тромбоцити плазмою і приливали отриману суспензію в кювету об'ємом 0,5 мл. Агрегацію індукували додаванням АДФ до концентрації 20 мкМ. Концентрацію АДФ підбирали у кожному експерименті так, щоб агрегація була оборотною, і максимум припадав на 2 хв після додавання АДФ, не перевищуючи 50%. Світлорозсіювання суспензії тромбоцитів вимірювали за допомогою агрегометра, розробленого на біологічному факультеті МДУ ім. М.В. Ломоносова. Досліджувану сполуку (у вигляді водного розчину, при необхідності, що містить ДМСО до 0,2%) додавали в пробу до внесення індуктора агрегації (АДФ). ефективна дія спостерігалася при концентрації<30 мкМ. В частности, значение концентрации, при которой достигалось полумаксимальное ингибирование, (IC 50) для БДТТ составляло 6,4 мкМ. Согласно данным прототипа, для известного аналога (3,4-дигидро-3-винил-1,2-дитиин-2-оксида) в условиях in vitro IC 50 имела значение 100 мкМ.Пример 2. Острая токсичность БДТТ и его производных.Острую токсичность соединений настоящего изобретения определяли известным способом по ЛД 50 с использованием беспородных мышей обоего пола средней массой 21 г при комнатной температуре; стандартное питание и воду давали ad libitum в течение всего эксперимента; подвижность животных не ограничивали. Растворы соединений в ДМСО вводили с помощью стерильного шприца внутрибрюшинно. После инъекции за животными вели наблюдение в течение 48 ч по истечении этого времени за мышами наблюдали дополнительно в течение 72 ч (ни одно из животных не погибло в течение дополнительного промежутка времени). Полученные результаты свидетельствуют о том, что значение ЛД 50 для БДТТ составляет >100 мг/кг, а для його похідних не нижче 50 мг/кг.Дані, наведені в прикладі 1, показують, що описуваний спосіб дозволяє інгібувати агрегацію тромбоцитів в умовах in vitro більш ефективно порівняно з відомим способом.
формула винаходу
Спосіб інгібування агрегації тромбоцитів шляхом введення в середу, що містить дані клітини, серусодержащих гетероциклічних сполук, який відрізняється тим, що як серусодержащих гетероциклічних сполук застосовують бензо-1,2-дитіол-3-тіон і його похідні загальної формули  де R 1 -R 4 - Н або 1-4 - алкіл.
де R 1 -R 4 - Н або 1-4 - алкіл.
Схожі патенти:
Винахід відноситься до органічної хімії та фармакології, а саме до суміші ізомерів калієвої солі 2-оцтової кислоти в мольному співвідношенні 1:3, що виявляє кардіотонічну активність
Система гемостазу виконує в організмі такі основні функції:
Підтримує кров у судинах у рідкому стані, що необхідно для нормального кровопостачання органів та тканин;
Забезпечує зупинку кровотечі при пошкодженні судинної стінки.
Зупинка кровотечі (гемостаз - від грецької hemo- Кров, stasis- зупинка) досягається за участю кількох механізмів. Після пошкодження судинної стінки виникає спазм судин. Ця негайна реакція на травму може зупинити кровотечу лише за незначних ушкоджень дрібних судин. В основному зупинка кровотечі досягається завдяки утворенню тромбів, які перешкоджають крововтраті, закриваючи місце ушкодження. Таке локальне утворення тромбів (гемостатичних пробок) при ушкодження судин є захисною реакцією.
Однак за певних умов тромби утворюються всередині судин, закриваючи їх просвіт і перешкоджаючи нормальному кровотоку. Внутрішньосудинне утворення тромбів може відбуватися за патологічних змін ендотелію судин, включаючи його ушкодження, пов'язані з атеросклерозом, підвищенням артеріального тиску або іншими факторами. Причиною утворення тромбів можуть бути аномальні зміни кровотоку (наприклад, зниження його швидкості) або недостатність деяких білків, що перешкоджають тромбоутворенню.
Тромбоутворення відбувається за участю двох основних процесів: агрегації тромбоцитів та зсідання крові (гемокоагуляції).
Агрегація тромбоцитів - це поєднання тромбоцитів у конгломерати (агрегати) різної величини та щільності. Цей процес ініціюється при пошкодженні судинної стінки. У місці ушкодження тромбоцити спочатку зв'язуються з фактором Віллебранда та колагеном субендотеліального шару (відбувається адгезія тромбоцитів).Взаємодія з колагеном спричиняє активацію тромбоцитів (рис. 27-1). При цьому самі тромбоцити стають джерелами речовин, що стимулюють агрегацію, таких як тромбоксан A 2 АДФ,
серотонін. Тромбін, який утворюється локально у процесі згортання крові, також індукує агрегацію тромбоцитів. Крім того, індукторами агрегації є катехоламіни, фактор активації тромбоцитів та деякі інші ендогенні речовини.
Агрегації тромбоцитів перешкоджають простациклін та ендотеліальний релаксуючий фактор, які утворюються клітинами ендотелію судин та вивільняються у кровотік. При пошкодженні ендотеліальних клітин синтез цих речовин знижується і на такому фоні дія речовин, що стимулюють агрегацію, домінує. В результаті тромбоцити поєднуються в агрегати, з яких формується тромбоцитарний тромб.
Тромбоцитарний тромб стає міцнішим завдяки ниткам фібрину, який утворюється в процесі згортання крові.Основні учасники цього процесу – білки плазми крові, звані факторами згортання крові.
Плазмові фактори згортання синтезуються в печінці та циркулюють у крові у неактивній формі. При пошкодженні судинної стінки відбувається швидка активація фактора VII за участю тканинного фактора- трансмембранного білка, який синтезується різними клітинами (у тому числі активованими ендотеліальними клітинами) та в нормі з кров'ю не контактує. Експресія тканинного фактора на поверхні клітин при пошкодженні ендотелію значно прискорює активацію фактора VII (перетворення його на фактор VIIa) у присутності іонів Са 2+ . Під дією фактора VIIa (у комплексі з тканинним фактором) відбувається послідовна активація інших факторів згортання крові (IX та X) у складній аутокаталітичній системі, яка називається каскадом згортання крові. В результаті під дією фактора Xa утворюється тромбін (фактор На), який перетворює циркулюючий в крові розчинний білок фібриноген (фактор I) на нерозчинний фібрин (рис. 27-5). Фібрин полімеризується і заповнюючи простір між тромбоцитами, зміцнює тромбоцитарний тромб. Фібринові нитки пронизують тромб, утворюючи мережу, яка затримує еритроцити, що циркулюють в крові. Відбувається формування червоного тромбу.
Згортанню крові протидіють речовини, які є природними інгібіторами активних факторів згортання крові.
Активація фактора Х під дією фактора VIIa перешкоджає інгібітор шляху тканинного фактора,синтезований ендотеліальними
клітинами. Інгібітором тромбіну та деяких інших активних факторів згортання (Xa, IXa XIa, XIIa) є антитромбін III- Білок, що циркулює в плазмі крові, який діє в комплексі з гепарином або гепариноподібними речовинами (присутні на поверхні неушкоджених ендотеліальних клітин). Ці речовини багаторазово прискорюють інактивацію факторів згортання крові під дією антитромбіну III.
Інгібітор необхідних для утворення тромбіну факторів VIIIa та Va - активований протеїн C.Цей білок синтезується в печінці за участю вітаміну K, циркулює в крові в неактивній формі та активується під дією тромбіну на поверхні неушкоджених ендотеліальних клітин. Активація протеїну C збільшується при надмірному утворенні тромбіну. При локальному утворенні тромбів у місці ушкодження судинної стінки вищезгадані інгібітори сприяють підтримці крові в рідкому стані, перешкоджаючи зростанню тромбу всередині судини.
Агрегація тромбоцитів та згортання крові взаємопов'язані. Переважання того чи іншого процесу в механізмі тромбоутворення залежить від калібру судини та швидкості кровотоку. Агрегація тромбоцитів має значення для формування тромбів за високої швидкості кровотоку, тобто. у артеріях. У венозних судинах, де швидкість кровотоку невелика, переважає процес зсідання крові.
Подальша доля тромбу залежить від активності фібринолітичної системи. Якщо ця система працює нормально, відбувається поступове розчинення фібрину (фібриноліз) за участю ферменту плазміну, який утворюється з неактивного попередника (плазміногену) під впливом активаторів. Дію плазміну перешкоджають циркулюючі в крові антиплазміни. Активатори плазміногену нейтралізуються специфічними інгібіторами.
Порушення процесів агрегації тромбоцитів та зсідання крові та/або підвищення активності фібринолітичної системи можуть призвести до кровоточивості, а надмірна активація цих процесів або пригнічення фібринолізу – до виникнення внутрішньосудинних тромбів (тромбозу). В результаті тромбозу артеріальних судин зменшується приплив крові до тканин і розвивається їхня ішемія. Наслідком ішемії є загибель клітин (некроз). Тромбози можуть бути причиною таких тяжких ускладнень як інфаркт міокарда (тромбоз коронарних артерій), ішемічний інсульт (тромбоз судин мозку) і т.д. Венозні тромбози можуть бути причиною емболії легеневої артерії.
Для попередження тромбозів використовують речовини, які пригнічують агрегацію тромбоцитів і згортання крові, таким чином перешкоджаючи утворенню тромбів. При тромбозах використовують також речовини, що викликають лізис тромбів, – тромболітичні (фібринолітичні) засоби.
Для зупинки кровотеч застосовують засоби, що підвищують згортання крові, та засоби, що пригнічують фібриноліз. Вибір тих чи інших засобів залежить від причини кровотечі.
Практичне значення мають такі групи засобів, які впливають тромбообразование.
Засоби, що знижують агрегацію тромбоцитів(антиагреганти).
Кошти, що впливають на згортання крові.
Кошти, що знижують згортання крові (антикоагулянти).
Засоби, що підвищують зсідання крові (гемостатики).
Кошти, що впливають на фібриноліз.
Фібринолітичні (тромболітичні) засоби.
Антифібринолітичні засоби (інгібітори фібринолізу).
27.1. ЗАСОБИ, ЗНИЖУЮЧІ АГРЕГАЦІЮ ТРОМБОЦИТІВ (АНТИАГРЕГАНТИ)
Тромбоцити – невеликі за розміром формові елементи крові дископодібної форми утворюються як фрагменти мегакаріоцитів кісткового мозку. Тромбоцити циркулюють у крові протягом 6-12 днів, а потім захоплюються тканинними макрофагами.
Ендотелій судин впливає на функціональну активність тромбоцитів. Ендотеліальні клітини виділяють у кровотік простациклін (простагландин I 2) та ендотеліальний релаксуючий фактор, який ідентифікують з оксидом азоту - NO. Ці речі перешкоджають агрегації тромбоцитів. Крім того, ендотеліальні клітини секретують речовини, що зменшують згортання крові та сприяють лізису тромбу. Все це забезпечує антитромбогенні властивості неушкодженого ендотелію судин.
При пошкодженні ендотелію судин, що може бути викликано різними факторами (механічна травма, інфекції, атеросклеротичні зміни судинної стінки, підвищення артеріального тиску та ін.), антитромбогенні властивості ендотелію знижуються, що створює умови для формування тромбу. Порушується синтез простацикліну та ендотеліального релаксуючого фактора і це полегшує контакт
тромбоцитів із пошкодженою поверхнею ендотелію. Тромбоцити накопичуються в місці пошкодження і взаємодіють із субендотелією судин: безпосередньо або через фактор Віллебранда (його секретують активовані тромбоцити та ендотеліальні клітини) вони зв'язуються з колагеном та іншими білками субендотелію за участю специфічних глікопротеїнів, локалізованих у мембрані. Фактор Віллебранда зв'язується з глікопротеїном Ib, а колаген – з глікопротеїном Ia тромбоцитарної мембрани (див. рис. 27-1). Вплив колагену (а також тромбіну, який у невеликих кількостях утворюється локально вже на початковому етапі тромбоутворення) на тромбоцити викликає зміну їхнього стану – активацію. Тромбоцити змінюють свою форму (з дископодібних вони стають розпластаними з безліччю відростків – псевдоподій) та покривають пошкоджену поверхню судини.
При активації тромбоцити вивільняють різні біологічно активні речовини, що у неактивованих тромбоцитах перебувають у гранулах (α-гранули, щільні гранули). Щільні гранули є сховищем речовин, що стимулюють агрегацію тромбоцитів: АДФ та серотоніну. Вивільнення цих речовин із тромбоцитарних гранул відбувається внаслідок підвищення внутрішньоклітинної концентрації Са 2+ при дії на тромбоцити колагену, тромбіну та інших індукторів агрегації, у тому числі й самого АДФ. АДФ, що вивільняється в кровотік, стимулює специфічні (пуринергічні) рецептори, локалізовані в мембрані тромбоцитів. Через рецептори, пов'язані з G-білками (Р2Y12-пуринергічні рецептори), АДФ викликає пригнічення аденілатциклази та зниження рівня цАМФ, що призводить до підвищення рівня Са2 у цитоплазмі тромбоцитів (рис. 27-2).
Крім того, при активації тромбоцитів підвищується активність фосфоліпази А 2 тромбоцитарних мембран - ферменту, що бере участь в утворенні арахідонової кислоти з мембранних фосфоліпідів. У тромбоцитах з арахідонової кислоти під впливом циклооксигенази спочатку синтезуються циклічні ендопероксиди (простагландини G 2 /H 2), а з них за участю тромбоксансин-
Тетази утворюється тромбоксан А 2 - активний стимулятор агрегації тромбоцитів та вазоконстриктор. Після вивільнення в кровотік тромбоксан А2 стимулює тромбоксанові рецептори тромбоцитарних мембран. В результаті через пов'язані з цими рецепторами q -білки активується фосфоліпаза C і збільшується утворення
Мал.27-1. Адгезія та агрегація тромбоцитів при поваленні судинної стінки: ЕК – ендотеліальна клітина; ФВ – фактор фон Віллебранда; ТхА 2 - тромбоксан А 2; ПГІ 2 – простациклін; NO – ендотеліальний релаксуючий фактор; GP – глікопротеїни; GP llb/llla - глікопротеїни llb/llla (З: Katzung B.G. Bazic and Clinical Pharmacology - NY, 2001, з ізм.)
інозитол-1,4,5-трифосфату, що сприяє вивільненню Са 2+ з внутрішньоклітинного депо тромбоцитів (роль кальцієвого депо в тромбоцитах виконує система щільних трубочок). Це призводить до збільшення цитоплазматичної концентрації Са2+ (рис. 27-2). Тромбоксан А 2 викликає підвищення концентрації Са 2+ та у гладком'язових клітинах судин, що призводить до вазоконстрикції.

Мал. 27-2. Мехінізми дії антиагрегантів (ацетилсаліцилової кислоти, тиклопідину та епопростенолу): ЕК – ендотеліальна клітина; ФО - фосфоліпіди клітинних мемебран; АК - архідонова кислота; ФЛА 2 - фосфоліпаза А 2; ЦОГ – циклооксигеназа; ТС – тромбоксансинтетаза; ПС – простациклінсинтетаза; ПГG 2 /H 2 - циклічні ендопероксиди; ТхА 2 - тромбоксан А 2; ПГІ 2 – простациклін; АЦ – аденілатциклаза; ФЛС – фосфоліпаза С; IP 3 - інозитол-1, 4, 5-трифосфат
Таким чином, АДФ та тромбоксан А 2 підвищують рівень Са 2+ у цитоплазмі тромбоцитів. Цитоплазматичний Са 2+ викликає зміну конформації глікопротеїнів IIb/IIIa в мембрані тромбоцитів, внаслідок чого вони набувають здатності зв'язувати фібриноген. Одна молекула фібриногену має дві ділянки зв'язування для глікопротеїнів IIb/IIIa і таким чином може поєднати між собою два тромбоцити (рис. 27-3). Поєднання багатьох тромбоцитів фібриногеновими містками призводить до утворення тромбоцитарних агрегатів.
Протилежним чином агрегацію тромбоцитів впливає простациклін (простагландин I 2). Як і тромбоксан, простациклін
утворюється із циклічних ендопероксидів, але під дією іншого ферменту - простациклінсинтетази. Простациклін синтезується ендотеліальними клітинами і вивільняється в кровотік, де стимулює простациклінові рецептори в мембрані тромбоцитів і пов'язану з ними через G s-білок аденілатциклазу. В результаті в тромбоцитах підвищується рівень цАМФ та знижується концентрація цитоплазматичного Са 2+ (див. рис. 27-2). Це перешкоджає зміні конформації глікопротеїнів IIb/IIIa, і вони втрачають здатність зв'язувати фібриноген. Таким чином, простациклін попереджає агрегацію тромбоцитів. Під дією простацикліну знижується концентрація Са 2+ у клітинах гладком'язових судин, що призводить до розширення судин.

Можна виділити таку послідовність основних подій, що призводять до агрегації тромбоцитів (див. схему 27-1).
Основна спрямованість дії антиагрегантів, які нині застосовуються у клінічній практиці, пов'язана з усуненням дії тромбоксану А 2 та АДФ, а також із блокадою глікопротеїнів IIb/IIIa мембран тромбоцитів. Використовують також речовини іншого механізму дії, які підвищують концентрацію цАМФ у тромбоцитах і, отже, знижують концентрацію Са 2+ .
Виділяють такі групи засобів, що зменшують агрегацію тромбоцитів.
Засоби, що інгібують синтез тромбоксану A 2 . - інгібітори циклооксигенази:
ацетилсаліцилова кислота.

Схема 27.1. Механізм агрегації тробоцитів
Інгібітори циклооксигенази та тромбоксансинтетази: індобуфен.
Засоби, що стимулюють простациклінові рецептори:
епопростенол**.
Засоби, що перешкоджають дії АДФ на тромбоцити:
тиклопідін; клопідогрел.
Засоби, що інгібують фосфодіестеразу тромбоцитів:
дипіридамол
Засоби, які блокують глікопротеїни IIb/IIIa мембран тромбоцитів.
Моноклональні антитіла: абциксимаб.
Синтетичні блокатори глікопротеїнів IIb/IIIa: ептифібатид; тирофібан.
Засоби, що інгібують синтез тромбоксану A 2
Ацетилсаліцилова кислота (аспірин*) - відомий протизапальний, аналгетичний та жарознижувальний засіб. В даний час широко застосовується як антиагрегант. Антиагрегантну дію ацетилсаліцилової кислоти пов'язують із її інгібуючим впливом на синтез тромбоксану A 2 у тромбоцитах.
Ацетилсаліцилова кислота незворотно інгібує циклооксигеназу (викликає незворотне ацетилювання ферменту) і таким чином порушує утворення з арахідонової кислоти циклічних ендопероксидів, попередників тромбоксану A 2 та простагландинів. Тому під дією ацетилсаліцилової кислоти зменшується не тільки синтез тромбоксану A 2 у тромбоцитах, а й синтез простацикліну в ендотеліальних клітинах судин (див. рис. 27-2). Однак шляхом підбору відповідних доз і режиму застосування можна досягти переважної дії ацетилсаліцилової кислоти на синтез тромбоксану A 2 . Це пов'язано із суттєвими відмінностями між тромбоцитами та ендотеліальними клітинами.
Тромбоцити – без'ядерні клітини – не мають системи ресинтезу білка і, отже, не здатні синтезувати циклооксигеназу. Тому при необоротному інгібуванні цього ферменту порушення синтезу тромбоксану A 2 зберігається протягом усього життя тромбоциту, тобто. протягом 7-10 днів. Внаслідок утворення нових тромбоцитів антиагрегантна дія ацетилсаліцилової кислоти триває менший період часу, і тому для досягнення стабільного ефекту препарату (тобто стабільного зниження рівня тромбоксану) його рекомендують призначати 1 раз на добу.
У клітинах ендотелію судин відбувається ресинтез циклоксигенази, і активність цього ферменту відновлюється через кілька годин після прийому ацетилсаліцилової кислоти. Тому при призначенні препарату 1 раз на добу суттєвого зниження синтезу простацикліну не відбувається.

Крім того, ацетилсаліцилова кислота приблизно на 30% піддається пресистемному метаболізму в печінці, тому її концентрація в системному кровотоку нижча, ніж у портальній крові. В результаті на тромбоцити, що циркулюють у портальному кровотоку, ацетилсаліцилова кислота діє у більш високих концентраціях, ніж на ендотеліальні клітини системних судин. Тому для придушення синтезу тромбоксану A 2 у тромбоцитах необхідні менші дози ацетилсаліцилової кислоти, ніж для придушення синтезу простацикліну в клітинах ендотелію.
З цих причин при збільшенні дози та кратності призначення ацетилсаліцилової кислоти її пригнічує на синтез простацикліну стає більш вираженим, що може призвести до зменшення антиагрегантного ефекту. У зв'язку із зазначеними особливостями ацетилсаліцилову кислоту як антиагрегант рекомендують призначати у невеликих дозах (в середньому 100 мг) 1 раз на добу.
Як антиагрегант ацетилсаліцилову кислоту використовують при нестабільній стенокардії, для профілактики інфаркту міокарда, ішемічного інсульту та тромбозів периферичних судин, для запобігання утворенню тромбів при аортокоронарному шунтуванні та коронарній ангіопластикі. Ацетилсаліцилову кислоту призначають внутрішньо у дозах 75-160 мг (за окремими показаннями – в інтервалі доз від 50 до 325 мг) 1 раз на добу протягом тривалого часу. В даний час у розпорядженні лікарів є препарати ацетилсаліцилової кислоти, призначені для профілактики тромбозів, які містять 50-325 мг діючої речовини, у тому числі таблетки, вкриті кишковорозчинною оболонкою - Ацекардол * , Аспікор * , Кардіопірін * , Аспірин * , Тромбо АСС * та ін. Антиагрегантна дія ацетилсаліцилової кислоти настає швидко (протягом 20-30 хв). Лікарські форми з кишково-розчинною оболонкою починають діяти повільніше, проте при тривалому застосуванні їхня ефективність практично не відрізняється від ефективності звичайних таблеток. Для досягнення швидшого ефекту таблетки ацетилсаліцилової кислоти слід розжувати.
Основні побічні ефекти ацетилсаліцилової кислоти пов'язані з пригніченням циклооксигенази. При цьому порушується утворення простагландинів Е2 і I2, які мають антисекреторну та гастропротекторну дію (знижують секрецію хлористоводневої кислоти парієтальними клітинами шлунка, підвищують секрецію слизу та бікарбонатів). В результаті навіть при нетривалому застосуванні ацетилсаліцилова кислота може спричинити пошкодження епітелію шлунка та дванадцятипалої кишки (ульцерогенний ефект). Вплив на слизову оболонку шлунка менш виражено при використанні лікарських форм з кишковорозчинною оболонкою. При застосуванні ацетилсаліцилової кислоти можливі шлунково-кишкові кровотечі та інші геморагічні ускладнення. Ризик таких ускладнень нижче при призначенні ацетилсаліцилової кислоти в дозі 100 мг на добу та менше. Виборче інгібування ЦОГ призводить до активації ліпоксигеназного шляху перетворення арахідонової кислоти та утворення лейкотрієнів, що мають бронхоконстрикторні властивості. У хворих на бронхіальну астму ацетилсаліцилова кислота може провокувати початок нападу («аспіринова астма»). Можливі алергічні реакції.
Для зменшення ульцерогенної дії ацетилсаліцилової кислоти запропоновано комбінований препарат Кардіомагніл*, що містить гідроксид магнію. Гідроксид магнію нейтралізує хлористоводневу кислоту шлунка (антацидну дію), знижуючи її шкідливий вплив на слизову оболонку. Препарат застосовують за тими ж показаннями, що і ацетилсаліцилову кислоту, у тому числі для вторинної профілактики ішемічного інсульту.
Індобуфен (ібустрин *) зменшує синтез тромбоксану A 2 одночасно інгібуючи циклооксигеназу і тромбоксансинтетазу. На відміну від ацетилсаліцилової кислоти, індобуфен викликає оборотне інгібування циклооксигенази. При прийомі препарату відбувається відносне збільшення кількості простацикліну (збільшується співвідношення простациклін/тромбоксан A 2 ). Індобуфен пригнічує адгезію та агрегацію тромбоцитів. Показання до застосування та побічні ефекти такі ж, як у ацетилсаліцилової кислоти.
Засоби, що стимулюють простациклінові рецептори
Ще один шлях зменшення агрегації тромбоцитів – стимуляція простациклінових рецепторів. З цією метою використовують
препарат простацикліну е п о п о с т е н о л * . Дія простацикліну протилежна дії тромбоксану A 2 як на тромбоцити, а й у тонус судин. Він викликає вазодилатацію та зниження АТ. Цей ефект простацикліну використовують при легеневій гіпертензії. Так як простациклін швидко руйнується в крові (t 1/2 близько 2 хв) і тому діє нетривало, препарат вводять інфузійно. Через коротку дію епопростенол * не знайшов широкого застосування як антиагреганту. Можлива сфера використання антиагрегантної дії епопростенолу – профілактика агрегації тромбоцитів при екстракорпоральному кровообігу.
Засоби, що перешкоджають дії АДФ на тромбоцити
Тиклопідін (тиклід*) - похідне тієнопіридину, що інгібує агрегацію тромбоцитів, що викликається АДФ. Тиклопідін є проліками, його антиагрегантний ефект пов'язаний з утворенням активного метаболіту за участю мікросомальних ферментів печінки. Метаболіт тиклопідину містить тіолові групи, за допомогою яких він незворотно зв'язується з Р2Y12-пуринергічними рецепторами в мембрані тромбоцитів. Це призводить до усунення стимулюючої дії АДФ на тромбоцити та зниження концентрації цитоплазматичного Са 2+ . В результаті зменшується експресія глікопротеїнів IIb/IIIa у мембрані тромбоцитів та їх зв'язування з фібриногеном (див. рис. 27-2). Через незворотний характер дії тиклопідин має тривалий антиагрегантний ефект.
Максимальний ефект при постійному прийомі тиклопідину досягається через 7-11 днів (час, необхідний для утворення та розвитку дії активного метаболіту) і після відміни препарату зберігається протягом усього періоду життя тромбоцитів (7-10 днів).
Тиклопідин призначають для вторинної профілактики ішемічного інсульту, для запобігання тромбозу при облітеруючих захворюваннях нижніх кінцівок, при аортокоронарному шунтуванні та стентуванні коронарних артерій. Препарат ефективний при вживанні, призначають 2 рази на добу під час їди.
Застосування тиклопідину обмежено у зв'язку з його побічними ефектами. Можливі зниження апетиту, нудота, блювання, діарея (20%), біль у животі, шкірні висипання (11-14%). Позначено
підвищення у плазмі крові рівня атерогенних ліпопротеїнів. Кровоточивість - загальне ускладнення при використанні антиагрегантів. Небезпечним ускладненням є нейтропенія, яка трапляється протягом перших трьох місяців лікування у 1-2,4% хворих. Можливі тромбоцитопенія, агранулоцитоз, дуже рідко – апластична анемія. У зв'язку з цим протягом перших місяців лікування потрібний систематичний контроль картини крові.
Клопідогрел (плавікс*, зілт*) подібний до тиклопідину за хімічною структурою, основними ефектами та механізмом дії. Як і тиклопідин, є проліками і піддається перетворенню в печінці з утворенням активного метаболіту. Значне пригнічення агрегації тромбоцитів відмічено з другого дня лікування, максимальний ефект досягається через 4-7 днів. Після відміни препарату його дія зберігається протягом 7-10 днів. Клопідогрел перевершує тиклопідин за активністю - у добовій дозі 75 мг він викликає таке ж зниження агрегації тромбоцитів та подовження часу кровотечі, як і тиклопідин у добовій дозі 500 мг.

Застосовують клопідогрел за тими ж показаннями, що і ацетилсаліцилову кислоту, при її непереносимості. Приймають внутрішньо 1 раз на день незалежно від їди. Клопідогрел можна поєднувати з ацетилсаліциловою кислотою, тому що препарати інгібують різні механізми агрегації тромбоцитів і тому посилюють дію один одного (проте при такому поєднанні вище небезпека геморагічних ускладнень).
Порівняно з тиклопідином побічні ефекти клопідогрелу менш виражені (діарея – 4,5%, висип – 6%). Застосування клопідогрелу пов'язане з меншим ризиком виникнення такого серйозного ускладнення, як нейтропенія (0,1%), рідше виникає тромбоцитопенія. Як рідкісне ускладнення, як і при прийомі тиклопідину, можливий розвиток тромботичної тромбоцитопенічної пурпури.
Засоби, що інгібують фосфодіестеразу тромбоцитів
Дипіридамол (курантил, персантин) спочатку був запропонований як коронаророзширювальний засіб. Пізніше було виявлено його здатність пригнічувати агрегацію тромбоцитів. В даний час дипіридамол застосовують в основному як антиагрегант для профілактики тромбозів. Антиагрегантну дію дипіридамолу пов'язують із підвищенням рівня цАМФ у тромбоцитах, внаслідок чого у них знижується концентрація цитоплазматичного Ca 2+ . Відбувається це з кількох причин. По-перше, дипіридамол пригнічує фосфодіестеразу, яка інактивує цАМФ. Крім того, дипіридамол пригнічує захоплення аденозину ендотеліальними клітинами та еритроцитами та його метаболізм (інгібує аденозиндезаміназу), тим самим підвищуючи рівень аденозину в крові (рис. 27-4). Аденозин стимулює А 2 -рецептори тромбоцитів та підвищує активність пов'язаної з цими рецепторами аденілатциклази, в результаті в тромбоцитах збільшується утворення цАМФ та знижується рівень цитоплазматичного Ca 2+ . Дипіридамол також підвищує рівень цАМФ у клітинах гладком'язових судин, викликаючи вазорелаксацію.

Застосовують дипіридамол для профілактики ішемічного інсульту, а також при захворюваннях периферичних артерій (в основному в поєднанні з ацетилсаліциловою кислотою, оскільки сам дипіридамол має слабку антиагрегантну дію). Призначають внутрішньо 3-4 рази на день за 1 годину до їди. У поєднанні з пероральними антикоагулянтами дипіридамол призначають для попередження утворення тромбів при мітральному ваді серця.
При застосуванні дипіридамолу можливі головний біль, запаморочення, гіпотензія, диспептичні явища,
шкірні висипки. Небезпека кровотеч менша, ніж при застосуванні ацетилсаліцилової кислоти. Дипіридамол протипоказаний при стенокардії напруги (можливий «синдром обкрадання»).

Мал. 27-4. Механізм антиагрегатної дії дипіридамолу: ЕК – ендотеліальна клітина; А2-Р - аденозиновий А2-рецептор; ФДЕ-фосфодіестераза цАМФ; АЦ – аденілатциклаза; GP IIb/IIIa - глікопротеїни IIb/IIIa
Пентоксифілін (агапурин*, трентал*), як і дипіридамол, інгібує фосфодіестеразу та підвищує рівень цАМФ. В результаті в тромбоцитах знижується рівень цитоплазматичного Ca 2+, що призводить до зменшення їхньої агрегації. Пентоксифілін має й інші властивості: підвищує деформованість еритроцитів, знижує в'язкість крові, виявляє судинорозширювальну дію, покращуючи мікроциркуляцію.
Пентоксифілін застосовують при порушеннях мозкового кровообігу, розладах периферичного кровообігу різного генезу, судинної патології очей (див. розділ «Засоби, що застосовуються при порушенні мозкового кровообігу»). Можливі побічні ефекти: диспептичні явища, запаморочення, почервоніння обличчя, зниження АТ, тахікардія, алергічні реакції, кровотечі. Як і дипіридамол, може провокувати напади при стенокардії напруги.
Засоби, що блокують глікопротеїни IIb/IIIa мембран тромбоцитів
Ця група антиагрегантів, які безпосередньо взаємодіють з глікопротеїнами IIb/IIIa мембран тромбоцитів та порушують їх зв'язування з фібриногеном, з'явилася відносно недавно.
Абциксимаб (реопро*) - перший препарат із цієї групи є «химерними» мишачими/людськими моноклональними антитілами (Fab-фрагмент мишачих антитіл до глікопротеїнів IIb/IIIa, поєднаний з Fc-фрагментом Ig людини). Абциксимаб неконкурентно пригнічує зв'язування фібриногену з глікопротеїнами IIb/IIIa на мембрані тромбоцитів, порушуючи їх агрегацію (див. рис. 27-3). Агрегація тромбоцитів нормалізується через 48 годин після одноразового введення. Препарат вводять внутрішньовенно (у вигляді інфузії) для профілактики тромбозу при ангіопластику коронарних артерій. При застосуванні абциксимабу можливі кровотечі, зокрема внутрішні (шлунково-кишкові, внутрішньочерепні, кровотечі з сечостатевих шляхів), нудота, блювання, гіпотензія, брадикардія, алергічні реакції аж до анафілактичного шоку, тромбоцитопенія.
Пошуки менш алергогенних препаратів з таким самим механізмом дії призвели до створення синтетичних блокаторів глікопротеїнів IIb/IIIa. На основі барборину (пептид, виділений з отрути карликової гримучої змії) був отриманий препарат е п т і ф і ба т і д (інтегрилін *) - циклічний гектапептид, що імітує амінокислотну послідовність ланцюга фібриногену, яка безпосередньо зв'язується з глікопротеїнами IIb/III. Ептифібатід конкурентно витісняє фібриноген із зв'язку з рецепторами, викликаючи оборотне порушення агрегації тромбоцитів. Препарат вводять внутрішньовенно як інфузії; Антиагрегантний ефект настає протягом 5 хв і зникає через 6-12 годин після припинення введення. Препарат рекомендований для запобігання тромбоутворенню при черезшкірній коронарній ангіопластиці, при нестабільній стенокардії, для профілактики інфаркту міокарда. Небезпечне ускладнення при застосуванні ептифібатиду – кровотеча; можлива тромбоцитопенія.
Тирофібан (аграстат*) – непептидний блокатор глікопротеїнів IIb/IIIa, аналог тирозину. Як і ептифібатид, тирофібан блокує глікопротеїнові IIb/IIIa рецептори конкурентно. Вводять препарат внутрішньовенно (інфузійно). Швидкість настання ефекту, тривалість дії та показання до застосування такі ж, як у ептифібатиду. Побічні ефекти – кровотечі, тромбоцитопенія.
Щоб розширити можливості застосування препаратів цієї групи, були створені блокатори глікопротеїнів IIb/IIIa, ефективні при введенні внутрішньо - ксемилофібан*, сибрафібан* та ін. Проте випробування цих препаратів виявили їх недостатню ефективність та побічний ефект у вигляді вираженої тромбоцитопенії.
27.2. ЗАСОБИ, ЩО ВПЛИВАЮТЬ НА ЗВЕРТАННЯ КРОВІ
Ушкодження судинної стінки ініціює не лише агрегацію тромбоцитів, а й згортання крові. Відомо безліч факторів (плазмових, тканинних, тромбоцитарних), що у цьому процесі. Більшість із них – це білки плазми крові, які циркулюють у неактивному стані, але послідовно активуються у процесі згортання крові. Для пояснення дії лікарських препаратів слід згадати фактор VII (проконвертин), фактор IX (Крістмаса), фактор Х (Стюарта – Прауер), фактор II (протромбін). Ці фактори згортання є проферментами і при активації перетворюються на протеолітичні ферменти (чинники ГХа, Ха та На). Фактори VIII і V після активації виконують роль білків-кофакторів ферментів (факторів IXа та Ха відповідно), підвищуючи їхню протеолітичну активність.
Фактор VII спочатку має невисоку протеолітичну активність, але в результаті взаємодії з тканинним фактором (див. стор. 481) вона швидко зростає. Активований фактор VII (фактор VIIa) разом з тканинним фактором і Са 2+ утворює комплекс, що викликає частковий протеоліз факторів IX і Х. Фактор IХа, своєю чергою, додатково активує фактор Х (утворюється фактор Ха). Фактор Ха діє на протромбін (фактор II) і перетворює його на тромбін (фактор На). Тромбін викликає частковий протеоліз фібриногену з утворенням фібрину (рис. 27-5).
Протеолітична активація факторів згортання крові значно прискорюється, якщо вони через іони Са 2+ зв'язуються з негативно зарядженими фосфоліпідами клітинних мембран. Ці фосфоліпіди виконують роль своєрідної матриці, на якій фактори згортання збираються в комплекси за участю іонів Са2+. При цьому швидкість активації факторів у цих комплексах зростає у 10 тисяч разів і більше. Необхідною умовою формування таких комплексів є здатність факторів II, VII, IX та Х зв'язуватися із Са 2+. Ці фактори містять негативно заряджені
залишки γ-карбоксиглутамінових кислот, які забезпечують їх зв'язування з Са 2+ . Утворення γ-карбоксиглутамінових кислот відбувається у печінці за участю вітаміну K. При дефіциті вітаміну K у крові з'являються неповноцінні II, VII, IX та Х фактори зсідання крові, що порушує утворення фібрину.

Мал. 27-5. Схема активації згортання крові при пошкодженні судинної стінки (З: Katzung B. G. Basic and clinical pharmacology. - NY, 2001, з ізм.): Жирною рисою підкреслені комплекси факторів згортання крові, пов'язані з негативно зарядженими фосфоліпідами клітинних мембран. Комплекс VIIa + ТФ + Са 2+ активує фактори Х та IX (ТФ – тканинний фактор). Комплекс IXa + VIIIa + Ca 2+ додатково активує фактор Х. Комплекс Ха + Va + Са 2+ (протромбіназ) сприяє перетворенню протромбіну на тромбін. Фактори, укладені прямокутники, інгібуються гепарином.
До білків плазми крові, які містять залишки γ-карбоксиглутамінових кислот та утворюються в печінці за участю вітаміну K, відносяться також протеїни C та S. Після активації протеїн C (Са) викликає протеолітичне розщеплення факторів VIIIа та Уа. Це призводить до порушення утворення тромбіну. Протеїн S виконує роль кофактора у реакціях протеолізу. Активація протеїну C відбувається під дією тромбіну на поверхні інтактних (неушкоджених) ендотеліальних клітин, які експресують тромбомодулін білок, що зв'язує одночасно протеїн C і тромбін.
27.2.1. Засоби, що знижують згортання крові (антикоагулянти)
Антикоагулянти, що використовуються в клінічній практиці, або пригнічують активні фактори згортання безпосередньо в крові, або порушують їх утворення в печінці. Тому їх поділяють на 2 групи:
(Діють безпосередньо в крові).
- Гепарин стандартний(Нефракціонований).
- Низькомолекулярні гепарини:
еноксапарин натрію;
Надропарин кальцію;
Далтепарин натрію;
Ревіпарин натрію.
- Гепариноїди:
Сулодексид;
Данапароїд ** .
- Препарат антитромбіну ІІІ.
- Препарати гірудину:
Лепірудін *.
- Активований протеїн C:
Дротрекогін альфа.
(пригнічують синтез факторів згортання печінки).
- Похідні кумарину:
Аценокумарол (синкумар *);
Варфарин (варфарекс *).
- Похідні індандіону:
Феніндіон (фенілін *).
Антикоагулянти прямої дії
Гепарин- сульфатований глікозаміноглікан (мукополісахарид), що складається з залишків D-глюкозаміну та D-глюкуронової кислоти. Гепарин утворюється опасистими клітинами у багатьох тканинах; у великій кількості його містять печінку, легені, слизова оболонка кишечника. Для медичних цілей гепарин виділяють із слизової оболонки кишечника свині та з легких великої рогатої худоби. В процесі
виділення отримують суміш фракцій з різною довжиною полісахаридного ланцюга та різною молекулярною масою (від 3000 до 40 000 Д). Фракції з різною молекулярною масою дещо відрізняються за біологічною активністю та фармакокінетичними властивостями. Тому препарати гепарину, одержувані різними способами і з різних джерел, можуть мати неоднакову антикоагулянтну активність, внаслідок чого необхідно проводити їх біологічну стандартизацію. Активність гепарину визначають за здатністю подовжувати час зсідання крові (1 мг стандартного гепарину містить 130 ОД).
Гепарин впливає на фактори зсідання крові тільки після утворення комплексу з ендогенним антикоагулянтом антитромбіном III. Антитромбін III, - глікопротеїн плазми крові, інгібує серинові протеази, до яких належать фактори зсідання крові IIа (тромбін), ЕХа та Ха (а також ХIа та ХIIа). Процес інактивації факторів під дією одного антитромбіну ІІІ протікає дуже повільно. Гепарин викликає конформаційні зміни в молекулі антитромбіну III, що призводить до прискорення цього процесу приблизно 1000 разів.

Основна дія комплексу гепарин-антитромбін III спрямована проти тромбіну та фактора Ха, але механізми пригнічення цих факторів мають деякі відмінності. Для інактивації тромбіну необхідно, щоб гепарин зв'язався як з молекулою антитромбіну III, так і молекулою тромбіну. Водночас швидка інактивація фактора Ха комплексом гепарин – антитромбін III не потребує зв'язування цього фактора з гепарином. Фракції гепарину з відносно коротким полімерним ланцюгом (менше 18 сахаридних одиниць) не можуть одночасно приєднувати антитромбін III і тромбін, тому не мають антитромбінової активності. Їхня дія в основному пов'язана з інактивацією фактора Ха і, отже, з порушенням перетворення протромбіну на тромбін.
Крім впливу на згортання крові гепарин має і деякі інші ефекти: знижує рівень ліпідів у крові внаслідок активації ліпопротеїнліпази (цей фермент гідролізує тригліцериди), пригнічує проліферацію гладких клітин.
Гепарин погано всмоктується при внутрішньовенному введенні, тому його вводять внутрішньовенно, іноді підшкірно. При внутрішньовенному введенні дія настає відразу і триває 2-6 годин. При підшкірному введенні гепарин починає діяти через 1-2 години, тривалість дії становить 8-12 годин (призначають 2-3 рази на добу). Гепарин у крові зв'язується з багатьма білками, у тому числі з тими, що його нейтралізують (тромбоцитарний фактор 4 та деякі інші). Високий рівень цих білків у крові може спричинити відносну резистентність до препарату. Крім того, гепарин зв'язується з макрофагами та ендотеліальними клітинами, при цьому відбувається його деградація (деполімеризація). Гепарин також метаболізується у печінці та виводиться нирками.
Застосовують гепарин для профілактики та лікування тромбозу глибоких вен та тромбоемболії легеневої артерії, при нестабільній стенокардії та інфаркті міокарда, для попередження тромбозу периферичних артерій, при протезуванні клапанів серця та екстракорпоральному кровообігу. Дозують гепарин у одиницях дії (ОД).
Найбільш часті ускладнення гепаринотерапії – кровотечі, причиною яких може бути пригнічення функції тромбоцитів або зменшення їх кількості (тромбоцитопенія). Зв'язування гепарину з фактором Віллебранда, мабуть, пояснює його інгібуючу дію на адгезію та агрегацію тромбоцитів. У таких випадках гепарин скасовують, а при серйозних кровотечах, крім того, внутрішньовенно вводять протаміну сульфат, який нейтралізує гепарин шляхом утворення нерозчинного комплексу.
Тромбоцитопенія виникає на 7-14 день лікування приблизно у 1-5% хворих, які отримують гепарин. Причиною є поява антитіл (IgG), спрямованих проти комплексу гепарин-фактор 4 тромбоцитів. Цей комплекс зв'язується з мембраною тромбоцитів при нейтралізації гепарину фактором 4, глікопротеїном тромбоцитарного походження, що вивільняється при агрегації тромбоцитів. Менш ніж у 1% хворих з тромбоцитопенією спостерігають тромбоз внаслідок ушкодження ендотеліальних
клітин та активації тромбоцитів антитілами до комплексу гепарин-фактор 4. Цей стан вимагає відміни гепарину та призначення антикоагулянтів, які не викликають тромбоцитопенію: данапароїд** та лепірудин**.
При тривалому введенні гепарину (більше 3 місяців) можливий розвиток остеопорозу. Це особливо важливо враховувати для призначення гепарину під час вагітності. Гіперкаліємія, пов'язана з інгібуванням синтезу альдостерону в надниркових залозах, - досить рідкісне ускладнення гепаринотерапії.
Низькомолекулярні (фракціоновані) гепарини складаються із фрагментів гепарину з молекулярною масою від 1000 до 10 000 Д (в середньому, 4000-5000 Д). Отримують їх шляхом фракціонування, гідролізу або деполімеризації звичайного (нефракціонованого) гепарину. Ці препарати, як і гепарин, діють на фактори згортання через антитромбін III, але відрізняються від гепарину наступними властивостями:
Більшою мірою пригнічують активність фактора Ха, ніж фактора IIа (в 3-4 рази);
Мають більшу біодоступність при підшкірному введенні (низькомолекулярні гепарини - близько 90%, стандартний гепарин - 20%);
Діють триваліше, що дозволяє вводити їх 1-2 рази на добу;
Мають меншу спорідненість до 4 фактора тромбоцитів, тому рідше, ніж стандартний гепарин, викликають тромбоцитопенію;
Рідше спричиняють остеопороз.
У вітчизняній практиці використовують наступні препарати низькомолекулярних гепаринів: енокосарійнатрії (клексан *), надропарин кальцію (фраксипарин *), д а л е т а - рин натрію (фрагмін *), ревіпарин натрію (кліварін*). Ці препарати неоднорідні за своїм складом (містять різні фракції гепарину), тому дещо відрізняються один від одного за фізико-хімічними, фармакокінетичними властивостями та активністю.
Низькомолекулярні гепарини застосовують для профілактики та лікування тромбозу глибоких вен (особливо після хірургічного втручання), для запобігання тромбоемболії легеневої артерії, а також при нестабільній стенокардії та інфаркті міокарда. Препарати низькомолекулярних гепаринів показані для профілактики
тики та терапії тромбозів в акушерській практиці. Вводять лише підшкірно. Дозують у ME (міжнародних одиницях).
Низькомолекулярні гепарини, як і препарати нефракціонованого гепарину, можуть спричинити кровотечі. У перші дні лікування можлива помірна тромбоцитопенія. Низькомолекулярні гепарини часом підвищують активність печінкових ферментів, можуть викликати алергічні реакції. Протаміну сульфат усуває ефекти низькомолекулярних гепаринів не повністю.
Нещодавно в клінічній практиці з'явився препарат фондапа - ринукс натрію-синтетичний пентасахарид, який, зв'язуючись з антитромбіном III, прискорює інактивацію фактора Ха. Препарат випускають у вигляді натрієвої солі, застосовують для профілактики венозних тромбозів та тромбоемболії легеневої артерії в ортопедичній хірургії.
Гепариноїди- сульфатовані глікозаміноглікани, споріднені за структурою гепарину. Як і гепарин, посилюють інгібуючу дію антитромбіну III на фактори зсідання крові. За багатьма важливими характеристиками відмінні від гепарину та низькомолекулярних гепаринів, тому їх виділяють у особливу групу. До цієї групи належать данапароїд і сулодексид. Отримують ці препарати із слизової оболонки кишечника свині.
Данапароїд** (органон**) містить суміш гепарансульфату, дерматансульфату і хондроїтинсульфату. Данапароїд p більш виражено інгібує фактор Ха, ніж протромбін. Препарат вводять під шкіру при профілактиці та лікуванні венозних тромбозів. Данапароїд p не зв'язується з фактором 4 тромбоцитів і не викликає тромбоцитопенію. Тому він показаний у тих випадках, коли терапія гепарином ускладнюється тромбоцитопенією.
Сулодексид (вессел Дуе Ф*) складається із суміші гепарансульфату та дерматансульфату. Сулодексид більшою мірою знижує активність фактора Ха, мало впливаючи на протромбін. Препарат підвищує фібринолітичну активність, надає захисну дію на ендотелій судин, має гіполіпідемічні властивості. Сулодексид показаний при захворюваннях периферичних судин із підвищеним ризиком тромбоутворення. Існують лікарські форми препарату для парентерального (внутрішньовенного та внутрішньом'язового) введення та для прийому внутрішньо.
Антитромбін IIIнеобхідний для прояву антикоагулянтної дії гепарину, низькомолекулярних гепаринів, а також гепариноїдів.
При спадковій недостатності антитромбіну III використовують його препарат, що вводять внутрішньовенно. При тривалому застосуванні гепарину збільшується споживання антитромбіну III, тому концентрація його у крові помітно знижується. Це зменшує ефективність проведеної гепаринотерапії. У таких випадках також вводять антітромбін III.
Гірудін- Білок з молекулярною масою 7 кД, вперше виявлений у слинних залозах медичних п'явок Hirudo medicinalis.Гірудин, як і гепарин, відноситься до антикоагулянтів, що діють безпосередньо в крові, але на відміну від гепарину, гірудин прямо інгібує тромбін: селективно зв'язується з ним та інактивує його без участі антитромбіну III. Інгібування має незворотний характер. На відміну від гепарину, гірудин має здатність інгібувати тромбін, пов'язаний з тромбом, і таким чином затримує зростання тромбу. Гірудин не взаємодіє з фактором 4 тромбоцитів, тому не викликає тромбоцитопенію.
Для клінічного застосування отримано рекомбінантний препарат гірудину - лепіндин* (рефлюдан*). Його рекомендують використовувати для профілактики можливих тромбоемболічних ускладнень при тромбоцитопенії, спричиненій гепарином. Вводять лепірудин внутрішньовенно. При використанні можливі кровотечі. Специфічного антидоту препарати гірудину не мають.
Дротрекогін альфа (зігріс*) – рекомбінантний препарат активованого протеїну С. Інгібує утворення тромбіну, викликаючи протеолітичну інактивацію факторів згортання крові VIIIа та Vа. Крім того, дротрекогін підвищує фібринолітичну активність плазми крові, знижуючи кількість інгібітору активатора плазміногену типу 1, що циркулює в крові. Всі ці властивості дротрекогіну визначають його ефективність при лікуванні септичного шоку (запалення та підвищення згортання крові – основні симптоми цього стану). Як і інші антикоагулянти, препарат може спричинити геморагічні ускладнення.
Антикоагулянти непрямої дії
Ці препарати, на відміну гепарину, не впливають на чинники згортання у крові. Вони інгібують син-
тез у печінці білків плазми крові, залежних від вітаміну K – фактора II (протромбін), факторів VII, IX та Х (див. рис. 27-5). Вітамін K необхідний для утворення функціонально повноцінних факторів, оскільки виконує роль коферменту реакції γ-карбоксилювання залишків глутамінових кислот. Коферментну активність виявляє відновлена форма вітаміну K – гідрохінон. У процесі карбоксилювання вітамін K-гідрохінон окислюється з утворенням неактивного вітаміну K-епоксиду. Антикоагулянти непрямої дії перешкоджають перетворенню (відновленню) неактивного вітаміну K-епоксиду на активний вітамін K-гідрохінон під дією епоксидредуктази та DT-діафорази, інгібуючи ці ферменти. Тому їх відносять до антагоністів вітаміну K (рис. 27-6).

Мал. 27-6.Механізм дії вітаміну К та антикоагулянтів непрямої дії
Антикоагулянти непрямої дії знижують концентрацію факторів згортання крові не відразу. Їхня дія характеризується латентним періодом. Так, антикоагулянтний ефект аценокумаролу досягає максимальної величини через 48 годин і більше. Такий повільний розвиток ефекту пояснюють тим, що при введенні цих препаратів у крові ще якийсь час циркулюють повноцінні фактори зсідання (швидкість настання ефекту визначається часом, протягом якого відбувається деградація факторів згортання протромбінового комплексу). Ефект антикоагулянтів непрямої дії зберігається близько 2-4 днів, препарати здатні до кумуляції.

Антикоагулянти непрямої дії застосовують для тривалої профілактики та лікування тромбозів та тромбоемболій (тромбозів глибоких вен, тромбоемболії легеневої артерії, тромбоемболічних ускладнень при миготливій аритмії передсердь, інфаркті міокарда; вання у післяопераційному періоді. Вводять усередину. Лікування проводять під обов'язковим контролем рівня протромбіну в плазмі шляхом визначення протромбінового часу - показника, величина якого залежить від вмісту в крові протромбіну і факторів IX і X.
Найчастішими ускладненнями при застосуванні антикоагулянтів непрямої дії є кровотечі. Ризик виникнення кровотеч посилюється при одночасному застосуванні аспірину та інших антиагрегантів. Для зупинки кровотеч, викликаних антикоагулянтами непрямої дії, слід вводити препарати вітаміну K 1 концентрат протромбінового комплексу (містить фактори II, VII, IX і X). Можливі інші побічні ефекти: алергічні реакції, діарея, дисфункція печінки, некроз шкіри. Препарати антикоагулянтів непрямої дії протипоказані при вагітності: вони проникають через плаценту і можуть чинити тератогенну дію (порушують формування скелета, оскільки
пригнічують утворення остеокальцину – вітамін K-залежного білка кісткової тканини). Феніндіон (фенілін*) може спричинити пригнічення кровотворення.
27.2.2. Засоби, що підвищують згортання крові
Засоби, що підвищують згортання крові, застосовують для зупинки кровотеч, тому їх відносять до гемостатичних засобів (гемостатиків) або антигеморагічним засобам. Ця група включає речовини, необхідні для утворення факторів згортання крові (препарати вітаміну K), та препарати самих факторів згортання.
Препарати вітаміну K
Вітамін K існує у вигляді двох форм - вітаміну K 1 (філлохінон), виявленого в рослинах, і вітаміну K 2 - групи сполук (менахінони), що синтезуються мікроорганізмами (зокрема, мікрофлорою кишечника людини). Вітаміни K 1 і K 2 - жиророзчинні сполуки, похідні 2-метил-1,4-нафтохінону, що відрізняються за довжиною та характером бічного вуглецевого ланцюга. Вітамін K j отриманий синтетичним способом, його препарат відомий під назвою ф і т о м е н а д і о н. Синтезований водорозчинний попередник вітаміну K - 2-метил-1,4-нафтохінон (менадіон), що має провітамінну активність. Ця сполука була названа вітаміном K 3 . Похідне вітаміну K 3 - менадіону натрію бісульфіт - використовують у медичній практиці під назвою в іка-сол *.
Вітамін K необхідний для синтезу в печінці протромбіну (фактору II) та факторів згортання крові VII, IX та Х, а також білків С та S. Відома участь вітаміну K у синтезі білка кісткової тканини остеокальцину.
Структура всіх вітамін-K-залежних білків має загальну особливість: ці білки містять залишки γ-карбоксиглутамінових кислот, що зв'язують іони Са2+. Вітамін K-гідрохінон виконує функцію коферменту в реакції γ-карбоксилювання залишків глутамінових кислот (див. рис. 27-6). При недостатності вітаміну K з'являються неактивні попередники факторів зсідання крові, нездатні пов'язувати Са 2+ . Дефіцит вітаміну K в організмі найшвидше призводить до порушення гемокоагуляції. Тому основними
та найбільш ранніми проявами K-вітамінної недостатності є кровотечі та крововиливи.
Препарати вітаміну K використовують для запобігання та зупинки кровотеч та інших геморагічних ускладнень, спричинених недостатністю вітаміну K в організмі, наприклад, при геморагічному синдромі новонароджених. К-авітаміноз у новонароджених може бути викликаний як недостатнім надходженням вітаміну K 1 , так і відсутністю мікрофлори кишечника, що синтезує вітамін K 2 . Для запобігання таким ускладненням рекомендують профілактичне введення вітаміну K 1 новонародженим у перші години життя.
Препарати вітаміну К показані при зниженні всмоктування вітаміну K у кишечнику у зв'язку з порушенням виділення жовчі при обтураційній жовтяниці (жовч необхідна для всмоктування жиророзчинного вітаміну K) або з синдромом мальабсорбції (при спру, ентероколітах, хворобі Крона та ін.).
Препарати вітаміну K 1 ефективні при кровотечах, спричинених антикоагулянтами непрямої дії. Вводять їх усередину і внутрішньовенно повільно.
Препарати вітаміну K можуть викликати алергічні реакції (висипання, свербіж, еритема, бронхоспазм). При внутрішньовенному введенні виникає ризик анафілактоїдних реакцій. При застосуванні препаратів вітаміну K 3 (вікасол*) у новонароджених існує небезпека розвитку гемолітичної анемії та гіпербілірубінемії.
Препарати факторів згортання крові
Необхідність у таких препаратах виникає за недостатності одного або декількох факторів згортання крові.
Антигемофільний фактор зсідання крові VIII (гемофіл М*, імунат* та ін.) являє собою сухий концентрат фактора VIII. Препарати одержують із плазми крові донорів, що зазнала подвійної вірусінактивації, стандартизують за змістом фактора VIII. Вони активніші і безпечніші, ніж кріопреципітат * .
Кріопреципітат* - концентрат білків плазми крові, до складу якого входять фактор VIII, фактор Віллебранда, фібронектин, а також меншою мірою інші фактори зсідання крові та невеликі кількості фібриногену.
Препарати вводять внутрішньовенно при спадковій (гемофілія A) та набутій недостатності фактора VIII. Кріопреципітат * ,
крім того, використовують для замісної терапії при хворобі Віллебранда (спадкова недостатність фактора фон Віллебранда) та афібриногенемії. При введенні можливі побічні реакції у вигляді тахікардії, гіпотензії, задишки, алергічні реакції (кропив'янка, підвищення температури тіла, анафілактичний шок), а також гемоліз еритроцитів.
Усі препарати факторів згортання, що отримуються з плазми крові, мають суттєву нестачу - можливість передачі вірусних інфекцій (ВІЛ, гепатиту). В даний час отримані рекомбінантні препарати фактора VIII та фактора Віллебранда, застосування яких знижує ризик інфікування.
Окрім препаратів факторів згортання, при легкій формі гемофілії A та хвороби Віллебранда застосовують аналог аргінінвазопресину десмопресин. Десмопресин підвищує вміст фактора Віллебранда в плазмі крові, сприяючи його виділенню з ендотеліальних клітин та збільшує активність фактора
VIII. Препарат вводять парентерально.
Фактор згортання крові IX (агемфіл B*, імунін*, октанайн*) – очищена фракція людської плазми, збагачена фактором IX. Застосовують при вродженому (гемофілія B) та набутому дефіциті фактора IX, а також при передозуванні антикоагулянтів непрямої дії. Побічні ефекти такі самі, як і препаратів фактора VIII.
Ептаког альфа активований (новосевен *) – рекомбінантний фактор згортання крові VIIa. Застосовують при недостатності фактора VII та інших факторів згортання (V, II,
IX, X).
Місцево для зупинки кровотеч із дрібних капілярів і паренхіматозних органів використовують препарат тромбіна (отримують з плазми крові донорів), а також гемостатичні губки (колагенову, желатинову).
Для зупинки маткових, легеневих, ниркових, кишкових та інших кровотеч використовують препарати лікарських рослин: листя кропиви, траву деревію, траву горця перцевого, траву горця ниркового, кору калини, квітки арніки, лагохілус п'янкий. Застосовують лікарські рослини у вигляді настоїв, настоянок та екстрактів внутрішньо та місцево.
27.3. ЗАСОБИ, ЩО ВПЛИВАЮТЬ НА ФІБРИНОЛІЗ
При утворенні тромбів відбувається активація фібринолітичної системи, яка забезпечує розчинення (лізис) фібрину та руйнування тромбу. Це призводить до відновлення нормального кровотоку.
У процесі фібринолізу неактивний плазміноген перетворюється на плазмін (фібринолізин) за участю активаторів плазміногену. Плазмін гідролізує фібрин із утворенням розчинних пептидів. Плазмін не має специфічності та викликає також руйнування фібриногену та деяких інших факторів згортання крові, що підвищує ризик розвитку кровотеч. Плазмін, що циркулює в крові, швидко інактивується α 2 -антиплазміном та іншими інгібіторами, тому в нормі не має системної фібриногенолітичної дії. Однак за певних патологічних станів або застосування фібринолітичних засобів можлива надмірна активація плазміногену плазми крові, що може стати причиною кровотеч.
27.3.1. Фібринолітичні (тромболітичні) засоби
Фібринолітичні засоби застосовують для розчинення тромбів, що утворилися при коронарному тромбозі (гострому інфаркті міокарда), тромбозі глибоких вен, гострому тромбозі периферичних артерій, тромбоемболії легеневої артерії.
Як фібринолітичні засоби застосовують препарати, які активують плазміноген: препарати стрептокінази, препарат тканинного активатора плазміногену, препарати урокінази.
Препарати стрептокінази
Стрептокіназа (кабікіназа *) - високоочищений білковий препарат, що отримується з культури β-гемолітичного стрептокока. Стрептокіназа набуває протеолітичної активності тільки в комплексі з плазміногеном. При введенні стрептокінази утворюється еквімолярний комплекс стрептокіназа-плазміноген, що перетворює плазміноген на плазмін. Стрептокіназа діє на плазміноген як у тромбі, так і у плазмі крові (рис. 27-7).
Стрептокіназу вводять внутрішньовенно крапельно при гострому інфаркті міокарда, спричиненому тромбозом коронарних судин (найбільше
ефективна перші 3-6 год), при тромбозі глибоких вен, тромбоемболії легеневої артерії, тромбоз судин сітківки. Дозують стрептокіназу в ME (міжнародних одиницях).
Часті ускладнення при застосуванні стрептокінази - кровотечі, які можуть бути пов'язані як з активацією плазміногену, що циркулює в крові (плазмін, що утворюється, руйнує фібриноген, внаслідок чого знижується агрегація тромбоцитів), так і з розчиненням фізіологічних тромбів. Можливі нудота, блювання, артеріальна гіпотензія. Внаслідок наявності антигенних властивостей стрептокіназу може спричинити алергічні реакції, включаючи анафілактичний шок. Небезпека зростає при повторному введенні препарату. Антитіла, що циркулюють у крові, можуть інактивувати стрептокіназу та знижувати ефективність терапії.
Аністреплаза** (еміназа**) – комплекс стрептокінази з ацильованим лізин-плазміногеном. Ацильна група у молекулі плазміногену закриває каталітичний центр, що перешкоджає активації плазміногену. Препарат є проліками і здатність перетворювати плазміноген на плазмін набуває тільки після відщеплення ацильної групи. Швидкість деацилювання і, отже, час утворення активного препарату залежить від характеру ацильної групи і може становити від 40 хвилин до кількох годин. Аністреплазу** вводять внутрішньовенно. Після одноразового введення фібринолітичний ефект зберігається 4-6 годин. Показання до застосування та побічні ефекти такі ж, як у стрептокінази.
Препарати тканинного активатора плазміногену та урокінази
Тканинний активатор плазміногену та урокіназу – основні фізіологічні активатори плазміногену.
Тканинний активатор плазміногену продукується ендотеліальними клітинами. Він викликає частковий протеоліз плазміногену, внаслідок чого той перетворюється на плазмін. Відмінна риса тканинного активатора - висока спорідненість до фібрину, який у сотні разів прискорює його дію на плазміноген. В результаті тканинний активатор з більшою швидкістю активує молекули плазміногену, які адсорбовані на нитках фібрину. Таким чином, дія тканинного активатора плазміногену обмежується фібрином тромбу. Потрапляючи в кровотік,

Мал. 27-7.Механізм дії фібринолітичних засобів: ТАП – тканинний активатор плазміногену; ПДФ – продукти деградації фібриногену; ЕК – ендотеліальна клітина; ? - Активація; Θ - лізис
тканинний активатор зв'язується зі специфічним інгібітором, тому мало діє на плазму, що циркулює в крові, і в меншій мірі знижує рівень фібриногену.
Для клінічного використання отримані рекомбінантні препарати тканинного активатора плазміногену: а л е п л а з а (актиліз *) і тен е т е п л а з (металіз *). Препарати вводять внутрішньовенно при гострому інфаркті міокарда, спричиненому тромбозом коронарних судин (ефективні у перші 6-12 годин), при тромбоемболії легеневої артерії. Незважаючи на те, що алтеплаза мало діє на плазму, що циркулює в крові, при її застосуванні часто виникають геморагічні ускладнення. Антигенних властивостей немає. Тенектеплаза має підвищену специфічність по відношенню до фібрину тромбу.
Урокіназа утворюється клітинами нирок, виявлена у сечі. У нирках утворюється одноланцюжкова урокіназа (проурокіназа), яка під дією плазміну перетворюється на активну форму - дволанцюжкову урокіназу. Дволанцюжкова урокіназа має пряму активуючу дію на плазміноген (утворення комплексу з плазміногеном не потрібно). Препарат дволанцюжкової урокінази одержують із культури ембріональних клітин нирок людини. Застосовують при гострому інфаркті міокарда, венозному та артеріальному тромбозі, тромбоемболії легеневої артерії. Вводять внутрішньовенно. Дозують у ME. Порівняно з тканинним активатором плазміногену урокіназа більшою мірою діє на плазму, що циркулює в крові, в результаті утворюється в крові плазмін викликає розпад фібриногену (див. рис. 27-7). При цьому знижується агрегація тромбоцитів і утворюються продукти деградації фібриногену, які мають антикоагулянтну активність. Основні побічні ефекти – кровотечі. Антигенними властивостями не має.
Отриманий рекомбінантний препарат одноланцюгової урокінази (проурокінази) - с а р у п л а з а *, що виявляє велику, ніж урокіназа, специфічність по відношенню до фібрину тромбу.
27.3.2. Антифібринолітичні засоби
Антифібринолітичні засоби застосовують для зупинки кровотеч, спричинених підвищеною активністю фібринолітичної системи, при травмах, хірургічних втручаннях, пологах,
захворюваннях печінки, простатитах, менорагії, а також при передозуванні фібринолітичних засобів. Для цих цілей використовують препарати, які пригнічують активацію плазміногену, або є інгібіторами плазміну.
Амінокапронова кислота зв'язується з плазміногеном і перешкоджає його перетворенню на плазмін. Крім того, вона перешкоджає дії плазміну на фібрин. Препарат вводять внутрішньо та внутрішньовенно. Можливі побічні ефекти: гіпотензія, брадикардія, аритмії, запаморочення, нудота, діарея. Подібною дією має амінометилбензойна кислота (амбен*, памба*).
Транексамова кислота (транексам*, циклокапрон*) пригнічує активацію плазміногену. Препарат вводять внутрішньо та внутрішньо. По ефективності перевершує амінокапронову кислоту, діє триваліше. З побічних ефектів викликає диспептичні явища (анорексію, нудоту, блювання, діарею), запаморочення, сонливість; можливі шкірні алергічні реакції.
Апротинін (гордокс*, контрикал*, трасилол*, інгітрил*) інгібує плазмін та інші протеолітичні ферменти. Препарат вводять внутрішньовенно. Побічні ефекти: гіпотензія, тахікардія, нудота, блювання, алергічні реакції.
Тромбоцити, найдрібніші кров'яні тільця (порівняно з лейкоцитами та еритроцитами), виконують найважливішу функцію – захищають організм від втрати крові. Агрегація тромбоцитів – це процес склеювання клітин між собою, початкова стадія утворення тромбу.
Другим етапом є закріплення тромбоцитів на стінці пошкодженої судини. На тромбоцитарну масу нашаровуються нитки фібрину, інші елементи, нові клітини, що злиплися. Таким чином, тромб розростається до розмірів, здатних перекрити діаметр судини і припинити кровотечу. Від швидкості процесу часом залежить життя.
Роль агрегації тромбоцитів у процесі згортання крові
Згортання крові залежить від безлічі факторів. Один із них, агрегація тромбоцитів, у здоровому організмі носить захисний пристосувальний характер. Клітини склеюються тільки в судині, що кровоточить. У разі процес грає позитивну роль.
Але відомі патологічні стани, у яких утворення тромбів небажано, оскільки веде до порушення харчування життєво важливих органів. Наприклад, при інфаркті міокарда, інсульті, тромбозі провідних артерій. Агрегаційна активність тромбоцитів сприймає бік патологічних змін. Проти неї доводиться боротися за допомогою різноманітних ліків.
Існує практична необхідність у визначенні кількісного вираження хорошої та поганої агрегації тромбоцитів. Для цього потрібно скористатися нормою та розрізняти відхилення.
Як визначити норму та патологію?
Чи може аналіз крові показати агрегаційну спроможність тромбоцитів конкретної людини? Адже для проведення дослідження береться кров із вени, і з цього моменту на клітини крові не діють накази організму. Такий вид аналізів називають "інвітро", дослівний переклад з латини "на склі, в пробірці". Вчені завжди намагаються вивчати реакцію в умовах, наближених до людського тіла. Тільки отримані таким шляхом дані можна вважати достовірними та користуватися ними у діагностиці.
Здібності тромбоцитів визначають за індукованою агрегацією. Це означає, що як речовина-індуктор використовуються засоби, не чужі організму за хімічним складом, здатні викликати тромбоутворення. Як індуктори застосовуються складові судинної стінки: аденозиндифосфат (АДФ), ристоцетин (ристоміцин), колаген, серотонін, арахідонову кислоту, адреналін.
Спонтанна агрегація визначається без індукторів.
Методики кількісного визначення ґрунтуються на пропущенні світлових хвиль через збагачену тромбоцитами плазму крові. Ступінь активності агрегації вивчають по різниці у світловій щільності плазми до початку згортання та після отримання максимального результату. Також визначають швидкість агрегації в першу хвилину, характер та форму хвиль.
Норма залежить від речовини-індуктора, його концентрації.
Агрегація тромбоцитів з АДФ зазвичай призначається та оцінюється у комплексі з колагеном, з ристоміцином та з адреналіном.
Норма аналізу з АДФ від 30,7 до 77,7%. Розмір агрегації тромбоцитів з адреналіном змінюється від 35 до 92,5%. При дослідженні з колагеном нормальними показниками вважаються від 464 до 931%.
Правила підготовки до взяття аналізу
Щоб здати аналіз крові на агрегаційну здатність, треба розуміти, що дослідження буде неточним у разі порушення правил підготовки. У крові будуть присутні речовини, що впливають на результат.
- За тиждень до здачі крові повинні бути скасовані всі лікарські препарати аспіринового ряду, діпіридамол, індометацин, сульфапіридазин, антидепресанти. Застосування цих препаратів пригнічує (пригнічує) тромбоутворення. Якщо не можна припинити прийом, слід проінформувати лаборанта.
- Мінімум 12 годин не можна їсти, особливо впливає на результати з'їдена жирна їжа.
- Пацієнт має бути максимально спокійним, не виконувати фізичної роботи.
- За добу виключити з їжі каву, алкоголь, часник, не палити.
- Аналіз не проводиться, якщо є активний запальний процес.
Під мікроскопом видно тромбоцити, що злиплися.
Аналіз крові на агрегацію тромбоцитів призначає лікар за необхідності лікування протизгортаючими препаратами, контролю за їх ефективністю, підборі оптимального дозування, для діагностики підвищеної кровоточивості.
Розшифровка результатів
Причини проведення досліджень одразу з трьома стандартними індукторами, а при необхідності додавання нових, полягають у переважному механізмі активації одного з факторів згортання. Діагностичне значення має виявлена змінена норма, наприклад, з АДФ за відсутності динаміки коїться з іншими індукторами. Оцінка результатів проводиться лікарем.
Зниження агрегації тромбоцитів може бути спричинене:
- успішним застосуванням антиагрегантної терапії;
- групою захворювань, які називають тромбоцитопатиями.

Апарат для проведення аналізу на агрегацію
Роль тромбоцитопатії
Тромбоцитопатії можуть бути спадковими або набутими внаслідок інших захворювань. Статистика каже, що на цю патологію страждає до 10% населення планети. Усі вони пов'язані з порушенням функцій тромбоцитів щодо накопичення певних речовин.
В результаті не відбувається згортання та утворення тромбів, що веде до посилених кровотеч при невеликих ранах, забитих місцях (внутрішня кровотеча).
Захворювання виявляються вже у дитячому віці з кровоточивості ясен, частих носових кровотеч, безлічі синців на тілі дитини, пухлини суглобів при забитих місцях. У дівчаток у період статевого дорослішання починаються тривалі та рясні менструації. Кровотечі призводять до розвитку недокрів'я (анемії).
Низька агрегаційна здатність при тромбоцитопатії може активізуватись вірусною та бактеріальною інфекцією, лікарськими препаратами, фізіотерапевтичними процедурами.

Носові кровотечі у 80% випадків спричинені тромбоцитопатією та лише 20% хворобами ЛОР-органів.
Вторинні тромбоцитопатії
Симптоматичні (вторинні) тромбоцитопатії формуються при хронічному лейкозі, мієломній хворобі. Такий стан характерний для кінцевої стадії ниркової недостатності (уремії), зниження функції щитовидної залози.
З тромбоцитопатиями зустрічаються хірурги при підвищеній кровоточивості під час оперативних втручань.
Підвищення агрегації тромбоцитів спостерігається при:
- поширеному атеросклерозі судин;
- гіпертонічної хвороби;
- інфаркт внутрішніх органів;
- тромбозі артерій черевної порожнини;
- інсульт;
- цукровий діабет.
Зміна агрегації під час вагітності
Агрегація тромбоцитів під час вагітності може відхилятися від нормальних показників.
Знижено агрегацію за рахунок недостатньої продукції тромбоцитів або порушення їх якісного складу. Це проявляється кровоточивістю, наявністю синців. Під час пологів потрібно враховувати можливість масивної кровотечі.
Агрегація підвищена найчастіше під час токсикозу у зв'язку із втратою рідини через блювання та проноси. Зростання концентрації крові призводить до підвищеного тромбоутворення. Це може призвести до викидня на ранніх термінах. Помірна гіперагрегація вважається нормальною при вагітності, вона пов'язана з розвитком плацентарного кровообігу.
- при невиношуванні вагітності;
- лікуванні безплідності;
- перед та під час прийому контрацептивних засобів;
- перед плановою вагітністю
Аналіз агрегаційних властивостей тромбоцитів дає змогу виявити ризик, прогнозувати небезпечні ускладнення протягом захворювань, своєчасно провести профілактичну терапію.
Тромбоцити – це кров'яні тільця, які не мають кольору. Вони виконують важливу функцію в організмі, захищаючи його від крововтрат. Цей процес – агрегація тромбоцитів у крові, він має свої нормативні показники.
Щоб розуміти, що це таке, необхідно мати уявлення про утворення тромбу, існуючі норми, небезпеку відхилень від нормальних значень.
Опис та роль у людському організмі
Після поранення тканин тромбоцити закріплюються на стінках судини, що зазнала пошкодження. Через війну відбувається склеювання клітин друг з одним. До маси, що утворилася, з часом приєднуються фібринові нитки, нові склеєні клітини та інші елементи.
На тлі цього відбувається розростання тромбу, який досягає великих розмірів, що може призвести до перекриття судини та зупинки кровотечі. Швидкість такого процесу є дуже важливою, оскільки саме від неї іноді залежить збереження людського життя.

На згортання крові впливає велика кількість факторів. Одним із них вважається агрегація. За відсутності патологічних станів вона виконує захисну пристосувальну функцію.
Агрегаційні особливості полягають у склеюванні клітин лише у пошкодженій судині. І тут процес вважається позитивним.
.jpg)
Проте є такі ситуації, коли тромбози небажані. Наприклад, якщо діагностовано інсульт, інфаркт міокарда.
Це тим, що формування тромбів перешкоджає нормальному надходженню необхідних речовин до життєво важливих органів.
У цьому випадку тромбоцити постають на бік патологічних процесів.. Боротися із відхиленнями від норми доводиться лише за допомогою лікарських препаратів.
Щоб ідентифікувати нормальні показники відхилень, необхідно проводити кількісний аналіз позитивної та негативної агрегації.
Види
У медичній практиці існує певна класифікація агрегації за видами. До них відносяться:

- Помірна агрегація. Діагностується переважно під час виношування дитини. Спровокувати стан може плацентарний кровообіг.
- Спонтанна агрегація. Для визначення не потрібний індуктор. Щоб виявити агрегаційну активність, кров переливають у пробірку, яка міститься у спеціальний прилад, де відбувається її нагрівання до 37 градусів.
- Індукована агрегація. Для проведення дослідження плазму додають індуктори. У цьому випадку здійснюється агрегація з АДФ, з колагеном, ристоміцином та адреналіном. Даний метод використовується у випадках, коли необхідно діагностувати деякі патології кров'яної рідини.
- Підвищена агрегація сприяє утворенню тромбів. Характерна симптоматика такого патологічного стану - оніміння та набряклість.
- Знижена агрегація найчастіше виявляється при порушеннях у роботі кровоносної системи. Зниження показників тромбоцитів провокує різні кровотечі. Зустрічається у представниць прекрасної статі під час менструального циклу.
Для здоров'я людини є небезпечним як підвищення, так і зниження агрегації. Тому рівень тромбоцитів у крові регулярно має контролюватись.
Симптоми відхилень від показників
Гіперагрегація супроводжується підвищеною в'язкістю крові та зменшенням швидкості її перебігу, що несприятливо впливає на всі системи та органи людини.
Однак існують патологічні стани, коли виражена агрегація є нормальним явищем, що у свою чергу не вважається приводом для відмови від постійного дослідження показників згортання.
До таких захворювань відносяться:
- підвищення артеріального тиску;
- цукровий діабет;
- онкозахворювання;
- судинні патології.
Несвоєчасне виявлення гіперагрегації та відсутність заходів допомоги можуть призвести до розвитку інфаркту, інсульту та тромбозів вен.
Зниження агрегаційних показників супроводжується тривалими кровотечами, зокрема внутрішніми, що проявляється формуванням гематом.
Що є нормою
Норми тромбоцитарного рівня у дорослого та дитини будуть дещо відрізнятися. Оптимальні значення показників представлені у таблиці нижче.
Якщо йдеться про нормальні значення агрегації, то це буде 25-75 відсотків. В даному випадку тромбоцити склеюються без відхилень і не становлять загрози для людського організму.
Яке проводиться дослідження
Аналізатором агрегації тромбоцитів є загальний аналіз крові. Однак існують інші дослідження, які дають більш точні результати. Серед основних методів виділяють такі тести:
.jpg)
- за Лі-Уайтом;
- коагулограму.
Суть їх у тому, що у кров втручають спеціальні речовини, які пригнічують агрегацію.
Дані компоненти схожі на речовини, що містяться в організмі людини, що провокує тромбоутворення. Такі компоненти називають індукторами.
Підготовка до аналізу
Перш ніж робити аналіз, потрібно пройти певну підготовку. Щоб результати були максимально точними, у кров'яній рідині не повинно бути речовин, які можуть негативно вплинути на неї.
Підготовчі заходи:
- За тиждень до аналізу виключаються лікарські препарати ряду аспіринових, оскільки в результаті їхнього прийому відбувається пригнічення тромбоутворення. Якщо скасувати ці кошти неможливо, лаборант, який проводить дослідження, повинен бути повідомлений.
- На термін о 12 годині потрібно відмовитися від вживання їжі. Продукти, особливо підвищеної жирності, також негативно впливають на результати.
- Не допускати фізичних та емоційних навантажень.
- За день не вживати спиртних напоїв, кави, часнику, не курити.
Аналіз відкладається у разі, якщо є активний запальний процес.
Проведення
Забір крові здійснюється вранці, у період із 7 до 10 годин. Дослідження може проводитись лише на голодний шлунок. Дозволяється пити негазовану воду.
Щоб провести гемотест, беруть кров'яну рідину із вени. Для цього застосовується одноразовий шприц. Після цього матеріал поміщають у агрегометр, у якому міститься 4-відсотковий розчин цитрату натрію. Потім ємність кілька разів перевертають. Після пробірку з кров'ю направляють до лабораторії для подальшого дослідження.
Розшифровка результатів
З урахуванням речовини, яка використовувалась під час проведення дослідження, відбувається розшифрування аналізу. Для цього отримані показники порівнюють із нормальними значеннями, які представлені нижче.
Якщо спостерігається збільшення норми, діагностується гіперагрегація. Вона може виникати при таких патологічних станах, як:
.jpg)
- лейкоз;
- патології шлунково-кишкового тракту чи нирок;
- атеросклероз;
- діабет;
- високий артеріальний тиск;
- сепсис;
- лімфогранулематоз.
При відхиленнях у менший бік діагностують гіпоагрегацію. Причинами її може бути патології крові, лікування антиагрегантами.
Відсоткове співвідношення показує рівень світлопропускної здатності плазми після того, як до неї буде додано речовину-індуктор. При низькому вмісті тромбоцитів цей показник дорівнює 100 відсоткам, при підвищеному - нулю.
Особливості агрегації у вагітних жінок
При вагітності допускаються відхилення від норми, які у період становлять від 30 до 60 відсотків.
Дезагрегація може спостерігатися при нестачі тромбоцитів, а також якщо відбувається зміна їх якісного складу, що проявляється кровоточивістю та синцями.
Підвищення агрегації відбувається при токсикозі, коли у пацієнтки відзначається велика втрата рідини внаслідок блювоти чи проносу. Збільшення концентрації крові провокує підвищену освіту тромбів. Це загрожує викиднем на ранньому терміні.
Як можна нормалізувати значення
Якщо діагностується порушення згортання кров'яної рідини, необхідно негайно вжити заходів щодо усунення патологічного стану. Підвищення агрегації може призвести до тромбозу, а зниження – до рясних та небезпечних кровотеч.
На початкових етапах розвитку гіперагрегації фахівці призначають прийом медикаментозних засобів, здатних розріджувати кров. Впоратися з поставленим завданням може звичайний аспірин.
З результатів додаткового обстеження нерідко прописують:
.jpg)
- аналгетики;
- новокаїнову блокаду;
- препарати, що сприяють розширенню судин;
- антикоагулянти, які запобігають швидкому згортанню.
Іноді щонайменше ефективними виявляються народні методи. Варто пам'ятати, що таке лікування в обов'язковому порядку узгоджується з лікарем.
Серед перевірених рецептів виділяють такі:
- Одну столову ложку буркуну залити 200 мл кип'яченої води та дати настоятися протягом 30 хвилин. Приготовлений склад вживати протягом дня кілька прийомів. Курс терапії становить один місяць.
- У рівних кількостях (по чайній ложці) імбиру та зеленого чаю заварити півтора літрами окропу. Додати щіпку кориці. Настояти протягом чверті години та приймати протягом доби.
- Щодня пити свіжий сік апельсина. Можна змішувати в рівних частках із гарбузовим.
Важливо також дотримуватись правильного харчування. У раціоні мають бути:
- цитрусові;
- імбир;
- часник;
- овочі червоного та зеленого кольору;
- морепродуктів.
При поганій згортання крові заборонено приймати препарати. які розріджують кров'яну рідину. Якщо перебіг процесу набув запущеної форми, то терапевтичні заходи здійснюються лише у стаціонарних умовах.
З медикаментозних засобів призначають:

- Емосинт;
- Амінокапронову та транексамову кислоту;
- Введення АТФ;
У раціоні обов'язково присутність гречаної каші, яєць, буряків та моркви, гранату, яловичої печінки, червоного м'яса.
Щоб підтримувати кров у нормальному стані, необхідно суворо дотримуватись питного режиму. За добу нормою вважається щонайменше півтора літрів чистої води. Їжа має бути свіжою та збалансованою.
Дотримання правил харчування – профілактика багатьох захворювань людського організму. Так само важливу роль відіграють і фізичні навантаження. Вони сприяють як зміцненню тіла, а й нормалізації всіх внутрішніх процесів.
При своєчасному діагностуванні відхилень агрегаційних показників можна запобігти безлічі захворювань та ускладнень. Стежити за рівнем агрегації тромбоцитів необхідно регулярно.
Тромбоцити – це кров'яні тільця невеликого розміру, які відповідають за згортання крові. Вони допомагають зупинити крововтрату, якщо виникає кровотеча.
З появою рани тромбоцити рухаються у травмовану зону. Тут вони закріплюються на стінці пошкодженої судини, внаслідок чого кровотеча зупиняється. Такий процес називається агрегацією тромбоцитів.
Агрегація тромбоцитів – це процес, у якому відбувається склеювання кров'яних тілець друг з одним і фіксування їх у стінці травмованого судини. Завдяки цьому зупиняється кровотеча. Однак такий процес може бути небезпечним для організму. У цьому випадку утворюється тромб, який за деяких обставин може спровокувати виникнення інфаркту та інсульту. Це може статися, якщо тромбоцити є надмірно активними і агрегація здійснюється занадто швидко.
Крім того, уповільнений процес теж не обіцяє для організму нічого хорошого. У цьому випадку через повільне склеювання тромбоцитів може виникнути погана згортання крові. Така патологія стає причиною виникнення анемії. При поганій згортання крові зупинити кровотечу проблематично, що може призвести до проблем зі здоров'ям і навіть до смерті. Щоб цього не сталося, необхідно стежити за рівнем тромбоцитів у крові та за їх здатністю до склеювання.
Процес агрегації тромбоцитів під час вагітності
 Вкрай важливо, щоб агрегація тромбоцитів при вагітності протікала нормально. Якщо процес відбувається занадто повільно, то при пологах або в післяпологовий період може відкритися кровотеча з матки, яка може призвести до смерті жінки. Крім цього, якщо агрегація тромбоцитів при вагітності здійснюється швидко, то можуть утворитися тромби, які в період вагітності можуть призвести до переривання на будь-якому терміні.
Вкрай важливо, щоб агрегація тромбоцитів при вагітності протікала нормально. Якщо процес відбувається занадто повільно, то при пологах або в післяпологовий період може відкритися кровотеча з матки, яка може призвести до смерті жінки. Крім цього, якщо агрегація тромбоцитів при вагітності здійснюється швидко, то можуть утворитися тромби, які в період вагітності можуть призвести до переривання на будь-якому терміні.
Уникнути такої ситуації можна, якщо вагітність планувати та заздалегідь подбати про стан свого здоров'я. Потрібно ще до зачаття з'ясувати, в якому стані знаходяться тромбоцити, і при необхідності вжити заходів, щоб виправити ситуацію. Якщо вагітність не планувалася, то патології агрегації можна уникнути, ставши на облік ранньому терміні. Тоді лікар призначить необхідні дослідження та допоможе позбавитися патологічного стану тромбоцитів у разі виявлення такого.
Норма тромбоцитів у крові
Щоб знати, в якому стані знаходиться рівень тромбоцитів, потрібно мати уявлення про їхню норму.
Якщо говорити про норму агрегації, вона становить 25-75%. В цьому випадку процес склеювання тромбоцитів відбувається добре і ніякої небезпеки для здоров'я не становить.
Якщо спостерігаються відхилення від норми, призначається відповідне лікування, яке допомагає виправити ситуацію.Аналіз крові на агрегацію тромбоцитів
Дослідити стан тромбоцитів допомагає аналіз крові, який називається індукованою агрегацією. У цьому випадку з вени пацієнта забирається кров, яка поєднується зі спеціальними речовинами. Такі засоби мають склад, що схожий на склад клітин організму, що беруть участь у процесі агрегації. За індуктори найчастіше беруть такі речовини:
- аденозиндіфосфат (АДФ);
- колаген;
- серотонін;
- ристоцетин;
- адреналін;
- арахідонову кислоту.
Найчастіше виконується агрегація тромбоцитів із АДФ. Щоб виконати дослідження, береться спеціальний прилад. Він називається аналізатором агрегації тромбоцитів. З його допомогою через кров пропускаються світлові хвилі перед початком згортання і після завершення цього процесу. Потім оцінюється результат.
Підготовка до здачі аналізів
 Щоб результат виявився максимально точним, необхідно дотримуватись наступних правил здачі аналізу крові:
Щоб результат виявився максимально точним, необхідно дотримуватись наступних правил здачі аналізу крові:
- Дослідження виконується на голодний шлунок. У цьому випадку відмовитися від їди потрібно за 12 годин до аналізу. При цьому можна пити чисту негазовану воду.
- За 7 днів до аналізу слід припинити медикаментозне лікування деякими лікарськими засобами. Якщо це зробити неможливо, то потрібно повідомити про це лікаря, який проводить аналіз.
- За кілька днів до аналізу слід уникати стресових ситуацій та фізичних навантажень.
- За 24 години необхідно припинити пити каву, курити, вживати спиртні напої та часник.
- Не можна проводити дослідження, якщо в організмі відбувається запальний процес.
Показання до проведення аналізу
 Аналіз на агрегацію тромбоцитів іноді можна здавати з власної ініціативи.
Аналіз на агрегацію тромбоцитів іноді можна здавати з власної ініціативи. Розшифровка результату аналізу індукованої агрегації
Розшифровка показників залежить від засобу, з допомогою якого проводилося дослідження. Для цього дані порівнюють із нормою.
Якщо результати відхиляються від норми у бік збільшення, діагностують підвищену агрегацію тромбоцитів. Такий стан виникає при: 
- підвищений артеріальний тиск;
- атеросклероз;
- лейкозі;
- цукровий діабет;
- онкологічних захворюваннях ШКТ чи нирок;
- лімфогранулематоз;
- сепсисі;
- видалення селезінки хірургічним шляхом.
Підвищена агрегація тромбоцитів може призвести до виникнення інфаркту, інсульту, тромбозу та летального результату через закупорку судини тромбом.
Якщо результати відхиляються від норми у бік зменшення, то діагностується знижена агрегація тромбозів. Це відбувається через:
- захворювань крові;
- тромбоцитопатії;
- Вживання антиагрегантів.
При зниженій агрегації судини стають крихкими. Крім цього, важко процес зупинки кровотечі, що може стати причиною смерті людини.
Засоби, що знижують процес агрегації
Деякі засоби пригнічують процес агрегації. До таких препаратів належать антиагреганти. До інгібіторів агрегації тромбоцитів належать такі засоби, як ацетилсаліцилова кислота, ібустрин, мікристин та інші. Такі препарати призначаються для лікування деяких захворювань. Однак якщо процес агрегації різко відхиляється від норми, препарати-інгібітори слід замінити іншими засобами, які не призводять до таких наслідків. Якщо ж такої можливості немає, лікар може призначити спеціальні препарати, що сприяють агрегації.
І підвищена та знижена агрегація може призвести до сумних наслідків. Тому залишати такі ситуації поза увагою не можна. У таких випадках слід звернутися до лікаря за призначенням відповідного лікування.