Sn เป็นองค์ประกอบทางเคมีตามที่อ่าน ชื่อขององค์ประกอบทางเคมี
2.1. ภาษาเคมีและส่วนประกอบ
มนุษยชาติใช้ภาษาต่างๆ มากมาย ยกเว้น ภาษาธรรมชาติ(ญี่ปุ่น อังกฤษ รัสเซีย รวมแล้วกว่า 2.5 พัน) ก็ยังมี ภาษาเทียมเช่น ภาษาเอสเปรันโต ในบรรดาภาษาเทียมคือ ภาษาหลากหลาย วิทยาศาสตร์. ดังนั้น ในวิชาเคมี เราจึงใช้ตัวมันเอง ภาษาเคมี.
ภาษาเคมี- ระบบสัญลักษณ์และแนวคิดที่ออกแบบมาเพื่อการบันทึกและการส่งข้อมูลทางเคมีที่กระชับ รัดกุม และเป็นภาพ
ข้อความที่เขียนด้วยภาษาธรรมชาติส่วนใหญ่แบ่งออกเป็นประโยค ประโยคเป็นคำ และคำเป็นตัวอักษร หากเราเรียกประโยค คำและตัวอักษรว่าส่วนต่างๆ ของภาษา เราก็จะแยกแยะส่วนที่คล้ายคลึงกันในภาษาเคมีได้ (ตารางที่ 2)
ตารางที่ 2ส่วนของภาษาเคมี
เป็นไปไม่ได้ที่จะเชี่ยวชาญภาษาใด ๆ ในคราวเดียว สิ่งนี้ใช้ได้กับภาษาเคมีด้วย ดังนั้น สำหรับตอนนี้ คุณจะทำความคุ้นเคยกับพื้นฐานของภาษานี้เท่านั้น: เรียนรู้ "ตัวอักษร" เรียนรู้ที่จะเข้าใจความหมายของ "คำ" และ "ประโยค" ในตอนท้ายของบทนี้ คุณจะได้พบกับ ชื่อเรื่องสารเคมีเป็นส่วนสำคัญของภาษาเคมี ในขณะที่คุณเรียนวิชาเคมี ความรู้เกี่ยวกับภาษาเคมีของคุณจะขยายและลึกซึ้งยิ่งขึ้น
ภาษาเคมี
1. คุณรู้จักภาษาเทียมอะไรบ้าง (ยกเว้นชื่อในตำราเรียน)?
2. ภาษาธรรมชาติแตกต่างจากภาษาเทียมอย่างไร?
3. คุณคิดว่าสามารถทำได้โดยไม่ต้องใช้ภาษาเคมีเมื่ออธิบายปรากฏการณ์ทางเคมีหรือไม่? ถ้าไม่ทำไม? ถ้าเป็นเช่นนั้นข้อดีและข้อเสียของคำอธิบายดังกล่าวจะเป็นอย่างไร
2.2. สัญลักษณ์ขององค์ประกอบทางเคมี
สัญลักษณ์สำหรับองค์ประกอบทางเคมีหมายถึงองค์ประกอบนั้นเองหรือหนึ่งอะตอมขององค์ประกอบนั้น
แต่ละสัญลักษณ์ดังกล่าวเป็นชื่อละตินแบบย่อขององค์ประกอบทางเคมี ซึ่งประกอบด้วยตัวอักษรละตินหนึ่งหรือสองตัว (ดูภาคผนวก 1 สำหรับอักษรละติน) สัญลักษณ์เป็นตัวพิมพ์ใหญ่ สัญลักษณ์เช่นเดียวกับชื่อรัสเซียและละตินขององค์ประกอบบางอย่างมีอยู่ในตารางที่ 3 ข้อมูลเกี่ยวกับที่มาของชื่อละตินก็มีให้เช่นกัน ไม่มีกฎทั่วไปสำหรับการออกเสียงสัญลักษณ์ ดังนั้น ตารางที่ 3 ยังแสดง "การอ่าน" ของสัญลักษณ์ นั่นคือวิธีที่สัญลักษณ์นี้อ่านในสูตรทางเคมี
เป็นไปไม่ได้ที่จะเปลี่ยนชื่อองค์ประกอบด้วยสัญลักษณ์ด้วยวาจาและอนุญาตให้ใช้ในข้อความที่เขียนด้วยลายมือหรือพิมพ์ แต่ไม่แนะนำ ปัจจุบันรู้จักองค์ประกอบทางเคมี 110 รายการ 109 รายการมีชื่อและสัญลักษณ์ที่ได้รับอนุมัติจากนานาชาติ สหภาพเคมีเชิงทฤษฎีและประยุกต์ (IUPAC)
ตารางที่ 3 ให้ข้อมูลเกี่ยวกับองค์ประกอบ 33 เท่านั้น สิ่งเหล่านี้คือองค์ประกอบที่คุณจะพบเป็นอย่างแรกเมื่อเรียนวิชาเคมี ชื่อรัสเซีย (ตามลำดับตัวอักษร) และสัญลักษณ์ขององค์ประกอบทั้งหมดมีอยู่ในภาคผนวก 2
ตารางที่ 3ชื่อและสัญลักษณ์ขององค์ประกอบทางเคมีบางชนิด
ชื่อ |
||||
ละติน |
การเขียน |
|||
| - | การเขียน |
ต้นทาง |
- | - |
| ไนโตรเจน | นู๋ไอโตรจีเนียม | จากภาษากรีก. “กำเนิดดินประสิว” | "th" | |
| อลูมิเนียม | อัลยูมิเนียม | ตั้งแต่ ลท. "สารส้ม" | "อลูมิเนียม" | |
| อาร์กอน | อากอน | จากภาษากรีก. "ไม่ใช้งาน" | "อาร์กอน" | |
| แบเรียม | บาเรียม | จากภาษากรีก. " หนัก" | "แบเรียม" | |
| บอ | บี orum | จากภาษาอาหรับ "แร่ขาว" | "บ่อ" | |
| โบรมีน | Br omum | จากภาษากรีก. "มีกลิ่นเหม็น" | "โบรมีน" | |
| ไฮโดรเจน | ชมไฮโดรเจน | จากภาษากรีก. "ให้กำเนิดน้ำ" | "เถ้า" | |
| ฮีเลียม | เขาเลียม | จากภาษากรีก. " ดวงอาทิตย์" | "ฮีเลียม" | |
| เหล็ก | เฟรัม | ตั้งแต่ ลท. "ดาบ" | "เฟอร์รัม" | |
| ทอง | Auรัม | ตั้งแต่ ลท. "การเผาไหม้" | "ออรัม" | |
| ไอโอดีน | ฉัน odum | จากภาษากรีก. " สีม่วง" | "ไอโอดีน" | |
| โพแทสเซียม | K alium | จากภาษาอาหรับ "น้ำด่าง" | "โพแทสเซียม" | |
| แคลเซียม | Caแอลเซียม | ตั้งแต่ ลท. "หินปูน" | "แคลเซียม" | |
| ออกซิเจน | อู๋ไซเจเนียม | จากภาษากรีก. "ผู้ผลิตกรด" | " เกี่ยวกับ" | |
| ซิลิคอน | ซิลิเซียม | ตั้งแต่ ลท. "หินเหล็กไฟ" | "ซิลิเซียม" | |
| คริปทอน | kr ypton | จากภาษากรีก. "ที่ซ่อนอยู่" | "คริปทอน" | |
| แมกนีเซียม | เอ็มเอ gนีเซียม | จากชื่อ คาบสมุทรแมกนีเซีย | "แมกนีเซียม" | |
| แมงกานีส | เอ็มเอ นกานุม | จากภาษากรีก. "การทำให้บริสุทธิ์" | "แมงกานีส" | |
| ทองแดง | Cuพรุม | จากภาษากรีก. ชื่อ เกี่ยวกับ. ไซปรัส | "คิวปรัม" | |
| โซเดียม | นาชัยชนะ | จากภาษาอาหรับ "ผงซักฟอก" | "โซเดียม" | |
| นีออน | เน่บน | จากภาษากรีก. " ใหม่" | "นีออน" | |
| นิกเกิล | นิโคลัม | จากเขา. "ทองแดงของเซนต์นิโคลัส" | "นิกเกิล" | |
| ปรอท | ชม ydrar g yrum | ลาด. "เงินเหลว" | "ไฮดราไจรัม" | |
| ตะกั่ว | พี lum ขอืม | ตั้งแต่ ลท. ชื่อของโลหะผสมของตะกั่วและดีบุก | "ลูกดิ่ง" | |
| กำมะถัน | สกำมะถัน | จากภาษาสันสกฤต "ผงไวไฟ" | "เอส" | |
| เงิน | อา r g entum | จากภาษากรีก. "สีอ่อน" | "อาร์เจนทัม" | |
| คาร์บอน | ค arboneum | ตั้งแต่ ลท. "ถ่านหิน" | "ซี" | |
| ฟอสฟอรัส | พีฟอสฟอรัส | จากภาษากรีก. "ผู้ให้แสงสว่าง" | "วิชาพลศึกษา" | |
| ฟลูออรีน | F luorum | ตั้งแต่ ลท. กริยา "ไหล" | "ฟลูออรีน" | |
| คลอรีน | Cl orum | จากภาษากรีก. "เขียว" | "คลอรีน" | |
| โครเมียม | คชม r omium | จากภาษากรีก. "สีย้อม" | "โครเมียม" | |
| ซีเซียม | คแอ่ สอุม | ตั้งแต่ ลท. "ฟ้าคราม" | "ซีเซียม" | |
| สังกะสี | Zฉัน นน้ำเชื้อ | จากเขา. "ดีบุก" | "สังกะสี" | |
2.3. สูตรทางเคมี
ใช้เพื่ออ้างถึงสารเคมี สูตรเคมี.
สำหรับสารโมเลกุล สูตรทางเคมียังสามารถระบุหนึ่งโมเลกุลของสารนี้
ข้อมูลเกี่ยวกับสารอาจแตกต่างกันจึงมีความต่างกัน ประเภทของสูตรเคมี.
สูตรทางเคมีแบ่งออกเป็นสี่ประเภทหลักขึ้นอยู่กับความสมบูรณ์ของข้อมูล: โปรโตซัว,
โมเลกุล, โครงสร้างและ เชิงพื้นที่.
ตัวห้อยในสูตรที่ง่ายที่สุดไม่มีตัวหารร่วม
ดัชนี "1" ไม่ได้ใส่ในสูตร
ตัวอย่างของสูตรที่ง่ายที่สุด: น้ำ - H 2 O ออกซิเจน - O กำมะถัน - S ฟอสฟอรัสออกไซด์ - P 2 O 5 บิวเทน - C 2 H 5 กรดฟอสฟอริก - H 3 PO 4 โซเดียมคลอไรด์ (เกลือแกง) - โซเดียมคลอไรด์
สูตรน้ำที่ง่ายที่สุด (H 2 O) แสดงว่าน้ำประกอบด้วยธาตุ ไฮโดรเจน(H) และองค์ประกอบ ออกซิเจน(O) และในส่วนใดส่วนหนึ่ง (ส่วนหนึ่งเป็นส่วนหนึ่งของบางสิ่งที่สามารถแบ่งออกได้โดยไม่สูญเสียคุณสมบัติของน้ำ) จำนวนของไฮโดรเจนอะตอมเป็นสองเท่าของจำนวนอะตอมของออกซิเจน
จำนวนอนุภาค, รวมทั้ง จำนวนอะตอม, เขียนแทนด้วยอักษรละติน นู๋. แสดงถึงจำนวนอะตอมไฮโดรเจน - นู๋ H และจำนวนอะตอมของออกซิเจนคือ นู๋ O เราสามารถเขียนได้ว่า
หรือ นู๋ชม: นู๋ O=2:1.
สูตรที่ง่ายที่สุดของกรดฟอสฟอริก (H 3 PO 4) แสดงให้เห็นว่ากรดฟอสฟอริกประกอบด้วยอะตอม ไฮโดรเจน, อะตอม ฟอสฟอรัสและอะตอม ออกซิเจนและอัตราส่วนของจำนวนอะตอมของธาตุเหล่านี้ในส่วนใดส่วนหนึ่งของกรดฟอสฟอริกเท่ากับ 3:1:4 นั่นคือ
นิวแฮมป์เชียร์: นู๋ป: นู๋ O=3:1:4.

สูตรที่ง่ายที่สุดสามารถวาดขึ้นสำหรับสารเคมีแต่ละชนิดและสำหรับสารโมเลกุลนอกจากนี้ สูตรโมเลกุล.
ตัวอย่างสูตรโมเลกุล: น้ำ - H 2 O ออกซิเจน - O 2 กำมะถัน - S 8 ฟอสฟอรัสออกไซด์ - P 4 O 10 บิวเทน - C 4 H 10 กรดฟอสฟอริก - H 3 PO 4
สารที่ไม่ใช่โมเลกุลไม่มีสูตรโมเลกุล
ลำดับของการเขียนสัญลักษณ์ขององค์ประกอบในสูตรที่ง่ายและซับซ้อนที่สุดจะพิจารณาจากกฎของภาษาเคมี ซึ่งคุณจะได้เรียนรู้เมื่อเรียนวิชาเคมี ลำดับของอักขระไม่ส่งผลต่อข้อมูลที่ถ่ายทอดโดยสูตรเหล่านี้
ของป้ายที่สะท้อนถึงโครงสร้างของสารที่เราจะใช้จนถึงตอนนี้เท่านั้น วาเลนซ์จังหวะ("แดช") เครื่องหมายนี้แสดงถึงการมีอยู่ระหว่างอะตอมของสิ่งที่เรียกว่า พันธะโควาเลนต์(นี่คือการเชื่อมต่อประเภทใดและคุณสมบัติของมันคืออะไรคุณจะพบได้ในไม่ช้า)

ในโมเลกุลของน้ำ อะตอมของออกซิเจนเชื่อมต่อกันด้วยพันธะธรรมดา (เดี่ยว) กับไฮโดรเจนสองอะตอม และอะตอมของไฮโดรเจนจะไม่เชื่อมต่อถึงกัน นี้แสดงให้เห็นอย่างชัดเจนโดยสูตรโครงสร้างของน้ำ ![]()
อีกตัวอย่างหนึ่ง: โมเลกุลกำมะถัน S 8 . ในโมเลกุลนี้ อะตอมของกำมะถัน 8 ตัวก่อให้เกิดวัฏจักรแปดสมาชิกซึ่งแต่ละอะตอมของกำมะถันเชื่อมต่อกับอะตอมอื่นอีกสองอะตอมด้วยพันธะธรรมดา เปรียบเทียบสูตรโครงสร้างของกำมะถันกับแบบจำลองสามมิติของโมเลกุลที่แสดงในรูปที่ 3. โปรดทราบว่าสูตรโครงสร้างของกำมะถันไม่ได้ถ่ายทอดรูปร่างของโมเลกุล แต่แสดงเฉพาะลำดับของการเชื่อมต่ออะตอมด้วยพันธะโควาเลนต์

สูตรโครงสร้างของกรดฟอสฟอริกแสดงให้เห็นว่าในโมเลกุลของสารนี้อะตอมออกซิเจนหนึ่งในสี่อะตอมเชื่อมต่อกับอะตอมของฟอสฟอรัสด้วยพันธะคู่เท่านั้นและอะตอมของฟอสฟอรัสก็เชื่อมต่อกับอะตอมออกซิเจนอีกสามอะตอมด้วยพันธะธรรมดา . นอกจากนี้ ออกซิเจนทั้งสามอะตอมแต่ละอะตอมยังเชื่อมต่อกันด้วยพันธะง่ายๆ กับอะตอมไฮโดรเจนหนึ่งในสามอะตอมที่มีอยู่ในโมเลกุล/p>
เปรียบเทียบแบบจำลองสามมิติของโมเลกุลมีเทนต่อไปนี้กับสูตรเชิงพื้นที่ โครงสร้าง และโมเลกุล:
|
|
|
ในสูตรเชิงพื้นที่ของมีเทน วาเลนซ์สโตรครูปลิ่ม แสดงให้เห็นว่าอะตอมของไฮโดรเจนตัวใด "อยู่ใกล้เรามากกว่า" และอันไหน "อยู่ไกลจากเรา" ราวกับอยู่ในมุมมอง
บางครั้งสูตรเชิงพื้นที่ระบุความยาวพันธะและค่ามุมระหว่างพันธะในโมเลกุลดังแสดงในตัวอย่างโมเลกุลของน้ำ

สารที่ไม่ใช่โมเลกุลไม่มีโมเลกุล เพื่อความสะดวกในการคำนวณทางเคมีในสารที่ไม่ใช่โมเลกุลเรียกว่า หน่วยสูตร.
ตัวอย่างองค์ประกอบของหน่วยสูตรของสารบางชนิด: 1) ซิลิกอนไดออกไซด์ (ทรายควอทซ์, ควอทซ์) SiO 2 - หน่วยสูตรประกอบด้วยอะตอมซิลิกอนหนึ่งอะตอมและออกซิเจนสองอะตอม 2) โซเดียมคลอไรด์ (เกลือทั่วไป) NaCl - หน่วยสูตรประกอบด้วยโซเดียมอะตอมหนึ่งอะตอมและคลอรีนหนึ่งอะตอม 3) ธาตุเหล็ก Fe - หน่วยสูตรประกอบด้วยเหล็ก 1 อะตอม หน่วยสูตรเป็นส่วนที่เล็กที่สุดของสารที่คงคุณสมบัติทางเคมีไว้เช่นเดียวกับโมเลกุล
ตารางที่ 4
ข้อมูลที่ถ่ายทอดโดยสูตรประเภทต่างๆ
ประเภทสูตร |
ข้อมูลผ่านตามสูตร |
|
| โปรโตซัว โมเลกุล โครงสร้าง เชิงพื้นที่ |
|
|
ให้เราพิจารณาด้วยตัวอย่างว่าสูตรข้อมูลประเภทต่าง ๆ ให้อะไรแก่เราบ้าง
1. สาร: กรดน้ำส้ม. สูตรที่ง่ายที่สุดคือ CH 2 O สูตรโมเลกุลคือ C 2 H 4 O 2 สูตรโครงสร้าง

สูตรที่ง่ายที่สุดบอกเราว่า
1) กรดอะซิติกประกอบด้วยคาร์บอน ไฮโดรเจน และออกซิเจน
2) ในสารนี้ จำนวนอะตอมของคาร์บอนสัมพันธ์กับจำนวนอะตอมไฮโดรเจนและจำนวนอะตอมของออกซิเจน เช่น 1:2:1 นั่นคือ นู๋ชม: นู๋ค: นู๋ O = 1:2:1.
สูตรโมเลกุลเสริมว่า
3) ในโมเลกุลของกรดอะซิติก - คาร์บอน 2 อะตอม, ไฮโดรเจน 4 อะตอมและออกซิเจน 2 อะตอม
สูตรโครงสร้างเสริมว่า
4, 5) ในโมเลกุล อะตอมของคาร์บอนสองอะตอมเชื่อมโยงกันด้วยพันธะเดี่ยว นอกจากนี้หนึ่งในนั้นเกี่ยวข้องกับอะตอมไฮโดรเจนสามอะตอมโดยแต่ละพันธะเดี่ยวและอีกพันธะหนึ่งมีอะตอมออกซิเจนสองอะตอมด้วยพันธะคู่หนึ่งพันธะและอีกพันธะหนึ่ง อะตอมออกซิเจนสุดท้ายยังเชื่อมโยงกันด้วยพันธะง่ายๆ กับอะตอมไฮโดรเจนที่สี่
2. สาร: เกลือแกง.
สูตรที่ง่ายที่สุดคือ NaCl
1) โซเดียมคลอไรด์ประกอบด้วยโซเดียมและคลอรีน
2) ในสารนี้ จำนวนโซเดียมอะตอมเท่ากับจำนวนอะตอมของคลอรีน
3. สาร: เหล็ก.
สูตรที่ง่ายที่สุดคือเฟ
1) องค์ประกอบของสารนี้มีเพียงธาตุเหล็กนั่นคือเป็นสารธรรมดา
4. สาร: กรดไตรเมตาฟอสฟอริก . สูตรที่ง่ายที่สุดคือ HPO 3 สูตรโมเลกุลคือ H 3 P 3 O 9 สูตรโครงสร้าง

1) องค์ประกอบของกรดไตรเมตาฟอสฟอริก ได้แก่ ไฮโดรเจน ฟอสฟอรัส และออกซิเจน
2) นู๋ชม: นู๋ป: นู๋ O = 1:1:3
3) โมเลกุลประกอบด้วยไฮโดรเจน 3 อะตอม ฟอสฟอรัส 3 อะตอม และออกซิเจน 9 อะตอม
4, 5) อะตอมของฟอสฟอรัสสามอะตอมและออกซิเจนสามอะตอม สลับกัน ก่อรูปวงจรหกส่วน ลิงก์ทั้งหมดในลูปนั้นเรียบง่าย นอกจากนี้ อะตอมของฟอสฟอรัสแต่ละอะตอมยังสัมพันธ์กับออกซิเจนอีก 2 อะตอม โดยอันหนึ่งเป็นพันธะคู่ และอีกอันเป็นพันธะธรรมดา อะตอมออกซิเจนทั้งสามแต่ละอะตอมที่เชื่อมโยงกันด้วยพันธะธรรมดากับอะตอมของฟอสฟอรัสก็เชื่อมโยงกันด้วยพันธะธรรมดากับอะตอมไฮโดรเจน
| กรดฟอสฟอริก - H 3 PO 4(ชื่ออื่นคือกรดฟอสฟอริก) เป็นสารผลึกไม่มีสีโปร่งใสของโครงสร้างโมเลกุล ละลายที่ 42 o C สารนี้ละลายได้ดีในน้ำและแม้กระทั่งดูดซับไอน้ำจากอากาศ (ดูดความชื้น) กรดฟอสฟอริกผลิตในปริมาณมากและใช้เป็นหลักในการผลิตปุ๋ยฟอสเฟต เช่นเดียวกับในอุตสาหกรรมเคมี ในการผลิตไม้ขีดไฟ และแม้แต่ในการก่อสร้าง นอกจากนี้กรดฟอสฟอริกยังใช้ในการผลิตซีเมนต์ในเทคโนโลยีทันตกรรมซึ่งเป็นส่วนหนึ่งของยาหลายชนิด กรดนี้มีราคาถูกเพียงพอที่ในบางประเทศ เช่น สหรัฐอเมริกา กรดฟอสฟอริกบริสุทธิ์มาก ซึ่งเจือจางด้วยน้ำสูง จะถูกเติมลงในเครื่องดื่มเพื่อทดแทนกรดซิตริกราคาแพง |
| มีเทน - CH 4หากคุณมีเตาแก๊สอยู่ที่บ้าน คุณจะเจอสารนี้ทุกวัน: ก๊าซธรรมชาติที่เผาไหม้ในหัวเตาของคุณคือมีเทน 95% มีเทนเป็นก๊าซที่ไม่มีสีและไม่มีกลิ่นซึ่งมีจุดเดือด -161 o C เมื่อผสมกับอากาศจะเกิดการระเบิดได้ ซึ่งอธิบายการระเบิดและไฟที่บางครั้งเกิดขึ้นในเหมืองถ่านหิน ชื่อที่สามของก๊าซมีเทน - ก๊าซหนอง - เกิดจากการที่ฟองอากาศของก๊าซเฉพาะนี้เพิ่มขึ้นจากก้นหนองบึงซึ่งเกิดขึ้นจากกิจกรรมของแบคทีเรียบางชนิด ในอุตสาหกรรมมีเทนใช้เป็นเชื้อเพลิงและวัตถุดิบในการผลิตสารอื่น ๆ มีเทนเป็นก๊าซที่ง่ายที่สุด ไฮโดรคาร์บอน. สารประเภทนี้ยังรวมถึงอีเทน (C 2 H 6) โพรเพน (C 3 H 8) เอทิลีน (C 2 H 4) อะเซทิลีน (C 2 H 2) และสารอื่น ๆ อีกมากมาย |
ตารางที่ 5.ตัวอย่างสูตรประเภทต่างๆ ของสารบางชนิด-
วิธีการใช้ตารางธาตุ? สำหรับคนที่ไม่ได้ฝึกหัด การอ่านตารางธาตุก็เหมือนกับการดูอักษรรูนโบราณของเอลฟ์เพื่อหาคนแคระ และตารางธาตุสามารถบอกอะไรเกี่ยวกับโลกได้มากมาย
นอกจากจะให้บริการคุณในการสอบแล้ว ยังจำเป็นสำหรับการแก้ปัญหาทางเคมีและทางกายภาพจำนวนมากอีกด้วย แต่จะอ่านได้อย่างไร? โชคดีที่วันนี้ทุกคนสามารถเรียนรู้ศิลปะนี้ได้ ในบทความนี้เราจะอธิบายวิธีทำความเข้าใจตารางธาตุ
ระบบธาตุเคมีเป็นระยะ (ตารางของ Mendeleev) เป็นการจำแนกองค์ประกอบทางเคมีที่สร้างการพึ่งพาคุณสมบัติต่าง ๆ ขององค์ประกอบในประจุของนิวเคลียสของอะตอม
ประวัติความเป็นมาของการสร้างโต๊ะ
Dmitri Ivanovich Mendeleev ไม่ใช่นักเคมีธรรมดาๆ ถ้ามีคนคิดอย่างนั้น เขาเป็นนักเคมี นักฟิสิกส์ นักธรณีวิทยา นักมาตรวิทยา นักนิเวศวิทยา นักเศรษฐศาสตร์ ช่างน้ำมัน นักบินอวกาศ ผู้ผลิตเครื่องมือและครู ในช่วงชีวิตของเขา นักวิทยาศาสตร์ได้ทำการวิจัยพื้นฐานมากมายในด้านความรู้ต่างๆ ตัวอย่างเช่น เป็นที่เชื่อกันอย่างกว้างขวางว่า Mendeleev เป็นผู้คำนวณความแรงในอุดมคติของวอดก้า - 40 องศา
เราไม่ทราบว่า Mendeleev ปฏิบัติต่อวอดก้าอย่างไร แต่เป็นที่ทราบแน่ชัดว่าวิทยานิพนธ์ของเขาในหัวข้อ "วาทกรรมเกี่ยวกับการรวมกันของแอลกอฮอล์กับน้ำ" ไม่มีส่วนเกี่ยวข้องกับวอดก้าและพิจารณาความเข้มข้นของแอลกอฮอล์จาก 70 องศา ด้วยคุณธรรมทั้งหมดของนักวิทยาศาสตร์ การค้นพบกฎธาตุเคมีเป็นระยะ ซึ่งเป็นหนึ่งในกฎพื้นฐานของธรรมชาติ ทำให้เขามีชื่อเสียงมากที่สุด

มีตำนานตามที่นักวิทยาศาสตร์ใฝ่ฝันถึงระบบธาตุ หลังจากนั้นเขาก็ต้องสรุปความคิดที่ปรากฏขึ้นเท่านั้น แต่ถ้าทุกอย่างเรียบง่าย .. การสร้างตารางธาตุรุ่นนี้ดูเหมือนจะไม่มีอะไรมากไปกว่าตำนาน เมื่อถูกถามว่าเปิดโต๊ะอย่างไร Dmitry Ivanovich เองก็ตอบว่า: “ ฉันคิดเกี่ยวกับมันมายี่สิบปีแล้วและคุณคิดว่า: ฉันนั่งและทันใดนั้น ... ก็พร้อม”
ในช่วงกลางของศตวรรษที่สิบเก้า นักวิทยาศาสตร์หลายคนพยายามปรับปรุงองค์ประกอบทางเคมีที่รู้จัก (63 องค์ประกอบที่รู้จัก) ให้มีประสิทธิภาพมากขึ้น ตัวอย่างเช่น ในปี 1862 Alexandre Émile Chancourtois วางองค์ประกอบตามเกลียวและสังเกตคุณสมบัติทางเคมีซ้ำ ๆ ของวัฏจักร
นักเคมีและนักดนตรี จอห์น อเล็กซานเดอร์ นิวแลนด์ส เสนอตารางธาตุในแบบฉบับของเขาในปี พ.ศ. 2409 ข้อเท็จจริงที่น่าสนใจคือในการจัดเรียงองค์ประกอบ นักวิทยาศาสตร์พยายามค้นหาความกลมกลืนทางดนตรีที่ลึกลับ ท่ามกลางความพยายามอื่น ๆ คือความพยายามของ Mendeleev ซึ่งได้รับการสวมมงกุฎด้วยความสำเร็จ

ในปีพ.ศ. 2412 ได้มีการตีพิมพ์โครงร่างแรกของตารางและวันที่ 1 มีนาคม พ.ศ. 2412 ถือเป็นวันแห่งการค้นพบกฎหมายเป็นระยะ สาระสำคัญของการค้นพบของ Mendeleev คือคุณสมบัติขององค์ประกอบที่มีมวลอะตอมเพิ่มขึ้นไม่เปลี่ยนแปลงอย่างจำเจ แต่เป็นระยะ
รุ่นแรกของตารางมีเพียง 63 องค์ประกอบ แต่ Mendeleev ได้ทำการตัดสินใจที่ไม่ได้มาตรฐานจำนวนมาก ดังนั้น เขาเดาว่าจะทิ้งที่ในตารางไว้สำหรับธาตุที่ยังไม่ถูกค้นพบ และยังเปลี่ยนมวลอะตอมของธาตุบางธาตุด้วย ความถูกต้องพื้นฐานของกฎหมายที่ Mendeleev ได้รับนั้นได้รับการยืนยันไม่นานหลังจากการค้นพบแกลเลียม สแกนเดียม และเจอร์เมเนียม ซึ่งนักวิทยาศาสตร์คาดการณ์ถึงการมีอยู่ของมัน
มุมมองสมัยใหม่ของตารางธาตุ
ด้านล่างเป็นตารางเอง
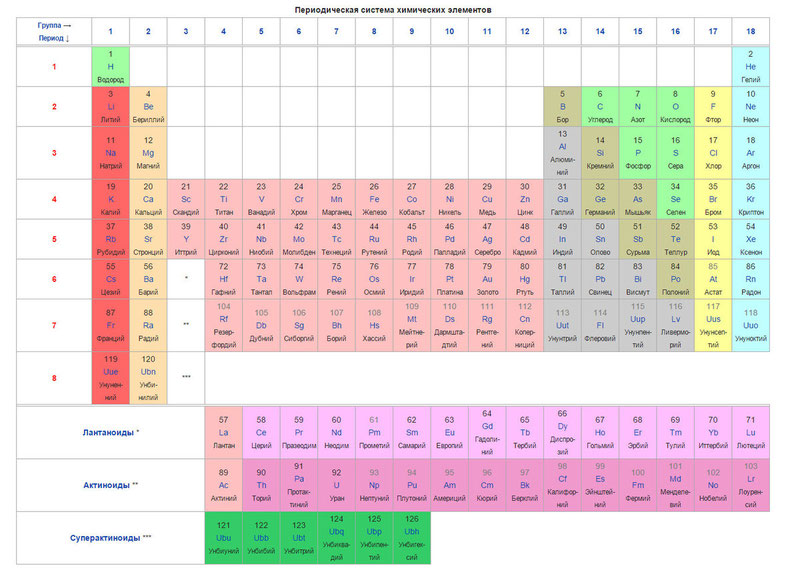
ทุกวันนี้ แทนที่จะใช้น้ำหนักอะตอม (มวลอะตอม) แนวคิดของเลขอะตอม (จำนวนโปรตอนในนิวเคลียส) ถูกนำมาใช้เพื่อจัดลำดับองค์ประกอบ ตารางประกอบด้วยองค์ประกอบ 120 ซึ่งจัดเรียงจากซ้ายไปขวาจากน้อยไปหามากของเลขอะตอม (จำนวนโปรตอน)
คอลัมน์ของตารางเรียกว่ากลุ่ม และแถวคือจุด มี 18 กลุ่มและ 8 คาบในตาราง
- คุณสมบัติของโลหะจะลดลงเมื่อเคลื่อนที่ไปตามช่วงเวลาจากซ้ายไปขวา และเพิ่มขึ้นในทิศทางตรงกันข้าม
- ขนาดของอะตอมลดลงเมื่อเคลื่อนจากซ้ายไปขวาตามช่วงเวลา
- เมื่อเคลื่อนที่จากบนลงล่างในกลุ่ม คุณสมบัติของโลหะที่ลดลงจะเพิ่มขึ้น
- คุณสมบัติการออกซิไดซ์และอโลหะเพิ่มขึ้นตามระยะเวลาจากซ้ายไปขวา
เราเรียนรู้อะไรเกี่ยวกับองค์ประกอบจากตาราง ตัวอย่างเช่น ลองพิจารณาองค์ประกอบที่สามในตาราง - ลิเธียม และพิจารณาอย่างละเอียด

ก่อนอื่น เราจะเห็นสัญลักษณ์ขององค์ประกอบและชื่อของมันอยู่ข้างใต้ ที่มุมบนซ้ายคือเลขอะตอมขององค์ประกอบ ตามลำดับที่องค์ประกอบนั้นอยู่ในตาราง เลขอะตอมดังที่ได้กล่าวไปแล้วนั้นมีค่าเท่ากับจำนวนโปรตอนในนิวเคลียส จำนวนโปรตอนบวกมักจะเท่ากับจำนวนอิเล็กตรอนเชิงลบในอะตอม (ยกเว้นไอโซโทป)
มวลอะตอมแสดงอยู่ใต้เลขอะตอม (ในตารางเวอร์ชันนี้) ถ้าเราปัดมวลอะตอมเป็นจำนวนเต็มที่ใกล้เคียงที่สุด เราจะได้ค่าที่เรียกว่าเลขมวล ความแตกต่างระหว่างเลขมวลกับเลขอะตอมให้จำนวนนิวตรอนในนิวเคลียส ดังนั้นจำนวนนิวตรอนในนิวเคลียสฮีเลียมคือสองและในลิเธียม - สี่
ดังนั้นหลักสูตร "Mendeleev's Table for Dummies" ของเราจึงสิ้นสุดลง โดยสรุป เราขอเชิญคุณชมวิดีโอเฉพาะเรื่อง และเราหวังว่าคำถามเกี่ยวกับวิธีใช้ตารางธาตุของ Mendeleev จะมีความชัดเจนมากขึ้นสำหรับคุณ เราเตือนคุณว่าการเรียนรู้วิชาใหม่นั้นมีประสิทธิภาพมากกว่าเสมอ ไม่ใช่เพียงลำพัง แต่ด้วยความช่วยเหลือจากที่ปรึกษาที่มีประสบการณ์ นั่นคือเหตุผลที่คุณไม่ควรลืมเกี่ยวกับบริการนักเรียนซึ่งยินดีที่จะแบ่งปันความรู้และประสบการณ์กับคุณ
การเรียนการสอน
ระบบเป็นระยะคือ "บ้าน" หลายชั้นซึ่งมีอพาร์ทเมนท์จำนวนมากตั้งอยู่ "ผู้เช่า" แต่ละคนหรือในอพาร์ตเมนต์ของเขาเองตามจำนวนที่กำหนดซึ่งเป็นแบบถาวร นอกจากนี้ องค์ประกอบยังมี "นามสกุล" หรือชื่อ เช่น ออกซิเจน โบรอน หรือไนโตรเจน นอกเหนือจากข้อมูลเหล่านี้แล้ว ยังมีการระบุ "อพาร์ตเมนต์" หรือข้อมูล เช่น มวลอะตอมสัมพัทธ์ ซึ่งอาจมีค่าที่แน่นอนหรือค่าที่ปัดเศษ
เช่นเดียวกับในบ้านใด ๆ มี "ทางเข้า" คือกลุ่ม นอกจากนี้ ในกลุ่ม องค์ประกอบจะอยู่ที่ด้านซ้ายและด้านขวา ขึ้นรูป . ขึ้นอยู่กับด้านที่มีมากกว่านั้นเรียกว่าด้านหลัก กลุ่มย่อยอื่น ๆ ตามลำดับจะเป็นรอง นอกจากนี้ในตารางยังมี "พื้น" หรือช่วงเวลา ยิ่งไปกว่านั้น ช่วงเวลาสามารถเป็นได้ทั้งขนาดใหญ่ (ประกอบด้วยสองแถว) และช่วงเวลาเล็ก (มีเพียงแถวเดียว)
ตามตาราง คุณสามารถแสดงโครงสร้างของอะตอมของธาตุ ซึ่งแต่ละธาตุมีนิวเคลียสที่มีประจุบวก ซึ่งประกอบด้วยโปรตอนและนิวตรอน ตลอดจนอิเล็กตรอนที่มีประจุลบที่หมุนรอบตัวมัน จำนวนของโปรตอนและอิเล็กตรอนตรงกันเป็นตัวเลขและถูกกำหนดในตารางด้วยเลขลำดับขององค์ประกอบ ตัวอย่างเช่น ธาตุเคมีกำมะถันมี #16 ดังนั้นจะมี 16 โปรตอนและ 16 อิเล็กตรอน
ในการกำหนดจำนวนนิวตรอน (อนุภาคเป็นกลางยังอยู่ในนิวเคลียส) ให้ลบหมายเลขซีเรียลออกจากมวลอะตอมสัมพัทธ์ของธาตุ ตัวอย่างเช่น เหล็กมีมวลอะตอมสัมพัทธ์เท่ากับ 56 และเลขลำดับเท่ากับ 26 ดังนั้น 56 - 26 = 30 โปรตอนในเหล็ก
อิเล็กตรอนอยู่ในระยะต่าง ๆ จากนิวเคลียส ก่อตัวเป็นระดับอิเล็กทรอนิกส์ ในการกำหนดจำนวนระดับอิเล็กทรอนิกส์ (หรือพลังงาน) คุณต้องดูจำนวนช่วงเวลาที่องค์ประกอบนั้นตั้งอยู่ เช่น อลูมิเนียมอยู่ในระยะที่ 3 จึงจะมี 3 ระดับ
ตามหมายเลขกลุ่ม (แต่สำหรับกลุ่มย่อยหลักเท่านั้น) คุณสามารถกำหนดความจุสูงสุดได้ ตัวอย่างเช่น องค์ประกอบของกลุ่มแรกของกลุ่มย่อยหลัก (ลิเธียม โซเดียม โพแทสเซียม ฯลฯ) มีความจุเท่ากับ 1 ดังนั้น องค์ประกอบของกลุ่มที่สอง (เบริลเลียม แมกนีเซียม แคลเซียม ฯลฯ) จะมี ความจุ 2
คุณยังสามารถวิเคราะห์คุณสมบัติขององค์ประกอบโดยใช้ตาราง จากซ้ายไปขวา คุณสมบัติของโลหะจะลดลงและคุณสมบัติที่ไม่ใช่โลหะเพิ่มขึ้น เห็นได้อย่างชัดเจนในตัวอย่างของคาบที่ 2: มันเริ่มต้นด้วยโซเดียมของโลหะอัลคาไล จากนั้นเป็นแมกนีเซียมของโลหะอัลคาไลน์เอิร์ท หลังจากนั้นเป็นอะลูมิเนียมที่เป็นองค์ประกอบแอมโฟเทอริก จากนั้นจึงเปลี่ยนเป็นซิลิกอนที่ไม่ใช่โลหะ ฟอสฟอรัส กำมะถัน และคาบสิ้นสุดด้วยสารที่เป็นก๊าซ - คลอรีนและอาร์กอน ในช่วงต่อไปจะสังเกตเห็นการพึ่งพาอาศัยกันที่คล้ายกัน
จากบนลงล่างจะมีการสังเกตรูปแบบ - คุณสมบัติของโลหะได้รับการปรับปรุงและรูปแบบที่ไม่ใช่โลหะจะลดลง ตัวอย่างเช่น ซีเซียมมีฤทธิ์มากกว่าโซเดียมมาก
ชื่อขององค์ประกอบทางเคมีทั้งหมดมาจากภาษาละติน นี่เป็นสิ่งจำเป็นก่อนอื่นเพื่อให้นักวิทยาศาสตร์จากประเทศต่างๆสามารถเข้าใจซึ่งกันและกันได้
สัญญาณทางเคมีของธาตุ
องค์ประกอบมักจะแสดงด้วยเครื่องหมายทางเคมี (สัญลักษณ์) ตามคำแนะนำของนักเคมีชาวสวีเดน Berzelius (1813) องค์ประกอบทางเคมีจะแสดงด้วยชื่อย่อหรืออักษรย่อและหนึ่งในตัวอักษรที่ตามมาของชื่อละตินขององค์ประกอบนี้ ตัวอักษรตัวแรกเป็นตัวพิมพ์ใหญ่เสมอตัวที่สองเป็นตัวพิมพ์เล็ก ตัวอย่างเช่นไฮโดรเจน (ไฮโดรเจน) แสดงด้วยตัวอักษร H, ออกซิเจน (Oxygenium) ด้วยตัวอักษร O, กำมะถัน (กำมะถัน) ด้วยตัวอักษร S; ปรอท (Hydrargyrum) - ด้วยตัวอักษร Hg, อลูมิเนียม (อลูมิเนียม) - Al, เหล็ก (Ferrum) - Fe เป็นต้น

ข้าว. 1. ตารางองค์ประกอบทางเคมีที่มีชื่อเป็นภาษาละตินและรัสเซีย
ชื่อองค์ประกอบทางเคมีของรัสเซียมักเป็นชื่อละตินที่มีส่วนท้ายที่ดัดแปลง แต่ก็มีองค์ประกอบหลายอย่างที่การออกเสียงแตกต่างจากภาษาละติน คำเหล่านี้เป็นคำภาษารัสเซียพื้นเมือง (เช่น เหล็ก) หรือคำที่เป็นคำแปล (เช่น ออกซิเจน)
ศัพท์เคมี
ศัพท์เคมี - ชื่อสารเคมีที่ถูกต้อง ศัพท์ภาษาละติน nomenclatura แปลว่า "รายชื่อ, ชื่อเรื่อง"
ในระยะเริ่มต้นของการพัฒนาเคมี ชื่อสุ่ม (ชื่อไม่สำคัญ) โดยพลการให้กับสาร ของเหลวระเหยเรียกว่าแอลกอฮอล์รวมถึง "ไฮโดรคลอริกแอลกอฮอล์" - สารละลายกรดไฮโดรคลอริก "ซิลิทรีแอลกอฮอล์" - กรดไนตริก "แอลกอฮอล์แอมโมเนีย" - สารละลายแอมโมเนียในน้ำ ของเหลวและของแข็งที่เป็นน้ำมันเรียกว่าน้ำมัน ตัวอย่างเช่น กรดซัลฟิวริกเข้มข้นเรียกว่า "น้ำมันกรดกำมะถัน" คลอไรด์สารหนู - "น้ำมันสารหนู"
บางครั้งสารได้รับการตั้งชื่อตามผู้ค้นพบเช่น "เกลือของ Glauber" Na 2 SO 4 * 10H 2 O ซึ่งค้นพบโดยนักเคมีชาวเยอรมัน I. R. Glauber ในศตวรรษที่ 17

ข้าว. 2. ภาพเหมือนของ I. R. Glauber
ชื่อโบราณสามารถบ่งบอกถึงรสชาติของสาร สี กลิ่น ลักษณะ และผลทางการแพทย์ สารหนึ่งบางครั้งมีหลายชื่อ
ในตอนท้ายของศตวรรษที่ 18 นักเคมีรู้จักสารประกอบไม่เกิน 150-200 ชนิด
ชื่อวิทยาศาสตร์ระบบแรกในวิชาเคมีได้รับการพัฒนาในปี พ.ศ. 2330 โดยคณะกรรมการนักเคมีที่นำโดย A. Lavoisier ระบบการตั้งชื่อทางเคมีของ Lavoisier เป็นพื้นฐานสำหรับการสร้างระบบการตั้งชื่อทางเคมีระดับชาติ เพื่อให้นักเคมีจากประเทศต่างๆ เข้าใจกัน ระบบการตั้งชื่อจะต้องเป็นหนึ่งเดียว ปัจจุบัน การสร้างสูตรเคมีและชื่อของสารอนินทรีย์อยู่ภายใต้ระบบกฎการตั้งชื่อที่สร้างขึ้นโดยคณะกรรมการของ International Union of Pure and Applied Chemistry (IUPAC) สารแต่ละชนิดถูกแทนด้วยสูตร ตามชื่อที่เป็นระบบของสารประกอบถูกสร้างขึ้น

ข้าว. 3. ก. ลาวัวซิเยร์.
เราได้เรียนรู้อะไรบ้าง?
องค์ประกอบทางเคมีทั้งหมดมีรากภาษาละติน โดยทั่วไปยอมรับชื่อละตินขององค์ประกอบทางเคมี ในภาษารัสเซีย พวกมันถูกถ่ายโอนโดยใช้การติดตามหรือการแปล อย่างไรก็ตาม คำบางคำมีความหมายดั้งเดิมของรัสเซีย เช่น ทองแดงหรือเหล็ก การตั้งชื่อทางเคมีขึ้นอยู่กับสารเคมีทั้งหมดที่ประกอบด้วยอะตอมและโมเลกุล เป็นครั้งแรกที่ระบบชื่อวิทยาศาสตร์ได้รับการพัฒนาโดย A. Lavoisier
แบบทดสอบหัวข้อ
รายงานการประเมินผล
คะแนนเฉลี่ย: 4.2. คะแนนที่ได้รับทั้งหมด: 768
หากตารางธาตุดูเหมือนยากสำหรับคุณที่จะเข้าใจ แสดงว่าคุณไม่ได้อยู่คนเดียว! แม้ว่าจะเข้าใจหลักการได้ยาก แต่การเรียนรู้ที่จะใช้งานจะช่วยในการศึกษาวิทยาศาสตร์ธรรมชาติ ในการเริ่มต้น ให้ศึกษาโครงสร้างของตารางและข้อมูลที่สามารถเรียนรู้ได้จากตารางเกี่ยวกับองค์ประกอบทางเคมีแต่ละชนิด จากนั้นคุณสามารถเริ่มสำรวจคุณสมบัติของแต่ละองค์ประกอบได้ และสุดท้าย โดยใช้ตารางธาตุ คุณสามารถกำหนดจำนวนนิวตรอนในอะตอมของธาตุเคมีชนิดใดชนิดหนึ่งได้
ขั้นตอน
ส่วนที่ 1
โครงสร้างตาราง-
อย่างที่คุณเห็น แต่ละองค์ประกอบถัดไปมีหนึ่งโปรตอนมากกว่าองค์ประกอบที่อยู่ข้างหน้าสิ่งนี้ชัดเจนเมื่อคุณดูเลขอะตอม เลขอะตอมจะเพิ่มขึ้นหนึ่งเมื่อคุณเลื่อนจากซ้ายไปขวา เนื่องจากองค์ประกอบถูกจัดเรียงเป็นกลุ่ม เซลล์ตารางบางเซลล์จึงยังคงว่างเปล่า
- ตัวอย่างเช่น แถวแรกของตารางมีไฮโดรเจนซึ่งมีเลขอะตอม 1 และฮีเลียมซึ่งมีเลขอะตอม 2 อย่างไรก็ตาม พวกมันอยู่คนละด้านเพราะอยู่คนละกลุ่ม
-
เรียนรู้เกี่ยวกับกลุ่มที่มีองค์ประกอบที่มีคุณสมบัติทางกายภาพและทางเคมีที่คล้ายคลึงกันองค์ประกอบของแต่ละกลุ่มจะอยู่ในคอลัมน์แนวตั้งที่สอดคล้องกัน ตามกฎแล้วจะมีการระบุด้วยสีเดียวกันซึ่งช่วยในการระบุองค์ประกอบที่มีคุณสมบัติทางกายภาพและทางเคมีที่คล้ายคลึงกันและทำนายพฤติกรรมของพวกเขา องค์ประกอบทั้งหมดของกลุ่มใดกลุ่มหนึ่งมีจำนวนอิเล็กตรอนเท่ากันในเปลือกนอก
- ไฮโดรเจนสามารถเกิดขึ้นได้ทั้งกับกลุ่มของโลหะอัลคาไลและกลุ่มของฮาโลเจน ในบางตารางจะระบุไว้ในทั้งสองกลุ่ม
- ในกรณีส่วนใหญ่ กลุ่มต่างๆ จะมีหมายเลขตั้งแต่ 1 ถึง 18 และตัวเลขจะอยู่ที่ด้านบนหรือด้านล่างของตาราง ตัวเลขสามารถระบุเป็นตัวเลขโรมัน (เช่น IA) หรืออารบิก (เช่น 1A หรือ 1)
- เมื่อย้ายไปตามคอลัมน์จากบนลงล่าง พวกเขาบอกว่าคุณกำลัง "กำลังดูกลุ่ม"
-
ค้นหาว่าเหตุใดจึงมีเซลล์ว่างในตารางองค์ประกอบไม่เพียง แต่เรียงลำดับตามเลขอะตอมเท่านั้น แต่ยังเรียงลำดับตามกลุ่มด้วย (องค์ประกอบของกลุ่มเดียวกันมีคุณสมบัติทางกายภาพและเคมีที่คล้ายคลึงกัน) ซึ่งจะทำให้เข้าใจได้ง่ายขึ้นว่าองค์ประกอบทำงานอย่างไร อย่างไรก็ตาม เมื่อเลขอะตอมเพิ่มขึ้น จะไม่พบองค์ประกอบที่อยู่ในกลุ่มที่สอดคล้องกันเสมอไป ดังนั้นจึงมีเซลล์ว่างในตาราง
- ตัวอย่างเช่น 3 แถวแรกมีเซลล์ว่าง เนื่องจากโลหะทรานซิชันพบได้เฉพาะจากเลขอะตอม 21 เท่านั้น
- องค์ประกอบที่มีเลขอะตอมตั้งแต่ 57 ถึง 102 เป็นของธาตุหายาก และมักจะอยู่ในกลุ่มย่อยที่แยกต่างหากที่มุมล่างขวาของตาราง
-
แต่ละแถวของตารางแสดงถึงช่วงเวลาองค์ประกอบทั้งหมดในช่วงเวลาเดียวกันมีจำนวนออร์บิทัลของอะตอมเท่ากันซึ่งอิเล็กตรอนอยู่ในอะตอม จำนวนของออร์บิทัลสอดคล้องกับจำนวนคาบ ตารางประกอบด้วย 7 แถว นั่นคือ 7 จุด
- ตัวอย่างเช่น อะตอมของธาตุในคาบแรกมีหนึ่งออร์บิทัล และอะตอมของธาตุในคาบที่เจ็ดมี 7 ออร์บิทัล
- ตามกฎแล้ว ช่วงเวลาจะถูกระบุด้วยตัวเลขตั้งแต่ 1 ถึง 7 ทางด้านซ้ายของตาราง
- เมื่อคุณเคลื่อนไปตามเส้นจากซ้ายไปขวา จะมีการกล่าวกันว่าคุณกำลัง "สแกนผ่านจุด"
-
เรียนรู้ที่จะแยกแยะระหว่างโลหะ เมทัลลอยด์ และอโลหะคุณจะเข้าใจคุณสมบัติขององค์ประกอบได้ดีขึ้นถ้าคุณสามารถระบุได้ว่าเป็นของประเภทใด เพื่อความสะดวก ในตารางส่วนใหญ่ โลหะ เมทัลลอยด์ และอโลหะจะแสดงด้วยสีต่างๆ โลหะอยู่ทางซ้าย และอโลหะอยู่ทางด้านขวาของโต๊ะ Metalloids ตั้งอยู่ระหว่างพวกเขา
ตอนที่ 2
การกำหนดองค์ประกอบ-
แต่ละองค์ประกอบถูกกำหนดด้วยตัวอักษรละตินหนึ่งหรือสองตัวตามกฎแล้ว สัญลักษณ์องค์ประกอบจะแสดงเป็นตัวอักษรขนาดใหญ่ตรงกลางเซลล์ที่เกี่ยวข้อง สัญลักษณ์คือชื่อย่อสำหรับองค์ประกอบที่เหมือนกันในภาษาส่วนใหญ่ เมื่อทำการทดลองและทำงานกับสมการเคมี มักใช้สัญลักษณ์ของธาตุ ดังนั้นจึงมีประโยชน์ที่จะจำไว้
- โดยทั่วไปแล้ว สัญลักษณ์องค์ประกอบจะเป็นชวเลขสำหรับชื่อภาษาละติน แม้ว่าสำหรับบางองค์ประกอบ โดยเฉพาะองค์ประกอบที่ค้นพบเมื่อเร็วๆ นี้ พวกมันได้มาจากชื่อสามัญ ตัวอย่างเช่น ฮีเลียมแสดงด้วยสัญลักษณ์ He ซึ่งใกล้เคียงกับชื่อสามัญในภาษาส่วนใหญ่ ในเวลาเดียวกัน ธาตุเหล็กถูกกำหนดให้เป็นเฟ ซึ่งเป็นตัวย่อของชื่อละติน
-
ให้ความสนใจกับชื่อเต็มขององค์ประกอบ หากระบุไว้ในตาราง"ชื่อ" ขององค์ประกอบนี้ใช้ในข้อความปกติ ตัวอย่างเช่น "ฮีเลียม" และ "คาร์บอน" เป็นชื่อของธาตุ โดยปกติ แม้ว่าจะไม่เสมอไป ชื่อเต็มขององค์ประกอบจะได้รับภายใต้สัญลักษณ์ทางเคมีของธาตุ
- บางครั้งชื่อขององค์ประกอบจะไม่ถูกระบุไว้ในตารางและให้เฉพาะสัญลักษณ์ทางเคมีเท่านั้น
-
หาเลขอะตอม.โดยปกติเลขอะตอมของธาตุจะอยู่ที่ด้านบนสุดของเซลล์ที่เกี่ยวข้อง ตรงกลางหรือที่มุม นอกจากนี้ยังสามารถปรากฏใต้สัญลักษณ์หรือชื่อองค์ประกอบ ธาตุมีเลขอะตอมตั้งแต่ 1 ถึง 118
- เลขอะตอมเป็นจำนวนเต็มเสมอ
-
จำไว้ว่าเลขอะตอมสอดคล้องกับจำนวนโปรตอนในอะตอมอะตอมทั้งหมดของธาตุมีจำนวนโปรตอนเท่ากัน จำนวนโปรตอนในอะตอมของธาตุนั้นไม่เหมือนกับอิเล็กตรอน มิฉะนั้นองค์ประกอบทางเคมีอื่นจะกลายเป็น!
- เลขอะตอมของธาตุยังสามารถใช้เพื่อกำหนดจำนวนอิเล็กตรอนและนิวตรอนในอะตอม
-
โดยปกติจำนวนอิเล็กตรอนจะเท่ากับจำนวนโปรตอนข้อยกเว้นคือกรณีที่อะตอมแตกตัวเป็นไอออน โปรตอนมีประจุบวกและอิเล็กตรอนมีประจุลบ เนื่องจากอะตอมมักจะเป็นกลาง จึงมีจำนวนอิเล็กตรอนและโปรตอนเท่ากัน อย่างไรก็ตาม อะตอมสามารถรับหรือสูญเสียอิเล็กตรอนได้ ซึ่งในกรณีนี้ อะตอมจะกลายเป็นไอออนไนซ์
- ไอออนมีประจุไฟฟ้า หากมีโปรตอนในไอออนมากกว่า แสดงว่ามีประจุบวก ซึ่งในกรณีนี้ จะมีการใส่เครื่องหมายบวกหลังสัญลักษณ์ธาตุ ถ้าไอออนมีอิเลคตรอนมากกว่า แสดงว่ามีประจุลบ ซึ่งแสดงด้วยเครื่องหมายลบ
- เครื่องหมายบวกและลบจะถูกละไว้หากอะตอมไม่ใช่ไอออน
-
ตารางธาตุหรือตารางธาตุขององค์ประกอบทางเคมี เริ่มต้นที่ด้านซ้ายบนและสิ้นสุดที่ส่วนท้ายของบรรทัดสุดท้ายของตาราง (ล่างขวา) องค์ประกอบในตารางถูกจัดเรียงจากซ้ายไปขวาโดยเรียงลำดับจากน้อยไปมากของเลขอะตอม เลขอะตอมจะบอกจำนวนโปรตอนในอะตอมหนึ่งอะตอม นอกจากนี้ เมื่อเลขอะตอมเพิ่มขึ้น มวลอะตอมก็เช่นกัน ดังนั้นโดยตำแหน่งของธาตุในตารางธาตุ คุณสามารถกำหนดมวลอะตอมของมันได้








