ความยาวพันธะและรัศมีที่มีประสิทธิภาพของอะตอมและไอออน รัศมีอะตอม: มันคืออะไรและจะตรวจสอบได้อย่างไร ในการเชื่อมต่อกับรัศมีอะตอม
การแบ่งพันธะเคมีออกเป็นประเภทมีเงื่อนไข
สำหรับพันธะโลหะเนื่องจากการดึงดูดของอิเล็กตรอนและไอออนของโลหะ สัญญาณบางอย่างของพันธะโควาเลนต์เป็นลักษณะเฉพาะ หากเราคำนึงถึงการทับซ้อนกันของออร์บิทัลของอะตอมของอะตอม ในการก่อตัวของพันธะไฮโดรเจน นอกเหนือจากปฏิกิริยาของไฟฟ้าสถิตแล้ว ธรรมชาติของตัวรับและตัวรับของปฏิกิริยายังมีบทบาทสำคัญ
นอกจากนี้ยังเป็นไปไม่ได้ที่จะวาดขอบเขตที่คมชัดระหว่างพันธะขั้วไอออนิกและโควาเลนต์ เป็นไปไม่ได้ที่จะระบุพันธะระหว่างโลหะและอโลหะกับประเภทไอออนิก เป็นเรื่องปกติที่จะต้องพิจารณาพันธะไอออนิกระหว่างอะตอมซึ่งความแตกต่างของอิเล็กโตรเนกาติวีตี้มากกว่าหรือเท่ากับ 2 (ในระดับ Pauling) ตัวอย่างเช่น ในโซเดียมออกไซด์ พันธะ Na 2 O (3.44 - 0.93 = 2.51) เป็นพันธะไอออนิก และในแมกนีเซียมโบรไมด์ MgBr พันธะโควาเลนต์ (2.96 - 1.31 = 1.65)
ในสารจริง พันธะเคมีทุกประเภทไม่พบในรูปแบบบริสุทธิ์ สำหรับสารประกอบส่วนใหญ่ ชนิดของพันธะจะอยู่ตรงกลาง สิ่งนี้เป็นไปได้ เนื่องจากธรรมชาติของพันธะเคมีเหมือนกัน - เป็นปฏิกิริยาทางไฟฟ้าสถิตของอิเล็กตรอนและนิวเคลียสภายในและระหว่างอะตอมที่อยู่ใกล้กันในระยะไกล เมื่อเกิดการทับซ้อนกันของเปลือกอิเล็กตรอนอย่างมีประสิทธิภาพ
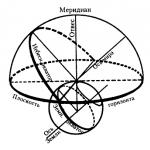
ดังนั้น การเปลี่ยนแปลงอย่างต่อเนื่องระหว่างกรณีการจำกัดทั้งหมดจึงเป็นไปได้: พันธะไอออนิก โควาเลนต์ โลหะ และพันธะที่เหลือ การมองเห็นการเปลี่ยนแปลงสามารถแสดงเป็นจัตุรมุขที่จุดยอดซึ่งมีตัวแทนที่รุนแรงตามขอบมีการเปลี่ยนแปลงระหว่างสองประเภทและบนใบหน้าและภายในปริมาตรของจัตุรมุขมีพันธบัตรประเภทผสมที่ซับซ้อน
รัศมีที่มีประสิทธิภาพของอะตอมและไอออน
ภายใต้ รัศมีที่มีประสิทธิภาพของอะตอมและไอออน เข้าใจรัศมีของทรงกลมของอะตอมหรือไอออน นั่นคือ ระยะทางต่ำสุดที่ศูนย์กลางของทรงกลมของอะตอมหรือไอออนสามารถเข้าใกล้พื้นผิวของอะตอมที่อยู่ใกล้เคียงได้
ในการกำหนดรัศมีที่มีประสิทธิภาพของอะตอมหรือไอออน โครงสร้างผลึกจะแสดงเป็นลูกบอลต่อเนื่องกัน ระยะห่างระหว่างซึ่งเท่ากับผลรวมของรัศมี ขึ้นอยู่กับชนิดของพันธะเคมีระหว่างหน่วยโครงสร้างของผลึก ประกอบด้วย: รัศมีโลหะ รัศมีไอออนิก รัศมีโควาเลนต์ และรัศมีแวนเดอร์วาลส์
รัศมีโลหะ
กำหนดระยะห่างระหว่างอะตอมข้างเคียงเพียงครึ่งเดียว ซึ่งได้มาจากการวิเคราะห์การเลี้ยวเบนของรังสีเอกซ์:

รัศมีไอออน
ในการคำนวณรัศมีของไอออน สันนิษฐานว่าด้วยขนาดของไพเพอร์และแอนไอออนที่ต่างกันมากเพียงพอ แอนไอออนขนาดใหญ่จะสัมผัสกัน และไอออนบวกที่มีขนาดเล็กกว่าจะอยู่ในช่องว่างระหว่างแอนไอออน จากนั้นจึงรัศมีของประจุลบ จะ:
รัศมีของไอออนบวกคือ:

รัศมีโควาเลนต์
รัศมีโควาเลนต์ถูกกำหนดให้เป็นครึ่งหนึ่งของระยะห่างระหว่างอะตอม (ความยาวพันธะ): .
นอกจากนี้ เมื่อคำนวณรัศมีโควาเลนต์ จะพิจารณาความสามารถขององค์ประกอบบางอย่างในการสร้างพันธะหลายตัว ซึ่งลดระยะห่างระหว่างอะตอมและประเภทของการผสมพันธุ์ของอะตอมกลางด้วย

รัศมี Van der Waals คำนวณสำหรับอะตอมที่เชื่อมต่อกันโดยแรงระหว่างโมเลกุลเท่านั้น คำนวณเป็นครึ่งหนึ่งของระยะห่างระหว่างจุดศูนย์กลางของอะตอม: .

เนื่องจากวิธีการคำนวณรัศมีอะตอมและไอออนิกแตกต่างกัน จึงมีตารางรัศมีจำนวนมาก
ผลึกไอออนิก
ความสัมพันธ์ของไอออนบวกและแอนไอออนในผลึกเกิดขึ้นเนื่องจากการดึงดูดของประจุไฟฟ้าคูลอมบ์ ในโมเลกุล ประจุมีปฏิสัมพันธ์กับแรง ค่า Rคือระยะห่างระหว่างสองไอออน ถ้าระยะนี้อยู่ไกลไม่สิ้นสุด แรงจะเป็นศูนย์ ที่ระยะทางจำกัด แรงปฏิสัมพันธ์ของไอออนที่มีประจุตรงข้ามสองตัวจะเป็นลบ ซึ่งสอดคล้องกับแรงดึงดูด ไอออนมักจะเข้าใกล้ระยะทางต่ำสุดที่อนุญาต ซึ่งสอดคล้องกับสถานะการยึดเกาะที่มั่นคง แรงปฏิกิริยาของไอออนที่มีประจุเท่ากันสองตัวนั้นเป็นค่าบวก ซึ่งสอดคล้องกับแรงผลัก ไอออนมักจะกระเจิงและไม่ก่อให้เกิดการเชื่อมต่อที่เสถียรในทุกระยะ ดังนั้นพลังงานการก่อตัวของผลึกจะต้องเป็นลบ เงื่อนไขนี้เกิดขึ้นได้ในระหว่างการก่อตัวของผลึกไอออนิก
ไม่มีโมเลกุลในผลึกไอออนิก ดังนั้นจึงไม่มีขอบเขตระหว่างหน่วยโครงสร้าง ไอออนสามารถคิดได้ว่าเป็นลูกบอลที่มีประจุซึ่งมีการกระจายสนามแรงอย่างสม่ำเสมอในทุกทิศทางในอวกาศ ดังนั้นไอออนแต่ละตัวจึงสามารถดึงดูดไอออนของเครื่องหมายตรงข้ามมาที่ตัวมันเองในทิศทางใดก็ได้ ดังนั้นพันธะไอออนิก ไม่มีทิศทาง
ปฏิสัมพันธ์ของสองไอออนที่มีเครื่องหมายตรงข้ามไม่สามารถนำไปสู่การชดเชยร่วมกันของสนามแรงได้ ด้วยเหตุนี้พวกเขาจึงรักษาความสามารถในการดึงดูดไอออนของเครื่องหมายตรงข้ามในทิศทางอื่น ดังนั้นพันธะไอออนิก ไม่อิ่มตัว
ไพเพอร์มีแนวโน้มที่จะล้อมรอบตัวเองด้วยแอนไอออนให้มากที่สุดเท่าที่จะเป็นไปได้เพื่อให้คูลอมบ์ขับไล่ไอออนที่มีเครื่องหมายเดียวกันออกจากกันได้รับการชดเชยด้วยการดึงดูดคูลอมบ์ร่วมกันของไพเพอร์และแอนไอออน ดังนั้นโครงสร้างที่มีพันธะเคมีประเภทไอออนิกจึงมีลักษณะเฉพาะด้วยจำนวนการประสานงานสูงและการบรรจุทรงกลมที่หนาแน่นที่สุด ความสมมาตรของผลึกไอออนิกมักจะสูง
สารผลึกที่มีพันธะเคมีประเภทไอออนิกมีลักษณะเป็นฉนวน, ความเปราะบาง, ค่าเฉลี่ยของความแข็งและความหนาแน่น, การนำความร้อนและไฟฟ้าต่ำ
อะตอมไอออน; มีความหมายรัศมีของทรงกลมแทนอะตอมหรือไอออนเหล่านี้ในโมเลกุลหรือผลึก รัศมีอะตอมทำให้สามารถประมาณระยะห่างระหว่างนิวเคลียร์ (ระหว่างอะตอม) ในโมเลกุลและคริสตัลได้
ความหนาแน่นของอิเล็กตรอนของอะตอมที่ถูกแยกเดี่ยวจะลดลงอย่างรวดเร็วเมื่อระยะห่างจากนิวเคลียสเพิ่มขึ้น เพื่อให้รัศมีของอะตอมถูกกำหนดเป็นรัศมีของทรงกลมซึ่งส่วนหลัก (เช่น 99%) ของความหนาแน่นของอิเล็กตรอนคือ เข้มข้น อย่างไรก็ตาม ในการประมาณระยะทางระหว่างนิวเคลียร์ กลับกลายเป็นว่าสะดวกกว่าในการตีความรัศมีอะตอมในวิธีที่ต่างออกไป สิ่งนี้นำไปสู่คำจำกัดความและระบบต่าง ๆ ของรัศมีอะตอม
รัศมีโควาเลนต์ของอะตอม X ถูกกำหนดเป็นครึ่งหนึ่งของความยาวพันธะเคมี XX อย่างง่าย ดังนั้นสำหรับฮาโลเจน รัศมีโควาเลนต์คำนวณจากระยะห่างระหว่างนิวเคลียร์ที่สมดุลในโมเลกุล X 2 สำหรับกำมะถันและซีลีเนียม - ในโมเลกุล S 8 และ Se 8 สำหรับคาร์บอน - ในผลึกเพชร ข้อยกเว้นคืออะตอมไฮโดรเจน ซึ่งรัศมีอะตอมของโควาเลนต์จะอยู่ที่ 30:00 น. ในขณะที่ระยะทางระหว่างนิวเคลียร์ครึ่งหนึ่งในโมเลกุล H 2 คือ 37 น. สำหรับสารประกอบที่มีพันธะโควาเลนต์ ตามกฎแล้ว หลักการบวกจะเป็นไปตามนั้น (ความยาวของพันธะ X–Y เท่ากับผลรวมของรัศมีอะตอมของอะตอม X และ Y โดยประมาณ) ซึ่งทำให้สามารถทำนายความยาวพันธะได้ ในโมเลกุล polyatomic
รัศมีไอออนิกถูกกำหนดให้เป็นค่าที่ผลรวมของไอออนคู่หนึ่ง (เช่น X + และ Y -) เท่ากับระยะทางระหว่างนิวเคลียร์ที่สั้นที่สุดในผลึกไอออนิกที่สอดคล้องกัน รัศมีไอออนิกมีหลายระบบ ระบบต่างกันในค่าตัวเลขสำหรับไอออนแต่ละตัว ขึ้นอยู่กับรัศมีและไอออนที่ใช้เป็นพื้นฐานในการคำนวณรัศมีของไอออนอื่นๆ ตัวอย่างเช่น ตาม Pauling นี่คือรัศมีของ O 2- ion ซึ่งมีค่าเท่ากับ 140 pm ตามแชนนอน - รัศมีของไอออนเดียวกันซึ่งเท่ากับ 121 น. แม้จะมีความแตกต่างเหล่านี้ ระบบต่างๆ ในการคำนวณระยะทางระหว่างนิวเคลียร์ในผลึกไอออนิกก็ให้ผลลัพธ์ที่ใกล้เคียงกันโดยประมาณ
รัศมีโลหะถูกกำหนดให้เป็นระยะห่างที่สั้นที่สุดเพียงครึ่งเดียวระหว่างอะตอมในโครงผลึกของโลหะ สำหรับโครงสร้างโลหะที่แตกต่างกันในประเภทของการบรรจุ รัศมีเหล่านี้จะแตกต่างกัน ความใกล้ชิดของค่าของรัศมีอะตอมของโลหะต่างๆ มักจะทำหน้าที่เป็นตัวบ่งชี้ถึงความเป็นไปได้ของการก่อตัวของสารละลายที่เป็นของแข็งโดยโลหะเหล่านี้ การเติมแต่งของรัศมีทำให้สามารถทำนายพารามิเตอร์ของโครงผลึกของสารประกอบระหว่างโลหะได้
รัศมี Van der Waals ถูกกำหนดให้เป็นปริมาณที่มีผลรวมเท่ากับระยะทางที่อะตอมสองอะตอมที่ไม่เกี่ยวข้องทางเคมีของโมเลกุลที่แตกต่างกันหรือกลุ่มอะตอมที่แตกต่างกันของโมเลกุลเดียวกันสามารถเข้าถึงได้ โดยเฉลี่ยแล้ว รัศมี van der Waals มีขนาดใหญ่กว่ารัศมีโควาเลนต์ประมาณ 80 น. รัศมี Van der Waals ใช้ในการตีความและทำนายความเสถียรของโครงสร้างโมเลกุลและการจัดลำดับโครงสร้างของโมเลกุลในผลึก
Lit.: Housecroft K. , Constable E. หลักสูตรเคมีทั่วไปสมัยใหม่ ม., 2545 ต. 1
รัศมีอะตอมที่มีประสิทธิภาพ - ดู รัศมีอะตอม
พจนานุกรมธรณีวิทยา: ใน 2 เล่ม - ม.: เนดรา. แก้ไขโดย K.N. Paffengolts et al.. 1978 .
ดูว่า "EFFECTIVE ATOMIC RADIUS" ในพจนานุกรมอื่นๆ คืออะไร:
ค่าใน Å ที่แสดงลักษณะขนาดของอะตอม โดยปกติ แนวคิดนี้จะเข้าใจว่าเป็น RA ที่มีประสิทธิผล ซึ่งคำนวณเป็นครึ่งหนึ่งของระยะห่างระหว่างอะตอม (ระหว่างนิวเคลียร์) ในสารประกอบโฮโมอะตอมมิก กล่าวคือ ในโลหะและอโลหะ เพราะอยู่คนเดียวและ... สารานุกรมธรณีวิทยา
แพลตตินั่ม- (แพลตตินัม) โลหะแพลตตินั่ม คุณสมบัติทางเคมีและทางกายภาพของแพลตตินั่ม โลหะแพลตตินั่ม คุณสมบัติทางเคมีและฟิสิกส์ของแพลตตินั่ม การผลิตและการใช้แพลตตินั่ม เนื้อหา หมวดที่ 1 ที่มาของชื่อแพลตตินั่ม หมวด ๒ สถานการณ์ใน ... ... สารานุกรมของนักลงทุน
ลักษณะที่ทำให้สามารถประมาณระยะทางระหว่างอะตอม (ระหว่างนิวเคลียร์) ในโมเลกุลและผลึกได้ รัศมีอะตอมอยู่ที่ 0.1 นาโนเมตร ส่วนใหญ่จะพิจารณาจากข้อมูลการวิเคราะห์โครงสร้างเอ็กซ์เรย์ * * * อะตอม… … พจนานุกรมสารานุกรม
โลหะ- (Metal) นิยามโลหะ สมบัติทางกายภาพและเคมีของโลหะ นิยามโลหะ สมบัติทางกายภาพและเคมีของโลหะ การประยุกต์ใช้โลหะ สารบัญ เนื้อหา คำจำกัดความ ค้นหาในธรรมชาติ คุณสมบัติ คุณสมบัติลักษณะเฉพาะ ... ... สารานุกรมของนักลงทุน
94 Neptunium ← Plutonium → Americium Sm Pu ... Wikipedia
คำขอ "ลิเธียม" เปลี่ยนเส้นทางที่นี่ ดูความหมายอื่นๆ ด้วย บทความนี้เกี่ยวกับองค์ประกอบทางเคมี สำหรับการใช้งานทางการแพทย์ ดูที่ การเตรียมลิเธียม 3 ฮีเลียม ← ลิเธียม ... Wikipedia
55 ซีนอน ← ซีเซียม → แบเรียม ... Wikipedia
การตรวจสอบโครงสร้างในเวอร์จิเนียขึ้นอยู่กับการศึกษาการกระจายเชิงมุมของความเข้มกระเจิงของรังสีเอกซ์ (รวมถึงซินโครตรอน) อิเล็กตรอนหรือฟลักซ์นิวตรอน และรังสี Mössbauer g ที่ศึกษาในเวอร์จิเนีย ตอบกลับ แยกแยะ… สารานุกรมเคมี
รัศมีที่มีประสิทธิภาพของอะตอมหรือไอออนเป็นที่เข้าใจกันว่ารัศมีของทรงกลมของการกระทำของมัน และอะตอม (ไอออน) ถือเป็นลูกบอลที่ไม่สามารถบีบอัดได้ โดยใช้แบบจำลองดาวเคราะห์ของอะตอม มันถูกแสดงเป็นนิวเคลียสที่อิเล็กตรอนโคจรรอบวงโคจร ลำดับขององค์ประกอบในระบบธาตุของ Mendeleev สอดคล้องกับลำดับของการเติมเปลือกอิเล็กตรอน รัศมีที่มีประสิทธิภาพของไอออนขึ้นอยู่กับการครอบครองของเปลือกอิเล็กตรอน แต่ไม่เท่ากับรัศมีของวงโคจรด้านนอก ในการกำหนดรัศมีที่มีประสิทธิภาพ อะตอม (ไอออน) ในโครงสร้างผลึกจะแสดงเป็นลูกบอลแข็งที่สัมผัสกัน เพื่อให้ระยะห่างระหว่างจุดศูนย์กลางของพวกมันเท่ากับผลรวมของรัศมี รัศมีอะตอมและอิออนถูกกำหนดโดยการทดลองจากการวัดรังสีเอ็กซ์ของระยะทางระหว่างอะตอมและคำนวณทางทฤษฎีบนพื้นฐานของแนวคิดทางกลของควอนตัม
ขนาดของรัศมีไอออนิกเป็นไปตามกฎหมายต่อไปนี้:
1. ภายในแถวแนวตั้งหนึ่งแถวของระบบธาตุ รัศมีของไอออนที่มีประจุเท่ากันจะเพิ่มขึ้นตามจำนวนอะตอมที่เพิ่มขึ้น เนื่องจากจำนวนเปลือกอิเล็กตรอนเพิ่มขึ้น และด้วยเหตุนี้ขนาดของอะตอม
2. สำหรับธาตุเดียวกัน รัศมีไอออนิกจะเพิ่มขึ้นตามประจุลบที่เพิ่มขึ้นและลดลงตามประจุบวกที่เพิ่มขึ้น รัศมีของประจุลบมีขนาดใหญ่กว่ารัศมีของประจุบวก เนื่องจากประจุลบมีอิเล็กตรอนมากเกินไป ในขณะที่ประจุบวกมีข้อบกพร่อง ตัวอย่างเช่น สำหรับ Fe, Fe 2+, Fe 3+ รัศมีมีผลคือ 0.126, 0.080 และ 0.067 nm ตามลำดับ สำหรับ Si 4-, Si, Si 4+ รัศมีมีผลคือ 0.198, 0.118 และ 0.040 nm
3. ขนาดของอะตอมและไอออนเป็นไปตามคาบของระบบ Mendeleev ข้อยกเว้นคือองค์ประกอบตั้งแต่หมายเลข 57 (แลนทานัม) ถึงหมายเลข 71 (ลูทีเนียม) โดยที่รัศมีอะตอมไม่เพิ่มขึ้น แต่ลดลงอย่างสม่ำเสมอ (ที่เรียกว่าการหดตัวของแลนทาไนด์) และองค์ประกอบจากหมายเลข 89 (แอกทิเนียม) ขึ้นไป ( การหดตัวของแอคตินอยด์ที่เรียกว่า)
รัศมีอะตอมขององค์ประกอบทางเคมีขึ้นอยู่กับหมายเลขประสานงาน การเพิ่มจำนวนการประสานงานจะมาพร้อมกับการเพิ่มขึ้นของระยะทางระหว่างอะตอมเสมอ ในกรณีนี้ ค่าความต่างสัมพัทธ์ระหว่างค่าของรัศมีอะตอมที่สอดคล้องกับเลขโคออร์ดิเนชันที่ต่างกันสองตัวไม่ได้ขึ้นอยู่กับชนิดของพันธะเคมี (โดยมีเงื่อนไขว่าชนิดของพันธะในโครงสร้างที่เปรียบเทียบตัวเลขโคออร์ดิเนชันจะเหมือนกัน) การเปลี่ยนแปลงรัศมีอะตอมด้วยการเปลี่ยนแปลงจำนวนการประสานงานมีผลอย่างมากต่อขนาดของการเปลี่ยนแปลงเชิงปริมาตรระหว่างการแปลงแบบพหุมอร์ฟิค ตัวอย่างเช่น เมื่อเหล็กถูกทำให้เย็นลง การเปลี่ยนแปลงจากการดัดแปลงลูกบาศก์ที่มีใบหน้าเป็นศูนย์กลางเป็นการดัดแปลงลูกบาศก์ที่มีศูนย์กลางอยู่ที่ 906 ° C ควรมาพร้อมกับการเพิ่มปริมาตร 9% อันที่จริง ปริมาตรที่เพิ่มขึ้นคือ 0.8 %. นี่เป็นเพราะความจริงที่ว่าเนื่องจากการเปลี่ยนแปลงในหมายเลขประสานงานจาก 12 เป็น 8 รัศมีอะตอมของเหล็กลดลง 3% กล่าวคือ การเปลี่ยนแปลงรัศมีอะตอมระหว่างการแปลงแบบพหุมอร์ฟิคส่วนใหญ่ชดเชยการเปลี่ยนแปลงเชิงปริมาตรที่จะเกิดขึ้นหากรัศมีอะตอมไม่เปลี่ยนแปลงในกรณีนี้ รัศมีอะตอมของธาตุสามารถเปรียบเทียบได้กับเลขพิกัดเดียวกันเท่านั้น
รัศมีอะตอม (อิออน) ยังขึ้นอยู่กับชนิดของพันธะเคมี
ในผลึกที่มีพันธะโลหะ รัศมีอะตอมถูกกำหนดเป็นครึ่งหนึ่งของระยะห่างระหว่างอะตอมระหว่างอะตอมที่ใกล้ที่สุด ในกรณีของสารละลายที่เป็นของแข็ง รัศมีอะตอมของโลหะจะแปรผันอย่างซับซ้อน
ภายใต้รัศมีโควาเลนต์ของธาตุที่มีพันธะโควาเลนต์จะเข้าใจได้ว่าครึ่งหนึ่งของระยะห่างระหว่างอะตอมระหว่างอะตอมที่ใกล้ที่สุดซึ่งเชื่อมต่อกันด้วยพันธะโควาเลนต์เดี่ยว คุณลักษณะของรัศมีโควาเลนต์คือความคงตัวของพวกมันในโครงสร้างโควาเลนต์ที่ต่างกันซึ่งมีจำนวนโควาเลนต์เหมือนกัน ดังนั้น ระยะทางในพันธะ CC เดี่ยวในเพชรและไฮโดรคาร์บอนอิ่มตัวจะเท่ากันและเท่ากับ 0.154 นาโนเมตร
รัศมีไอออนในสารที่มีพันธะไอออนิกไม่สามารถกำหนดเป็นผลรวมของระยะห่างระหว่างไอออนที่ใกล้ที่สุดได้ครึ่งหนึ่ง ตามกฎแล้วขนาดของไพเพอร์และแอนไอออนแตกต่างกันอย่างมาก นอกจากนี้ ความสมมาตรของไอออนยังแตกต่างจากทรงกลมอีกด้วย มีหลายวิธีในการประมาณค่าของรัศมีไอออนิก ตามแนวทางเหล่านี้ รัศมีไอออนของธาตุจะถูกประมาณการ จากนั้นรัศมีไอออนของธาตุอื่นๆ จะถูกหาจากระยะทางระหว่างอะตอมที่กำหนดโดยการทดลอง
รัศมี Van der Waals กำหนดขนาดที่มีประสิทธิภาพของอะตอมของก๊าซมีตระกูล นอกจากนี้ รัศมีอะตอมของ Van der Waals ยังถือเป็นครึ่งหนึ่งของระยะห่างระหว่างนิวเคลียร์ระหว่างอะตอมที่เหมือนกันที่ใกล้ที่สุดซึ่งไม่ได้ถูกพันธะทางเคมี กล่าวคือ ที่อยู่ในโมเลกุลต่างๆ (เช่น ในผลึกโมเลกุล)
เมื่อใช้ค่ารัศมีอะตอม (อิออน) ในการคำนวณและการสร้าง ค่าควรนำมาจากตารางที่สร้างตามระบบเดียว
ลักษณะสำคัญของอะตอมคือขนาดของอะตอม นั่นคือรัศมีอะตอม ขนาดของอะตอมแต่ละอะตอมไม่ได้ถูกกำหนด เนื่องจากขอบเขตภายนอกของมันถูกเบลอเนื่องจากการมีอยู่ของอิเล็กตรอนที่จุดต่าง ๆ ในปริภูมินิวเคลียร์ ด้วยเหตุนี้จึงขึ้นอยู่กับชนิดของพันธะระหว่างอะตอม โลหะ โควาเลนต์ แวนเดอร์วาลส์ ไอออนิก และรัศมีอะตอมอื่นๆ
รัศมี "โลหะ" (ฉัน)พบโดยการหารครึ่งระยะทางระหว่างอะตอมที่สั้นที่สุดในโครงสร้างผลึกของสารธรรมดาที่มีจำนวนการประสานงานเท่ากับ 12 ที่ค่าอื่นของ c.h. การแก้ไขที่จำเป็นจะถูกนำมาพิจารณา
ค่านิยม รัศมีโควาเลนต์ (r cov)คำนวณเป็นครึ่งหนึ่งของความยาวของพันธะโฮโมอะตอม หากไม่สามารถกำหนดความยาวของพันธะโฮโมอะตอมมิกเดี่ยวได้ ค่า r cov ของอะตอมของธาตุ A ได้มาจากการลบรัศมีโควาเลนต์ของอะตอมของธาตุ B ออกจากความยาวของพันธะเฮเทอโรอะตอมมิก AB รัศมีโควาเลนต์ขึ้นอยู่กับขนาดของเปลือกอิเล็กตรอนชั้นในเป็นหลัก
รัศมีของอะตอมที่ไม่ผูกกับวาเลนซ์ - van der Waals รัศมี (r w)กำหนดขนาดอะตอมที่มีประสิทธิภาพเนื่องจากแรงผลักของระดับพลังงานที่เติม
ค่าพลังงานอิเล็กตรอนถูกกำหนดโดยกฎของสเลเตอร์ ทำให้สามารถประมาณค่าสัมพัทธ์ - ขนาดปรากฏของอะตอม - r cmp (รัศมีเชิงประจักษ์)
ความยาวของพันธะมีหน่วยเป็นอังสตรอม (1 Å = 0.1 นาโนเมตร = 100 น.)
| ธาตุ | ฉัน | r cov | rw | r cmp |
| ชม | 0.46 | 0.37 | 1.20 | 0.25 |
| เขา | 1.22 | 0.32 | 1.40 | - |
| หลี่ | 1.55 | 1.34 | 1.82 | 1.45 |
| เป็น | 1.13 | 0.90 | - | 1.05 |
| บี | 0.91 | 0.82 | - | 0.85 |
| ค | 0.77 | 0.77 | 1.70 | 0.70 |
| นู๋ | 0.71 | 0.75 | 1.55 | 0.65 |
| อู๋ | - | 0.73 | 1.52 | 0.60 |
| F | - | 0.71 | 1.47 | 0.50 |
| เน่ | 1.60 | 0.69 | 1.54 | - |
| นา | 1.89 | 1.54 | 2.27 | 1.80 |
| มก. | 1.60 | 1.30 | 1.73 | 1.50 |
| อัล | 1.43 | 1.18 | - | 1.25 |
| ซิ | 1.34 | 1.11 | 2.10 | 1.10 |
| พี | 1.30 | 1.06 | 1.80 | 1.00 |
| ส | - | 1.02 | 1.80 | 1.00 |
| Cl | - | 0.9 | 1.75 | 1.00 |
| อา | 1.92 | 0.97 | 1.88 | - |
| K | 2.36 | 1.96 | 2.75 | 2.20 |
| Ca | 1.97 | 1.74 | - | 1.80 |
| sc | 1.64 | 1.44 | - | 1.60 |
| Ti | 1.46 | 1.36 | - | 1.40 |
| วี | 1.34 | 1.25 | - | 1.35 |
| Cr | 1.27 | 1.27 | - | 1.40 |
| มิน | 1.30 | 1.39 | - | 1.40 |
| เฟ | 1.26 | 1.25 | - | 1.40 |
| co | 1.25 | 1.26 | - | 1.35 |
| นิ | 1.24 | 1.21 | 1.63 | 1.35 |
| Cu | 1.28 | 1.38 | 1.40 | 1.35 |
| สังกะสี | 1.39 | 1.31 | 1.39 | 1.35 |
| กา | 1.39 | 1.26 | 1.87 | 1.30 |
| เก | 1.39 | 1.22 | - | 1.25 |
| เนื่องจาก | 1.48 | 1.19 | 1.85 | 1.15 |
| เซ | 1.60 | 1.16 | 1.90 | 1.15 |
| Br | - | 1.14 | 1.85 | 1.15 |
| kr | 1.98 | 1.10 | 2.02 | - |
| Rb | 2.48 | 2.11 | - | 2.35 |
| ซีเนียร์ | 2.15 | 1.92 | - | 2.00 |
| Y | 1.81 | 1.62 | - | 1.80 |
| Zr | 1.60 | 1.48 | - | 1.55 |
| Nb | 1.45 | 1.37 | - | 1.45 |
| โม | 1.39 | 1.45 | - | 1.45 |
| Tc | 1.36 | 1.56 | - | 1.35 |
| รุ | 1.34 | 1.26 | - | 1.30 |
| Rh | 1.34 | 1.35 | - | 1.35 |
| Pd | 1.37 | 1.31 | 1.63 | 1.40 |
| Ag | 1.44 | 1.53 | 1.72 | 1.60 |
| ซีดี | 1.56 | 1.48 | 1.58 | 1.55 |
| ใน | 1.66 | 1.44 | 1.93 | 1.55 |
| sn | 1.58 | 1.41 | 2.17 | 1.45 |
| เต | 1.70 | 1.35 | 2.06 | 1.40 |
| ฉัน | - | 1.33 | 1.98 | 1.40 |
| เซ | 2.18 | 1.30 | 2.16 | - |
| Cs | 2.68 | 2.25 | - | 2.60 |
| บา | 2.21 | 1.98 | - | 2.15 |
| ลา | 1.87 | 1.69 | - | 1.95 |
| เซ | 1.83 | - | - | 1.85 |
| ปรือ | 1.82 | - | - | 1.85 |
| Nd | 1.82 | - | - | 1.85 |
| น | - | - | - | 1.85 |
| sm | 1.81 | - | - | 1.85 |
| สหภาพยุโรป | 2.02 | - | - | 1.80 |
| Gd | 1.79 | - | - | 1.80 |
| Tb | 1.77 | - | - | 1.75 |
| Dy | 1.77 | - | - | 1.75 |
| โฮ | 1.76 | - | - | 1.75 |
| เอ้อ | 1.75 | - | - | 1.75 |
| Tm | 1.74 | - | - | 1.75 |
| Yb | 1.93 | - | - | 1.75 |
| ลู่ | 1.74 | 1.60 | - | 1.75 |
| hf | 1.59 | 1.50 | - | 1.55 |
| ตาล | 1.46 | 1.38 | - | 1.45 |
| W | 1.40 | 1.46 | - | 1.35 |
| อีกครั้ง | 1.37 | 1.59 | - | 1.35 |
| Os | 1.35 | 1.28 | - | 1.30 |
| ไอร์ | 1.35 | 1.37 | - | 1.35 |
| ปตท | 1.38 | 1.28 | 1.75 | 1.35 |
| Au | 1.44 | 1.44 | 1.66 | 1.35 |
| hg | 1.60 | 1.49 | 1.55 | 1.50 |
| Tl | 1.71 | 1.48 | 1.96 | 1.90 |
| พีบี | 1.75 | 1.47 | 2.02 | 1.80 |
| บี | 1.82 | 1.46 | - | 1.60 |
| โป | - | - | - | 1.90 |
| ที่ | - | - | - | - |
| Rn | - | 1.45 | - | - |
| คุณพ่อ | 2.80 | - | - | - |
| รา | 2.35 | - | - | 2.15 |
| AC | 2.03 | - | - | 1.95 |
| ไทย | 180 | - | - | 1.80 |
| ปะ | 1.62 | - | - | 1.80 |
| ยู | 1.53 | - | 1.86 | 1.75 |
| Np | 1.50 | - | - | 1.75 |
| ผู่ | 1.62 | - | - | 1.75 |
| เป็น | - | - | - | 1.75 |
แนวโน้มทั่วไปของรัศมีอะตอมมีดังนี้ ในกลุ่ม รัศมีอะตอมจะเพิ่มขึ้น เนื่องจากจำนวนระดับพลังงานที่เพิ่มขึ้น ขนาดของออร์บิทัลของอะตอมที่มีค่าจำนวนมากของเลขควอนตัมหลักจะเพิ่มขึ้น สำหรับองค์ประกอบ d ซึ่งอะตอมของออร์บิทัลของระดับพลังงานก่อนหน้าถูกเติม แนวโน้มนี้ไม่มีลักษณะเฉพาะที่ชัดเจนระหว่างการเปลี่ยนจากองค์ประกอบของช่วงที่ห้าเป็นองค์ประกอบของช่วงที่หก
ในช่วงเวลาเล็กๆ รัศมีของอะตอมโดยทั่วไปจะลดลง เนื่องจากการเพิ่มขึ้นของประจุของนิวเคลียสระหว่างการเปลี่ยนผ่านไปยังองค์ประกอบถัดไปแต่ละองค์ประกอบทำให้เกิดแรงดึงดูดของอิเล็กตรอนภายนอกด้วยแรงที่เพิ่มขึ้น จำนวนระดับพลังงานในเวลาเดียวกันยังคงที่
การเปลี่ยนแปลงรัศมีอะตอมในช่วงเวลาสำหรับองค์ประกอบ d นั้นซับซ้อนกว่า
ค่าของรัศมีอะตอมค่อนข้างสัมพันธ์กันอย่างใกล้ชิดกับคุณลักษณะที่สำคัญของอะตอม เช่น พลังงานไอออไนเซชัน อะตอมสามารถสูญเสียอิเล็กตรอนได้ตั้งแต่หนึ่งตัวขึ้นไป กลายเป็นไอออนที่มีประจุบวก - ไอออนบวก ความสามารถนี้วัดได้จากพลังงานไอออไนเซชัน
รายชื่อวรรณกรรมที่ใช้แล้ว
- ป๊อปคอฟ วี.เอ., Puzakov S. A. เคมีทั่วไป: ตำราเรียน. - M.: GEOTAR-Media, 2010. - 976 p.: ISBN 978-5-9704-1570-2. [กับ. 27-28)
- Volkov, A.I. , Zharsky, I.M.หนังสืออ้างอิงทางเคมีขนาดใหญ่ / A.I. วอลคอฟ, ไอ.เอ็ม. ซาร์สกี้ - มินสค์: โรงเรียนสมัยใหม่ 2548 - 608 พร้อม ISBN 985-6751-04-7