Kas ir trombocītu agregācijas kavēšana? Zāles, kas ietekmē asinsvadu trombocītu hemostāzi Trombocītu agregāciju inhibē ca2 blokators
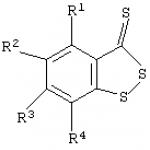
Izgudrojums attiecas uz fizioloģiju, farmakoloģiju un medicīnisko ķīmiju, jo īpaši uz uzlabotu metodi trombocītu agregācijas inhibēšanai. Šis mērķis tiek sasniegts ar aprakstīto uzlaboto metodi trombocītu agregācijas inhibēšanai, izmantojot sēru saturošus heterocikliskos savienojumus, kas sastāv no zināma benzo-1,2-ditiol-3-tiona (BDTT) vai tā atvasinājumu ar vispārīgo formulu izmantošanu kā sēru saturošu. heterocikliskie savienojumi
 kur R1-R4 = H vai C1-4alkilgrupa. Tehniskais rezultāts: ļauj efektīvāk inhibēt trombocītu agregāciju in vitro. Izgudrojums attiecas uz fizioloģiju, farmakoloģiju un medicīnisko ķīmiju, jo īpaši uz uzlabotu metodi trombocītu agregācijas inhibēšanai. Daudzu pētījumu rezultāti liecina, ka palielināta trombocītu agregācija galvenā loma daudzu sirds un asinsvadu slimību (piemēram, artēriju tromboze, miokarda infarkts, nestabila stenokardija) patoģenēzē. Savienojumi, kas var novērst trombocītu aktivāciju, ko var izraisīt endogēnie induktori (piemēram, adenozīna-5'-difosfāts /ADP), pašlaik tiek plaši izmantoti, lai efektīvi ietekmētu patoloģiskās izmaiņas hemostatiskajā sistēmā (B.A. Sidorenko, D. .V. Preobrazhensky klīniskā lietošana, lai novērstu trombocītu agregāciju, izmantojot sēru saturošus savienojumus trombocītu agregācija, 5,6,7-tetrahidrotienopiridīns (tiklopidīns) ar formulu I
kur R1-R4 = H vai C1-4alkilgrupa. Tehniskais rezultāts: ļauj efektīvāk inhibēt trombocītu agregāciju in vitro. Izgudrojums attiecas uz fizioloģiju, farmakoloģiju un medicīnisko ķīmiju, jo īpaši uz uzlabotu metodi trombocītu agregācijas inhibēšanai. Daudzu pētījumu rezultāti liecina, ka palielināta trombocītu agregācija galvenā loma daudzu sirds un asinsvadu slimību (piemēram, artēriju tromboze, miokarda infarkts, nestabila stenokardija) patoģenēzē. Savienojumi, kas var novērst trombocītu aktivāciju, ko var izraisīt endogēnie induktori (piemēram, adenozīna-5'-difosfāts /ADP), pašlaik tiek plaši izmantoti, lai efektīvi ietekmētu patoloģiskās izmaiņas hemostatiskajā sistēmā (B.A. Sidorenko, D. .V. Preobrazhensky klīniskā lietošana, lai novērstu trombocītu agregāciju, izmantojot sēru saturošus savienojumus trombocītu agregācija, 5,6,7-tetrahidrotienopiridīns (tiklopidīns) ar formulu I  ir trombocītu P 2T ADP receptoru antagonists (ASV patents Nr. 4963559, kl. 514-301, op. 1990. Ir arī pierādīts, ka kalcija kanālu blokators ir D-cis-3-acetoksi-2,3-). dihidro-5--2-(2-metoksifenil)-1,5-benzotiazepīna-4(5H)-ona hidrohlorīds (diltiazems) ar formulu II
ir trombocītu P 2T ADP receptoru antagonists (ASV patents Nr. 4963559, kl. 514-301, op. 1990. Ir arī pierādīts, ka kalcija kanālu blokators ir D-cis-3-acetoksi-2,3-). dihidro-5--2-(2-metoksifenil)-1,5-benzotiazepīna-4(5H)-ona hidrohlorīds (diltiazems) ar formulu II  piemīt antitrombotiska iedarbība (A.R.Dehpour, T.Samadian et al. “Diltiazema un verapamila ietekme uz ADP izraisītām trušu trombocītu formas izmaiņām un agregāciju” Gen. Pharmacol, 1995, v.26, Nr. 6, p.1295-1299 Iepriekš minētie savienojumi in vitro inhibēja trombocītu agregāciju, ko izraisa ADP koncentrācijā >300 μM benzo-1,2-ditiol-3-tion (BDTT) un tā atvasinājumi ar vispārīgo formulu III.
piemīt antitrombotiska iedarbība (A.R.Dehpour, T.Samadian et al. “Diltiazema un verapamila ietekme uz ADP izraisītām trušu trombocītu formas izmaiņām un agregāciju” Gen. Pharmacol, 1995, v.26, Nr. 6, p.1295-1299 Iepriekš minētie savienojumi in vitro inhibēja trombocītu agregāciju, ko izraisa ADP koncentrācijā >300 μM benzo-1,2-ditiol-3-tion (BDTT) un tā atvasinājumi ar vispārīgo formulu III.  kur R1R4 =H vai C1-6alkilgrupa, benzoilgrupa, (aizvietotā) aminosulfonilgrupa utt., kā organiskās sintēzes produkti (Eiropas patents Nr. 0043936, op. 1981. Šo savienojumu spēja novērst trombocītu agregācija nav pētīta .Aprakstītajam vistuvākā ir zināmā trombocītu agregācijas inhibēšanas metode, ievadot šīs šūnas saturošajā vidē sēru saturošus heterocikliskos savienojumus - aizvietoto 3,4-dihidro-1,2-ditiīnu-2. -oksīdi, jo īpaši šī metode izraisīja trombocītu agregācijas samazināšanos, izmantojot 3,4-dihidro-3-vinil-1,2-ditiīna-2-oksīdu ar formulu IV.
kur R1R4 =H vai C1-6alkilgrupa, benzoilgrupa, (aizvietotā) aminosulfonilgrupa utt., kā organiskās sintēzes produkti (Eiropas patents Nr. 0043936, op. 1981. Šo savienojumu spēja novērst trombocītu agregācija nav pētīta .Aprakstītajam vistuvākā ir zināmā trombocītu agregācijas inhibēšanas metode, ievadot šīs šūnas saturošajā vidē sēru saturošus heterocikliskos savienojumus - aizvietoto 3,4-dihidro-1,2-ditiīnu-2. -oksīdi, jo īpaši šī metode izraisīja trombocītu agregācijas samazināšanos, izmantojot 3,4-dihidro-3-vinil-1,2-ditiīna-2-oksīdu ar formulu IV.  salīdzinoši augstās koncentrācijās (piemēram, in vitro apstākļos konkrētam savienojumam, IC 50 = 100 μM) (Japānas patents 02204487, C 07 D 339/08, op. 1991, Chem. Abstr., 1991, v. 114, p. 6523s - prototips. Izgudrojuma mērķis ir izstrādāt efektīvāku trombocītu agregācijas inhibēšanas metodi. kas raksturīgs ar to, ka zināmi BDTT vai tā atvasinājumi ar augstāk minēto vispārīgo formulu, kur R1-R4 ir dotās vērtības. Vispārīgās formulas III savienojumi tika iegūti zināmā veidā - reaģējot ar atbilstošo neaizvietoto vai aizvietoto o-hloru. - vai o-brombenzilhlorīds vai bromīds ar sēru 50-200°C temperatūrā glikola monoalkilēterī sārmu metālu alkoksīda klātbūtnē Aprakstītais izgudrojums ir ilustrēts ar šādiem piemēriem. Cilvēka trombocītu inhibīcija agregācija BDTT un tā atvasinājumu ietekmē. Šī izgudrojuma produktu ietekme uz cilvēka trombocītu agregāciju tika pētīta ar labi zināmo Borna turbidimetrisko metodi. Šim nolūkam venozās asinis, kas tika ņemtas pulksten 8:00 no veseliem donoriem, tika centrifugētas ar ātrumu 450 g istabas temperatūrā plastmasas traukā 10 minūtes, izmantojot nātrija citrātu kā antikoagulantu. Supernatants, tas ir, ar trombocītiem bagāta plazma, tika savākta un centrifugēta ar ātrumu 650 g 30 minūtes, lai iegūtu plazmu ar trombocītiem. Trombocītu koncentrācija ar trombocītiem bagātā plazmā tika noregulēta uz 2,510 8 šūnām/ml, atšķaidot ar plazmu, kurā nav trombocītu, un iegūto suspensiju ielej 0,5 ml kivetē. Agregācija tika ierosināta, pievienojot ADP līdz koncentrācijai 20 μM. ADP koncentrācija tika izvēlēta katrā eksperimentā tā, lai agregācija būtu atgriezeniska, un maksimums notika 2 minūtes pēc ADP pievienošanas, nepārsniedzot 50%. Trombocītu suspensijas gaismas izkliede tika mērīta, izmantojot agregometru, kas izstrādāts Maskavas Valsts universitātes Bioloģijas fakultātē. M.V. Lomonosovs. Pētāmais savienojums (ūdens šķīduma veidā, ja nepieciešams, kas satur DMSO līdz 0,2%), tika pievienots paraugam pirms agregācijas induktora (ADP) pievienošanas. Šī izgudrojuma produkti koncentrācijā no 1 līdz 100 μM inhibēja trombocītu agregāciju, ko izraisīja 20 μM ADP, savukārt efektīva darbība tika novērota koncentrācijā<30 мкМ. В частности, значение концентрации, при которой достигалось полумаксимальное ингибирование, (IC 50) для БДТТ составляло 6,4 мкМ. Согласно данным прототипа, для известного аналога (3,4-дигидро-3-винил-1,2-дитиин-2-оксида) в условиях in vitro IC 50 имела значение 100 мкМ.Пример 2. Острая токсичность БДТТ и его производных.Острую токсичность соединений настоящего изобретения определяли известным способом по ЛД 50 с использованием беспородных мышей обоего пола средней массой 21 г при комнатной температуре; стандартное питание и воду давали ad libitum в течение всего эксперимента; подвижность животных не ограничивали. Растворы соединений в ДМСО вводили с помощью стерильного шприца внутрибрюшинно. После инъекции за животными вели наблюдение в течение 48 ч по истечении этого времени за мышами наблюдали дополнительно в течение 72 ч (ни одно из животных не погибло в течение дополнительного промежутка времени). Полученные результаты свидетельствуют о том, что значение ЛД 50 для БДТТ составляет >100 mg/kg, un tās atvasinājumiem ne mazāk kā 50 mg/kg Dati, kas sniegti 1. piemērā, liecina, ka aprakstītā metode ļauj efektīvāk inhibēt trombocītu agregāciju, salīdzinot ar zināmo metodi.
salīdzinoši augstās koncentrācijās (piemēram, in vitro apstākļos konkrētam savienojumam, IC 50 = 100 μM) (Japānas patents 02204487, C 07 D 339/08, op. 1991, Chem. Abstr., 1991, v. 114, p. 6523s - prototips. Izgudrojuma mērķis ir izstrādāt efektīvāku trombocītu agregācijas inhibēšanas metodi. kas raksturīgs ar to, ka zināmi BDTT vai tā atvasinājumi ar augstāk minēto vispārīgo formulu, kur R1-R4 ir dotās vērtības. Vispārīgās formulas III savienojumi tika iegūti zināmā veidā - reaģējot ar atbilstošo neaizvietoto vai aizvietoto o-hloru. - vai o-brombenzilhlorīds vai bromīds ar sēru 50-200°C temperatūrā glikola monoalkilēterī sārmu metālu alkoksīda klātbūtnē Aprakstītais izgudrojums ir ilustrēts ar šādiem piemēriem. Cilvēka trombocītu inhibīcija agregācija BDTT un tā atvasinājumu ietekmē. Šī izgudrojuma produktu ietekme uz cilvēka trombocītu agregāciju tika pētīta ar labi zināmo Borna turbidimetrisko metodi. Šim nolūkam venozās asinis, kas tika ņemtas pulksten 8:00 no veseliem donoriem, tika centrifugētas ar ātrumu 450 g istabas temperatūrā plastmasas traukā 10 minūtes, izmantojot nātrija citrātu kā antikoagulantu. Supernatants, tas ir, ar trombocītiem bagāta plazma, tika savākta un centrifugēta ar ātrumu 650 g 30 minūtes, lai iegūtu plazmu ar trombocītiem. Trombocītu koncentrācija ar trombocītiem bagātā plazmā tika noregulēta uz 2,510 8 šūnām/ml, atšķaidot ar plazmu, kurā nav trombocītu, un iegūto suspensiju ielej 0,5 ml kivetē. Agregācija tika ierosināta, pievienojot ADP līdz koncentrācijai 20 μM. ADP koncentrācija tika izvēlēta katrā eksperimentā tā, lai agregācija būtu atgriezeniska, un maksimums notika 2 minūtes pēc ADP pievienošanas, nepārsniedzot 50%. Trombocītu suspensijas gaismas izkliede tika mērīta, izmantojot agregometru, kas izstrādāts Maskavas Valsts universitātes Bioloģijas fakultātē. M.V. Lomonosovs. Pētāmais savienojums (ūdens šķīduma veidā, ja nepieciešams, kas satur DMSO līdz 0,2%), tika pievienots paraugam pirms agregācijas induktora (ADP) pievienošanas. Šī izgudrojuma produkti koncentrācijā no 1 līdz 100 μM inhibēja trombocītu agregāciju, ko izraisīja 20 μM ADP, savukārt efektīva darbība tika novērota koncentrācijā<30 мкМ. В частности, значение концентрации, при которой достигалось полумаксимальное ингибирование, (IC 50) для БДТТ составляло 6,4 мкМ. Согласно данным прототипа, для известного аналога (3,4-дигидро-3-винил-1,2-дитиин-2-оксида) в условиях in vitro IC 50 имела значение 100 мкМ.Пример 2. Острая токсичность БДТТ и его производных.Острую токсичность соединений настоящего изобретения определяли известным способом по ЛД 50 с использованием беспородных мышей обоего пола средней массой 21 г при комнатной температуре; стандартное питание и воду давали ad libitum в течение всего эксперимента; подвижность животных не ограничивали. Растворы соединений в ДМСО вводили с помощью стерильного шприца внутрибрюшинно. После инъекции за животными вели наблюдение в течение 48 ч по истечении этого времени за мышами наблюдали дополнительно в течение 72 ч (ни одно из животных не погибло в течение дополнительного промежутка времени). Полученные результаты свидетельствуют о том, что значение ЛД 50 для БДТТ составляет >100 mg/kg, un tās atvasinājumiem ne mazāk kā 50 mg/kg Dati, kas sniegti 1. piemērā, liecina, ka aprakstītā metode ļauj efektīvāk inhibēt trombocītu agregāciju, salīdzinot ar zināmo metodi.
Pretenzija
1. Metode trombocītu agregācijas inhibēšanai, ievadot sēru saturošus heterocikliskus savienojumus barotnē, kas satur šīs šūnas, kas raksturīga ar to, ka benzo-1,2-ditiol-3-tionu un tā atvasinājumus ar vispārējo formulu izmanto kā sēru saturošus heterocikliskus savienojumus.  kur R1-R4 ir H vai C1-4 ir alkilgrupa.
kur R1-R4 ir H vai C1-4 ir alkilgrupa.
Līdzīgi patenti:
Izgudrojums attiecas uz organisko ķīmiju un farmakoloģiju, proti, uz 2-etiķskābes kālija sāls izomēru maisījumu molārā attiecībā 1:3, kam piemīt kardiotoniska aktivitāte.
Hemostāzes sistēma organismā veic šādas galvenās funkcijas:
Uztur asinis traukos šķidrā stāvoklī, kas nepieciešams normālai orgānu un audu asins piegādei;
Nodrošina asiņošanas apturēšanu asinsvadu sieniņas bojājumu gadījumā.
Asiņošanas apturēšana (hemostāze - no grieķu valodas hemo- asinis, stāze- stop) tiek panākts, piedaloties vairākiem mehānismiem. Pēc asinsvadu sienas bojājumiem rodas asinsvadu spazmas. Šī tūlītējā reakcija uz traumu var apturēt asiņošanu tikai tad, ja mazu asinsvadu ievainojumi ir nelieli. Būtībā asiņošanas apturēšana tiek panākta, veidojot asins recekļus, kas novērš asins zudumu, aizverot traumas vietu. Šāda lokāla asins recekļu (hemostatisku aizbāžņu) veidošanās asinsvadu bojājumu gadījumā ir aizsargreakcija.
Tomēr noteiktos apstākļos asinsvadu iekšpusē veidojas asins recekļi, kas aizver to lūmenu un novērš normālu asins plūsmu. Intravaskulāra tromba veidošanās var notikt ar patoloģiskām izmaiņām asinsvadu endotēlijā, ieskaitot tā bojājumus, kas saistīti ar aterosklerozi, paaugstinātu asinsspiedienu vai citiem faktoriem. Asins recekļu veidošanās cēlonis var būt arī patoloģiskas izmaiņas asins plūsmā (piemēram, tās ātruma samazināšanās) vai noteiktu proteīnu deficīts, kas novērš asins recekļu veidošanos.
Tromboze notiek, piedaloties diviem galvenajiem procesiem: trombocītu agregācijai un asins koagulācijai (hemokoagulācijai).
Trombocītu agregācija - tā ir trombocītu kombinācija dažāda izmēra un blīvuma konglomerātos (agregātos). Šis process tiek uzsākts, ja tiek bojāta asinsvadu siena. Bojājuma vietā trombocīti vispirms saistās ar fon Vilebranda faktoru un subendotēlija slāņa kolagēnu (rodas trombocītu adhēzija). Mijiedarbība ar kolagēnu izraisa trombocītu aktivāciju (27.-1. att.). Šajā gadījumā trombocīti paši kļūst par vielu avotiem, kas stimulē agregāciju, piemēram, tromboksāns A2, ADP,
serotonīns. Trombīns, kas veidojas lokāli asins recēšanas laikā, arī izraisa trombocītu agregāciju. Turklāt kateholamīni, trombocītu aktivējošais faktors un dažas citas endogēnas vielas ir agregācijas induktori.
Trombocītu agregāciju novērš prostaciklīns un endotēlija relaksējošais faktors, ko ražo asinsvadu endotēlija šūnas un izdalās asinsritē. Kad endotēlija šūnas tiek bojātas, šo vielu sintēze samazinās un uz šī fona dominē vielu, kas stimulē agregāciju, iedarbība. Rezultātā trombocīti apvienojas agregātos, no kuriem veidojas trombocītu trombs.
Trombocītu trombs kļūst stiprāks, pateicoties fibrīna pavedieniem, kas veidojas procesā asins sarecēšana. Galvenie šī procesa dalībnieki ir asins plazmas olbaltumvielas, ko sauc par asinsreces faktoriem.
Plazmas koagulācijas faktori tiek sintezēti aknās un cirkulē asinīs neaktīvā formā. Ja asinsvadu siena ir bojāta, VII faktors tiek ātri aktivizēts ar līdzdalību audu faktors- transmembrānas proteīns, ko sintezē dažādas šūnas (tostarp aktivētās endotēlija šūnas) un kas parasti nesaskaras ar asinīm. Audu faktora ekspresija uz šūnas virsmas endotēlija bojājuma laikā būtiski paātrina VII faktora aktivāciju (tā pārvēršanos par VIIa faktoru) Ca 2+ jonu klātbūtnē. VIIa faktora ietekmē (kombinācijā ar audu faktoru) sarežģītā autokatalītiskā sistēmā, ko sauc par asins koagulācijas kaskādi, notiek secīga citu asinsreces faktoru (IX un X) aktivācija. Rezultātā Xa faktora ietekmē veidojas trombīns (Ha faktors), kas asinīs cirkulējošo šķīstošo proteīnu fibrinogēnu (I faktors) pārvērš nešķīstošā fibrīnā (27.-5. att.). Fibrīns polimerizējas un, aizpildot telpu starp trombocītiem, stiprina trombocītu trombu. Fibrīna pavedieni iekļūst asins receklī, veidojot tīklu, kas aiztur sarkanās asins šūnas, kas cirkulē asinīs. Veidojas sarkans asins receklis.
Asins recēšanu novērš vielas, kas ir dabiski aktīvo asinsreces faktoru inhibitori.
X faktora aktivācija ar VIIa faktoru tiek novērsta audu faktora ceļa inhibitors, sintezē endotēlija
šūnas. Trombīna un dažu citu aktīvo koagulācijas faktoru (Xa, IXa, XIa, XIIa) inhibitors ir antitrombīns III- proteīns, kas cirkulē asins plazmā, kas darbojas kombinācijā ar heparīnu vai heparīnam līdzīgām vielām (kas atrodas uz neskartu endotēlija šūnu virsmas). Šīs vielas ievērojami paātrina asinsreces faktoru inaktivāciju antitrombīna III ietekmē.
VIIIa un Va faktoru inhibitors, kas nepieciešams trombīna veidošanai aktivētais proteīns C.Šis proteīns tiek sintezēts aknās, piedaloties K vitamīnam, cirkulē asinīs neaktīvā formā un tiek aktivizēts ar trombīnu uz neskartu endotēlija šūnu virsmas. Proteīna C aktivācija palielinās līdz ar pārmērīgu trombīna veidošanos. Kad asinsvadu sieniņas bojājuma vietā veidojas lokāli asins recekļi, iepriekš minētie inhibitori palīdz uzturēt asinis šķidrā stāvoklī, novēršot asins recekļa veidošanos trauka iekšpusē.
Trombocītu agregācija un asins recēšana ir savstarpēji saistītas. Viena vai otra procesa pārsvars trombu veidošanās mehānismā ir atkarīgs no trauka kalibra un asins plūsmas ātruma. Trombocītu agregācijai ir lielāka nozīme asins recekļu veidošanā pie liela asins plūsmas ātruma, t.i. artērijās. Vēnu asinsvados, kur asins plūsmas ātrums ir zems, dominē asins recēšanas process.
Turpmākais tromba liktenis ir atkarīgs no fibrinolītiskās sistēmas aktivitātes. Ja šī sistēma funkcionē normāli, fibrīns pamazām izšķīst (fibrinolīze), piedaloties enzīmam plazmīnam, kas veidojas no neaktīva prekursora (plazminogēna) aktivatoru ietekmē. Plazmīna darbību novērš antiplazmīni, kas cirkulē asinīs. Plazminogēna aktivatorus neitralizē specifiski inhibitori.
Trombocītu agregācijas un asins koagulācijas procesu traucējumi un/vai palielināta fibrinolītiskās sistēmas aktivitāte var izraisīt asiņošanu, un pārmērīga šo procesu aktivizēšana vai fibrinolīzes kavēšana var izraisīt intravaskulāru asins recekļu veidošanos (trombozi). Arteriālo asinsvadu trombozes rezultātā samazinās asins plūsma audos un attīstās išēmija. Išēmijas sekas ir šūnu nāve (nekroze). Tromboze var izraisīt tādas nopietnas komplikācijas kā miokarda infarkts (koronāro artēriju tromboze), išēmisks insults (smadzeņu asinsvadu tromboze) utt. Vēnu tromboze var izraisīt plaušu emboliju.
Lai novērstu trombozi, tiek izmantotas vielas, kas kavē trombocītu agregāciju un asins recēšanu, tādējādi novēršot trombu veidošanos. Trombozei tiek izmantotas arī vielas, kas izraisa asins recekļu līzi - trombolītiskos (fibrinolītiskos) līdzekļus.
Lai apturētu asiņošanu, tiek izmantoti līdzekļi, kas palielina asins recēšanu, un līdzekļi, kas kavē fibrinolīzi. Viena vai otra izvēle ir atkarīga no asiņošanas cēloņa.
Praktiska nozīme ir sekojošām zāļu grupām, kas ietekmē trombu veidošanos.
Līdzekļi, kas samazina trombocītu agregāciju(antitrombocītu līdzekļi).
Zāles, kas ietekmē asins recēšanu.
Zāles, kas samazina asins recēšanu (antikoagulanti).
Zāles, kas palielina asins recēšanu (hemostatiskie līdzekļi).
Līdzekļi, kas ietekmē fibrinolīzi.
Fibrinolītiskie (trombolītiskie) līdzekļi.
Antifibrinolītiskie līdzekļi (fibrinolīzes inhibitori).
27.1. ZĀLES, KAS SAMAZINA TROMBĪTU AGREGĀCIJU (Pret trombocītu)
Trombocīti ir mazi diskveida asins elementi, kas veidojas kā kaulu smadzeņu megakariocītu fragmenti. Trombocīti cirkulē asinīs 6-12 dienas, un pēc tam tos uzņem audu makrofāgi.
Asinsvadu endotēlijs ietekmē trombocītu funkcionālo aktivitāti. Endotēlija šūnas atbrīvo asinsritē prostaciklīnu (prostaglandīnu I 2) un endotēlija relaksācijas faktoru, kas identificēts ar slāpekļa oksīdu – NO. Šīs vielas novērš trombocītu agregāciju. Turklāt endotēlija šūnas izdala vielas, kas samazina asins recēšanu un veicina trombu sabrukšanu. Tas viss nodrošina neskarta asinsvadu endotēlija antitrombogēnās īpašības.
Ja tiek bojāts asinsvadu endotēlijs, ko var izraisīt dažādi faktori (mehāniska trauma, infekcijas, aterosklerozes izmaiņas asinsvadu sieniņā, paaugstināts asinsspiediens u.c.), endotēlija antitrombogēnās īpašības samazinās, kas rada apstākļus veidošanās procesam. no asins recekļa. Tiek traucēta prostaciklīna un endotēlija relaksējošā faktora sintēze un tas atvieglo kontaktu
trombocīti ar bojātu endotēlija virsmu. Trombocīti uzkrājas bojājuma vietā un mijiedarbojas ar asinsvadu subendotēliju: tieši vai caur fon Vilebranda faktoru (ko izdala aktivēti trombocīti un endotēlija šūnas), tie saistās ar kolagēnu un citiem subendotēlija proteīniem, piedaloties trombocītā lokalizētiem specifiskiem glikoproteīniem. membrāna. Von Vilebranda faktors saistās ar glikoproteīnu Ib, bet kolagēns – ar trombocītu membrānas glikoproteīnu Ia (sk. 27-1. att.). Kolagēna (kā arī trombīna, kas lokāli veidojas nelielos daudzumos jau trombu veidošanās sākumposmā) ietekme uz trombocītiem izraisa to stāvokļa maiņu – aktivāciju. Trombocīti maina savu formu (no diska formas tie kļūst izkliedēti ar daudziem procesiem - pseidopodijas) un pārklāj bojāto kuģa virsmu.
Aktivizējoties, trombocīti izdala dažādas bioloģiski aktīvas vielas, kuras neaktivētajos trombocītos atrodas granulās (α-granulas, blīvas granulas). Blīvās granulas ir tādu vielu krātuve, kas stimulē trombocītu agregāciju: ADP un serotonīnu. Šo vielu izdalīšanās no trombocītu granulām notiek Ca 2+ intracelulārās koncentrācijas palielināšanās rezultātā kolagēna, trombīna un citu agregācijas induktoru, tostarp paša ADP, iedarbības rezultātā uz trombocītiem. Asinsritē nonākušais ADP stimulē specifiskus (purinerģiskos) receptorus, kas lokalizēti trombocītu membrānā. Caur G-proteīnu saistītiem receptoriem (P2Y 12 purinerģiskiem receptoriem) ADP izraisa adenilātciklāzes inhibīciju un cAMP līmeņa pazemināšanos, kas izraisa Ca 2 līmeņa paaugstināšanos trombocītu citoplazmā (27.-2. att.).
Turklāt, kad tiek aktivizēti trombocīti, palielinās trombocītu membrānas fosfolipāzes A2, enzīma, kas iesaistīts arahidonskābes veidošanā no membrānas fosfolipīdiem, aktivitāte. Trombocītos cikliskie endoperoksīdi (prostaglandīni G2/H2) vispirms tiek sintezēti no arahidonskābes ciklooksigenāzes ietekmē un no tiem, piedaloties tromboksanezīnam.
Tetāze ražo tromboksānu A 2, aktīvu trombocītu agregācijas stimulatoru un vazokonstriktoru. Kad tromboksāns A2 ir izlaists asinsritē, tas stimulē tromboksāna receptorus uz trombocītu membrānām. Tā rezultātā, izmantojot C, kas saistīti ar šiem receptoriem q -proteīnu fosfolipāze C tiek aktivizēta un veidošanās
Rīsi.27-1. Trombocītu adhēzija un agregācija asinsvadu sieniņas bojājuma laikā: EK - endotēlija šūna; VW - fon Vilebranda faktors; TxA 2 - tromboksāns A 2; PGI 2 - prostatciklīns; NĒ - endotēlija relaksējošais faktors; GP - glikoproteīni; GP llb/llla — glikoproteīni llb/llla (no: Katzung B.G. Bazic and Clinical Pharmacology — NY, 2001, ar grozījumiem)
inozitola-1,4,5-trifosfāts, kas veicina Ca 2+ izdalīšanos no trombocītu intracelulārās depo (kalcija depo lomu trombocītos veic blīvu kanāliņu sistēma). Tas izraisa Ca 2+ citoplazmas koncentrācijas palielināšanos (27.-2. att.). Tromboksāns A 2 izraisa Ca 2+ koncentrācijas palielināšanos asinsvadu gludās muskulatūras šūnās, kas izraisa vazokonstrikciju.

Rīsi. 27-2. Prettrombocītu līdzekļu (acetilsalicilskābe, tiklopidīns un epoprostenols) darbības mehānismi: EK - endotēlija šūna; PL - šūnu membrānu fosfolipīdi; AA - arhidonskābe; PLA 2 - fosfolipāze A 2; COX - ciklooksigenāze; TS - tromboksāna sintetāze; PS - prostaciklīna sintetāze; PGG 2 /H 2 - cikliskie endoperoksīdi; TxA 2 - tromboksāns A 2; PGI 2 - prostatciklīns; AC - adenilāta ciklāze; PLS - fosfolipāze C; IP 3 - inozīts-1, 4, 5-trifosfāts
Tādējādi ADP un tromboksāns A 2 paaugstina Ca 2+ līmeni trombocītu citoplazmā. Citoplazmas Ca 2+ izraisa glikoproteīnu IIb/IIIa konformācijas izmaiņas trombocītu membrānā, kā rezultātā tie iegūst spēju saistīt fibrinogēnu. Vienai fibrinogēna molekulai ir divas glikoproteīnu IIb/IIIa saistīšanās vietas, un tādējādi tā var apvienot divus trombocītus (27.-3. att.). Daudzu trombocītu savienošanās ar fibrinogēna tiltiem izraisa trombocītu agregātu veidošanos.
Prostaciklīnam (prostaglandīnam I 2) ir pretēja ietekme uz trombocītu agregāciju. Tāpat kā tromboksāns, prostatciklīns
veidojas no cikliskajiem endoperoksīdiem, bet cita enzīma – prostaciklīna sintetāzes – iedarbībā. Prostaciklīnu sintezē endotēlija šūnas un izdala asinsritē, kur tas stimulē trombocītu membrānas prostaciklīna receptorus un ar tiem saistīto adenilāta ciklāzi caur G s proteīnu. Tā rezultātā palielinās cAMP līmenis trombocītos un samazinās citoplazmas Ca 2+ koncentrācija (sk. 27-2. att.). Tas novērš glikoproteīnu IIb/IIIa konformācijas izmaiņas un tie zaudē spēju saistīt fibrinogēnu. Tādējādi prostaciklīns novērš trombocītu agregāciju. Prostaciklīna ietekmē samazinās Ca 2+ koncentrācija asinsvadu gludās muskulatūras šūnās, kas izraisa vazodilatāciju.

Var izdalīt šādu galveno notikumu secību, kas izraisa trombocītu agregāciju (skatīt 27-1. diagrammu).
Patlaban klīniskajā praksē lietoto prettrombocītu līdzekļu darbības galvenais akcents ir saistīts ar tromboksāna A 2 un ADP darbības likvidēšanu, kā arī ar trombocītu membrānu glikoproteīnu IIb/IIIa bloķēšanu. Tiek izmantotas arī vielas ar atšķirīgu darbības mehānismu, kas palielina cAMP koncentrāciju trombocītos un līdz ar to samazina Ca 2+ koncentrāciju tajos.
Izšķir šādas līdzekļu grupas, kas samazina trombocītu agregāciju.
Līdzekļi, kas inhibē tromboksāna A2 sintēzi. - Ciklooksigenāzes inhibitori:
acetilsalicilskābe.

Shēma 27.1. Trombocītu agregācijas mehānisms
Ciklooksigenāzes un tromboksāna sintetāzes inhibitori: indobufēns.
Līdzekļi, kas stimulē prostatasciklīna receptorus:
epoprostenols**.
Līdzekļi, kas traucē ADP ietekmi uz trombocītiem:
tiklopidīns; klopidogrels.
Līdzekļi, kas inhibē trombocītu fosfodiesterāzi:
dipiridamols
Līdzekļi, kas bloķē trombocītu membrānu glikoproteīnus IIb/IIIa.
Monoklonālās antivielas: abciksimabs.
Sintētiskie glikoproteīnu IIb/IIIa blokatori: eptifibatīds; tirofibāns.
Līdzekļi, kas inhibē tromboksāna A sintēzi 2
Acetilsalicilskābe (aspirīns*) ir labi zināms pretiekaisuma, pretsāpju un pretdrudža līdzeklis. Pašlaik plaši izmanto kā prettrombocītu līdzekli. Acetilsalicilskābes prettrombocītu iedarbība ir saistīta ar tās inhibējošo iedarbību uz tromboksāna A 2 sintēzi trombocītos.
Acetilsalicilskābe neatgriezeniski inhibē ciklooksigenāzi (izraisa neatgriezenisku enzīma acetilēšanu) un tādējādi izjauc ciklisko endoperoksīdu, tromboksāna A2 prekursoru un prostaglandīnu veidošanos no arahidonskābes. Tāpēc acetilsalicilskābes ietekmē samazinās ne tikai tromboksāna A 2 sintēze trombocītos, bet arī prostaciklīna sintēze asinsvadu endotēlija šūnās (sk. 27.-2. att.). Tomēr, izvēloties atbilstošas devas un režīmu, ir iespējams panākt acetilsalicilskābes preferenciālu ietekmi uz tromboksāna A 2 sintēzi. Tas ir saistīts ar ievērojamām atšķirībām starp trombocītiem un endotēlija šūnām.
Trombocīti – šūnas ar kodolu – nesatur proteīnu resintēzes sistēmu, un tāpēc tās nespēj sintezēt ciklooksigenāzi. Tāpēc ar neatgriezenisku šī enzīma inhibīciju tromboksāna A2 sintēzes traucējumi saglabājas visu trombocītu dzīves laiku, t.i. 7-10 dienu laikā. Jaunu trombocītu veidošanās dēļ acetilsalicilskābes prettrombocītu iedarbība saglabājas īsāku laiku, un tāpēc, lai panāktu stabilu zāļu iedarbību (t.i., stabilu tromboksāna līmeņa pazemināšanos), ieteicams tās parakstīt. vienreiz dienā.
Cikloksigenāze tiek atkārtoti sintezēta asinsvadu endotēlija šūnās, un šī enzīma aktivitāte tiek atjaunota dažu stundu laikā pēc acetilsalicilskābes lietošanas. Tādēļ, izrakstot zāles vienu reizi dienā, nav ievērojama prostatasciklīna sintēzes samazināšanās.

Turklāt aptuveni 30% acetilsalicilskābes tiek pakļauti pirmā loka metabolismam aknās, tāpēc tās koncentrācija sistēmiskajā cirkulācijā ir zemāka nekā portāla asinīs. Rezultātā acetilsalicilskābe iedarbojas uz trombocītiem, kas cirkulē portāla asinsritē lielākā koncentrācijā nekā uz sistēmisko asinsvadu endotēlija šūnām. Tāpēc, lai nomāktu tromboksāna A2 sintēzi trombocītos, ir nepieciešamas mazākas acetilsalicilskābes devas nekā prostaciklīna sintēzes nomākšanai endotēlija šūnās.
Šo iemeslu dēļ, palielinoties acetilsalicilskābes devai un ievadīšanas biežumam, tās inhibējošā iedarbība uz prostaciklīna sintēzi kļūst izteiktāka, kas var izraisīt prettrombocītu iedarbības samazināšanos. Saistībā ar šīm īpašībām acetilsalicilskābi kā prettrombocītu līdzekli ieteicams ordinēt nelielās devās (vidēji 100 mg) vienu reizi dienā.
Kā prettrombocītu līdzekli acetilsalicilskābi lieto nestabilas stenokardijas gadījumā, miokarda infarkta, išēmiska insulta un perifēro asinsvadu trombozes profilaksei, lai novērstu asins recekļu veidošanos koronāro artēriju šuntēšanas un koronārās angioplastikas laikā. Acetilsalicilskābi ordinē iekšķīgi 75-160 mg devās (noteiktām indikācijām - devu diapazonā no 50 līdz 325 mg) vienu reizi dienā ilgu laiku. Šobrīd ārstu rīcībā ir trombozes profilaksei paredzēti acetilsalicilskābes preparāti, kas satur 50-325 mg aktīvās vielas, tai skaitā zarnās šķīstošās tabletes - Acecardol*, Aspicor*, Cardiopyrin*, Aspirin Cardio*, Novandol*, Trombo ACC * uc Acetilsalicilskābes prettrombocītu iedarbība notiek ātri (20-30 minūšu laikā). Zarnu šķīstošās zāļu formas sāk darboties lēnāk, taču, ilgstoši lietojot, to efektivitāte praktiski neatšķiras no parasto tablešu efektivitātes. Lai panāktu ātrāku efektu, acetilsalicilskābes tabletes jāsakošļā.
Galvenās acetilsalicilskābes blakusparādības ir saistītas ar ciklooksigenāzes inhibīciju. Tas izjauc prostaglandīnu E 2 un I 2 veidošanos, kuriem ir antisekretāra un gastroprotektīva iedarbība (samazina sālsskābes sekrēciju kuņģa parietālajās šūnās, palielina gļotu un bikarbonātu sekrēciju). Tā rezultātā, pat īslaicīgi lietojot, acetilsalicilskābe var izraisīt kuņģa un divpadsmitpirkstu zarnas epitēlija bojājumus (ulcerogēna iedarbība). Ietekme uz kuņģa gļotādu ir mazāk izteikta, lietojot zarnās šķīstošās zāļu formas. Lietojot acetilsalicilskābi, iespējama kuņģa-zarnu trakta asiņošana un citas hemorāģiskas komplikācijas. Šādu komplikāciju risks ir mazāks, ja acetilsalicilskābi izraksta 100 mg/dienā vai mazākā devā. Selektīva COX inhibīcija noved pie lipoksigenāzes ceļa aktivizēšanas arahidonskābes pārvēršanai un leikotriēnu veidošanās, kam piemīt bronhokonstriktora īpašības. Pacientiem ar bronhiālo astmu acetilsalicilskābe var izraisīt lēkmes (“aspirīna astma”) rašanos. Iespējamas alerģiskas reakcijas.
Lai samazinātu acetilsalicilskābes čūlu izraisošo iedarbību, ir ierosināts kombinētais medikaments Cardiomagnyl *, kas satur magnija hidroksīdu. Magnija hidroksīds neitralizē sālsskābi kuņģī (antacīds efekts), samazinot tās kaitīgo ietekmi uz gļotādu. Zāles lieto tādām pašām indikācijām kā acetilsalicilskābi, tostarp išēmiska insulta sekundārai profilaksei.
Indobufēns (ibustrīns *) samazina tromboksāna A 2 sintēzi, vienlaikus inhibējot ciklooksigenāzi un tromboksāna sintetāzi. Atšķirībā no acetilsalicilskābes, indobufēns izraisa atgriezenisku ciklooksigenāzes inhibīciju. Lietojot šīs zāles, relatīvi palielinās prostaciklīna daudzums (palielinās prostaciklīna/tromboksāna A 2 attiecība). Indobufēns kavē trombocītu adhēziju un agregāciju. Lietošanas indikācijas un blakusparādības ir tādas pašas kā acetilsalicilskābei.
Līdzekļi, kas stimulē prostatasciklīna receptorus
Vēl viens veids, kā samazināt trombocītu agregāciju, ir prostatasciklīna receptoru stimulēšana. Šim nolūkam viņi izmanto
prostaciklīna preparāts e p o pro s t e n o l * . Prostaciklīna iedarbība ir pretēja tromboksāna A 2 iedarbībai ne tikai uz trombocītiem, bet arī uz asinsvadu tonusu. Tas izraisa vazodilatāciju un asinsspiediena pazemināšanos. Šo prostatasciklīna iedarbību izmanto plaušu hipertensijas gadījumā. Tā kā prostaciklīns tiek ātri iznīcināts asinīs (t 1/2 apmēram 2 minūtes) un tāpēc neiedarbojas ilgi, zāles ievada infūzijas veidā. Īsās darbības dēļ epoprostenols* nav plaši izmantots kā prettrombocītu līdzeklis. Iespējama epoprostenola prettrombocītu iedarbības izmantošanas joma ir trombocītu agregācijas novēršana ekstrakorporālās cirkulācijas laikā.
Līdzekļi, kas traucē ADP darbību uz trombocītiem
Tiklopidīns (ticlid*), tienopiridīna atvasinājums, inhibē trombocītu agregāciju, ko izraisa ADP. Tiklopidīns ir priekšzāles, tā antitrombocītu iedarbība ir saistīta ar aktīvā metabolīta veidošanos, kurā piedalās mikrosomu aknu enzīmi. Tiklopidīna metabolīts satur tiola grupas, caur kurām tas neatgriezeniski saistās ar P2Y 12 purinerģiskiem receptoriem trombocītu membrānā. Tas noved pie ADP stimulējošās iedarbības uz trombocītiem likvidēšanas un citoplazmas Ca 2+ koncentrācijas samazināšanās tajos. Tā rezultātā samazinās glikoproteīnu IIb/IIIa ekspresija trombocītu membrānā un saistīšanās ar fibrinogēnu (sk. 27.-2. att.). Tā kā tiklopidīna darbība ir neatgriezeniska, tam ir ilgstoša prettrombocītu iedarbība.
Maksimālais efekts, pastāvīgi lietojot tiklopidīnu, tiek sasniegts pēc 7-11 dienām (laiks, kas nepieciešams aktīvā metabolīta veidošanās un darbības attīstībai), un pēc zāļu lietošanas pārtraukšanas tas saglabājas visā trombocītu dzīves laikā (7-10). dienas).
Tiklopidīns ir paredzēts išēmiska insulta sekundārai profilaksei, trombozes profilaksei apakšējo ekstremitāšu obliterējošu slimību gadījumā, koronāro artēriju šuntēšanas un koronāro artēriju stentēšanas laikā. Zāles ir efektīvas, lietojot iekšķīgi, parakstītas 2 reizes dienā ēdienreizes laikā.
Tiklopidīna lietošana ir ierobežota tā blakusparādību dēļ. Iespējama apetītes zudums, slikta dūša, vemšana, caureja (20%), sāpes vēderā, izsitumi uz ādas (11-14%). Atzīmēts
aterogēno lipoproteīnu līmeņa paaugstināšanās asins plazmā. Asiņošana ir bieži sastopama komplikācija, lietojot prettrombocītu līdzekļus. Bīstama komplikācija ir neitropēnija, kas pirmajos trīs ārstēšanas mēnešos rodas 1-2,4% pacientu. Iespējama trombocitopēnija, agranulocitoze un ļoti reti aplastiskā anēmija. Šajā sakarā pirmajos ārstēšanas mēnešos ir nepieciešama sistemātiska asins ainas kontrole.
Klopidogrels (Plavix*, Zilt*) pēc ķīmiskās struktūras, galvenās iedarbības un darbības mehānisma ir līdzīgs tiklopidīnam. Tāpat kā tiklopidīns, tas ir priekšzāles un tiek pārveidots aknās, veidojot aktīvu metabolītu. Ievērojama trombocītu agregācijas inhibīcija tika novērota no otrās ārstēšanas dienas, maksimālais efekts tiek sasniegts pēc 4-7 dienām. Pēc zāļu lietošanas pārtraukšanas tā iedarbība ilgst 7-10 dienas. Klopidogrels pēc aktivitātes ir pārāks par tiklopidīnu – 75 mg dienas devā tas izraisa tādu pašu trombocītu agregācijas samazināšanos un asiņošanas laika pagarināšanos kā tiklopidīns 500 mg dienas devā.

Klopidogrelu lieto tādām pašām indikācijām kā acetilsalicilskābi nepanesības gadījumā. Lietojiet iekšķīgi 1 reizi dienā neatkarīgi no ēdienreizēm. Klopidogrelu var kombinēt ar acetilsalicilskābi, jo zāles inhibē dažādus trombocītu agregācijas mehānismus un tādējādi pastiprina viena otras iedarbību (tomēr ar šo kombināciju ir lielāks hemorāģisko komplikāciju risks).
Salīdzinot ar tiklopidīnu, klopidogrela blakusparādības ir mazāk izteiktas (caureja - 4,5%, izsitumi - 6%). Klopidogrela lietošana ir saistīta ar mazāku tādas nopietnas komplikācijas kā neitropēnijas risku (0,1%), un trombocitopēnija rodas retāk. Kā reta komplikācija, tāpat kā tiklopidīna gadījumā, var attīstīties trombotiska trombocitopēniskā purpura.
Trombocītu fosfodiesterāzes inhibitori
Dipiridamols (kurantils*, persantīns*) pirmo reizi tika piedāvāts kā koronāro asinsvadu paplašinātājs. Vēlāk tika atklāta tā spēja inhibēt trombocītu agregāciju. Pašlaik dipiridamolu galvenokārt izmanto kā prettrombocītu līdzekli trombozes profilaksei. Dipiridamola prettrombocītu iedarbība ir saistīta ar cAMP līmeņa paaugstināšanos trombocītos, kā rezultātā tajos samazinās citoplazmas Ca 2+ koncentrācija. Tas notiek vairāku iemeslu dēļ. Pirmkārt, dipiridamols inhibē fosfodiesterāzi, kas inaktivē cAMP. Turklāt dipiridamols kavē endotēlija šūnu un eritrocītu adenozīna uzņemšanu un tā metabolismu (inhibē adenozīna deamināzi), tādējādi paaugstinot adenozīna līmeni asinīs (27.-4. att.). Adenozīns stimulē trombocītu A 2 receptorus un palielina ar šiem receptoriem saistītās adenilātciklāzes aktivitāti, kā rezultātā palielinās cAMP veidošanās trombocītos un samazinās citoplazmas Ca 2+ līmenis. Dipiridamols arī palielina cAMP līmeni asinsvadu gludās muskulatūras šūnās, izraisot asinsvadu relaksāciju.

Dipiridamolu lieto išēmiska insulta profilaksei, kā arī perifēro artēriju slimībām (galvenokārt kombinācijā ar acetilsalicilskābi, jo pašam dipiridamolam ir vāja prettrombocītu iedarbība). Izrakstīts iekšķīgi 3-4 reizes dienā 1 stundu pirms ēšanas. Kombinācijā ar perorāliem antikoagulantiem dipiridamolu ordinē, lai novērstu asins recekļu veidošanos mitrālās sirds slimības gadījumā.
Lietojot dipiridamolu, rodas galvassāpes, reibonis, arteriāla hipotensija, dispepsijas simptomi,
ādas izsitumi. Asiņošanas risks ir mazāks nekā lietojot acetilsalicilskābi. Dipiridamols ir kontrindicēts stenokardijas (iespējams "zagšanas sindroma") gadījumos.

Rīsi. 27-4. Dipiridamola prettrombocītu darbības mehānisms: EC - endotēlija šūna; A 2 -P - adenozīna A 2 receptors; PDE - cAMP fosfodiesterāze; AC - adenilāta ciklāze; GP IIb/IIIa - glikoproteīni IIb/IIIa
Pentoksifilīns (agapurīns*, trentāls*), tāpat kā dipiridamols, inhibē fosfodiesterāzi un paaugstina cAMP līmeni. Tā rezultātā samazinās citoplazmas Ca 2 + līmenis trombocītos, kas izraisa to agregācijas samazināšanos. Pentoksifilīnam piemīt arī citas īpašības: tas palielina sarkano asins šūnu deformējamību, samazina asins viskozitāti, ir vazodilatējoša iedarbība, uzlabojot mikrocirkulāciju.
Pentoksifilīnu lieto smadzeņu asinsrites traucējumu, dažādas izcelsmes perifērās asinsrites traucējumu un acu asinsvadu patoloģiju gadījumos (skat. nodaļu “Smadzeņu asinsrites traucējumu gadījumos lietojamās zāles”). Iespējamās blakusparādības: dispepsijas simptomi, reibonis, sejas apsārtums, kā arī asinsspiediena pazemināšanās, tahikardija, alerģiskas reakcijas, asiņošana. Tāpat kā dipiridamols, tas var izraisīt lēkmes stenokardijas laikā.
Līdzekļi, kas bloķē trombocītu membrānu glikoproteīnus IIb/IIIa
Šī prettrombocītu līdzekļu grupa, kas tieši mijiedarbojas ar trombocītu membrānu glikoproteīniem IIb/IIIa un traucē to saistīšanos ar fibrinogēnu, parādījās salīdzinoši nesen.
Abciksimabs (reopro*) – pirmais medikaments no šīs grupas ir “himēriskā” peles/cilvēka monoklonālā antiviela (Fab fragments peles antivielām pret glikoproteīniem IIb/IIIa apvienojumā ar cilvēka Ig Fc fragmentu). Abciksimabs nekonkurējoši inhibē fibrinogēna saistīšanos ar glikoproteīniem IIb/IIIa uz trombocītu membrānas, izjaucot to agregāciju (skatīt 27.-3. att.). Trombocītu agregācija normalizējas 48 stundas pēc vienas devas lietošanas. Zāles ievada intravenozi (infūzijas veidā), lai novērstu trombozi koronāro artēriju angioplastikas laikā. Lietojot abciksimabu, ir iespējama asiņošana, tai skaitā iekšēja (kuņģa-zarnu trakta, intrakraniāla, asiņošana no uroģenitālā trakta), slikta dūša, vemšana, hipotensija, bradikardija, alerģiskas reakcijas līdz anafilaktiskajam šokam, trombocitopēnija.
Meklējot mazāk alerģiskas zāles ar tādu pašu darbības mehānismu, tika izveidoti sintētiski glikoproteīnu IIb/IIIa blokatori. Pamatojoties uz barborīnu (peptīdu, kas izolēts no pigmeja klaburčūskas indes), tika iegūts medikaments e p t i f i b a t i d (integrilīns *) - ciklisks hektapeptīds, kas imitē fibrinogēna ķēdes aminoskābju secību, kas tieši saistās ar glikoproteīniem IIb/III. Eptifibatīds konkurētspējīgi izspiež fibrinogēnu no saistīšanās ar receptoriem, izraisot atgriezeniskus trombocītu agregācijas traucējumus. Zāles ievada intravenozi infūzijas veidā; antitrombocītu iedarbība rodas 5 minūšu laikā un izzūd 6-12 stundas pēc lietošanas pārtraukšanas. Zāles ir ieteicamas trombu veidošanās profilaksei perkutānās koronārās angioplastikas laikā, nestabilas stenokardijas gadījumā un miokarda infarkta profilaksei. Bīstama komplikācija, lietojot eptifibatīdu, ir asiņošana; iespējama trombocitopēnija.
Tirofibāns (agrastats*) ir glikoproteīnu IIb/IIIa ne-peptīdu bloķētājs, tirozīna analogs. Tāpat kā eptifibatīds, tirofibāns konkurētspējīgi bloķē glikoproteīna IIb/IIIa receptorus. Zāles ievada intravenozi (infūzijas veidā). Iedarbības sākuma ātrums, darbības ilgums un lietošanas indikācijas ir tādas pašas kā eptifibatīdam. Blakusparādības - asiņošana, trombocitopēnija.
Lai paplašinātu šīs grupas zāļu lietošanas iespējas, tika izveidoti glikoproteīnu IIb/IIIa blokatori, kas ir efektīvi, ja tos lieto iekšķīgi - ksemilofibāns *, sibrafibāns * u.c. Tomēr šo zāļu testi atklāja to nepietiekamo efektivitāti un blakusparādību. smagas trombocitopēnijas forma.
27.2. NARKOTIKAS, KAS IETEKMĒ ASINS RESĒŠANU
Asinsvadu sieniņu bojājumi ierosina ne tikai trombocītu agregāciju, bet arī asins recēšanu. Šajā procesā ir iesaistīti daudzi zināmi faktori (plazma, audi, trombocīti). Lielākā daļa no tiem ir plazmas proteīni, kas cirkulē neaktīvā stāvoklī, bet pēc tam tiek aktivizēti asins recēšanas procesa laikā. Lai izskaidrotu zāļu iedarbību, jāmin VII faktors (prokonvertīns), IX faktors (Ziemassvētki), X faktors (Stuart-Prower), faktors II (protrombīns). Šie koagulācijas faktori ir proenzīmi un, aktivizējoties, tiek pārvērsti proteolītiskos enzīmos (faktori GCa, Xa un Na). VIII un V faktors pēc aktivācijas darbojas kā enzīmu kofaktoru proteīni (attiecīgi IXa un Xa faktori), palielinot to proteolītisko aktivitāti.
VII faktoram sākotnēji ir zema proteolītiskā aktivitāte, bet mijiedarbības rezultātā ar audu faktoru (sk. 481. lpp.) tas ātri palielinās. Aktivētais VII faktors (faktors VIIa) kopā ar audu faktoru un Ca 2+ veido kompleksu, kas izraisa IX un X faktoru daļēju proteolīzi. Savukārt IXa faktors papildus aktivizē X faktoru (veidojas Xa faktors). Xa faktors iedarbojas uz protrombīnu (II faktors) un pārvērš to trombīnā (Ha faktors). Trombīns izraisa daļēju fibrinogēna proteolīzi, veidojot fibrīnu (27.-5. att.).
Asins koagulācijas faktoru proteolītiskā aktivācija ir ievērojami paātrināta, ja tie caur Ca 2+ joniem saistās ar negatīvi lādētiem šūnu membrānu fosfolipīdiem. Šie fosfolipīdi darbojas kā sava veida matrica, uz kuras koagulācijas faktori tiek salikti kompleksos, piedaloties Ca 2 + joniem. Tajā pašā laikā faktoru aktivizācijas ātrums šajos kompleksos palielinās 10 tūkstošus reižu vai vairāk. Nepieciešams nosacījums šādu kompleksu veidošanai ir II, VII, IX un X faktoru spēja saistīties ar Ca 2 +. Šie faktori satur negatīvu lādiņu
γ-karboksiglutamīnskābju atliekas, kas nodrošina to saistīšanos ar Ca 2+. γ-karboksiglutamīnskābju veidošanās notiek aknās, piedaloties K vitamīnam. Ar K vitamīna deficītu asinīs parādās bojāti II, VII, IX un X asinsreces faktori, kas izjauc fibrīna veidošanos.

Rīsi. 27-5. Asins koagulācijas aktivizēšanas shēma asinsvadu sieniņas bojājuma gadījumā (No: Katzung B. G. Pamata un klīniskā farmakoloģija. - NY, 2001, ar grozījumiem): asins koagulācijas faktoru kompleksi, kas saistīti ar šūnu membrānu negatīvi lādētiem fosfolipīdiem, ir pasvītroti ar treknā līnija. Komplekss VIIa + TF + Ca 2+ aktivizē X un IX faktorus (TF - audu faktors). Komplekss IXa + VIIIa + Ca 2+ papildus aktivizē X faktoru. Komplekss Xa + Va + Ca 2+ (protrombināze) veicina protrombīna pārvēršanu trombīnā. Kastītēs ievietotos faktorus inhibē heparīns
Asins plazmas olbaltumvielas, kas satur γ-karboksiglutamīnskābes atlikumus un veidojas aknās, piedaloties K vitamīnam, ietver arī proteīnus C un S. Pēc aktivācijas proteīns C (Ca) izraisa VIIIa un Va faktoru proteolītisko šķelšanos. Tas izraisa trombīna veidošanās traucējumus. Proteīns S darbojas kā kofaktors proteolīzes reakcijās. C proteīna aktivācija notiek trombīna ietekmē uz neskartu (nebojātu) endotēlija šūnu virsmas, kas ekspresē proteīna trombomodulīnu, kas vienlaikus saista C proteīnu un trombīnu.
27.2.1. Antikoagulanti (antikoagulanti)
Klīniskajā praksē izmantotie antikoagulanti inhibē aktīvos recēšanas faktorus tieši asinīs vai traucē to veidošanos aknās. Tāpēc tos iedala 2 grupās:
(darbojas tieši asinīs).
- Heparīna standarts(nefrakcionēts).
- Zemas molekulmasas heparīni:
enoksaparīna nātrijs;
Nadroparīna kalcijs;
Dalteparīna nātrijs;
Reviparīna nātrijs.
- Heparinoīdi:
Sulodeksīds;
Danaparoid**.
- Antitrombīna III zāles.
- Hirudīna preparāti:
Lepirudīns*.
- Aktivētais proteīns C:
Alfa drotrekogīns.
(inhibē koagulācijas faktoru sintēzi aknās).
- Kumarīna atvasinājumi:
Acenokumarols (sinkumars*);
Varfarīns (varfareks*).
- Indāndiona atvasinājumi:
Fenindions (fenilīns*).
Tiešie antikoagulanti
Heparīns- sulfāts glikozaminoglikāns (mukopolisaharīds), kas sastāv no D-glikozamīna un D-glikuronskābes atlikumiem. Heparīnu ražo tuklo šūnas daudzos audos; to lielos daudzumos satur aknas, plaušas un zarnu gļotāda. Medicīniskiem nolūkiem heparīnu izdala no cūku zarnu gļotādas un no liellopu plaušām. Notiek
izolēšana rada frakciju maisījumu ar dažādu polisaharīdu ķēdes garumu un dažādu molekulmasu (no 3000 līdz 40 000 D). Frakcijas ar dažādu molekulmasu nedaudz atšķiras pēc bioloģiskās aktivitātes un farmakokinētiskajām īpašībām. Tāpēc ar dažādām metodēm un no dažādiem avotiem iegūtiem heparīna preparātiem var būt atšķirīga antikoagulanta aktivitāte, kā rezultātā nepieciešams veikt to bioloģisko standartizāciju. Heparīna aktivitāti nosaka tā spēja pagarināt asins recēšanas laiku (1 mg standarta heparīna satur 130 vienības).
Heparīnam ir ietekme uz asinsreces faktoriem tikai pēc kompleksa veidošanās ar endogēno antikoagulantu antitrombīnu III. Antitrombīns III, asins plazmas glikoproteīns, inhibē serīna proteāzes, kas ietver asins koagulācijas faktorus IIa (trombīnu), EXa un Xa (kā arī XIa un XIIa). Faktoru inaktivācijas process tikai antitrombīna III ietekmē norit ļoti lēni. Heparīns izraisa konformācijas izmaiņas antitrombīna III molekulā, kas noved pie šī procesa paātrinājuma aptuveni 1000 reizes.

Heparīna-antitrombīna III kompleksa galvenā darbība ir vērsta pret trombīnu un Xa faktoru, taču šo faktoru inhibīcijas mehānismiem ir dažas atšķirības. Lai inaktivētu trombīnu, heparīnam jāsaistās gan ar antitrombīna III molekulu, gan ar trombīna molekulu. Tajā pašā laikā ātrai Xa faktora inaktivācijai ar heparīna-antitrombīna III kompleksu nav nepieciešama šī faktora saistīšanās ar heparīnu. Heparīna frakcijas ar relatīvi īsu polimēra ķēdi (mazāk par 18 saharīdu vienībām) nevar vienlaikus saistīt antitrombīnu III un trombīnu, un tāpēc tām nav antitrombīna aktivitātes. To darbība galvenokārt ir saistīta ar Xa faktora inaktivāciju un līdz ar to protrombīna pārvēršanas trombīnā pārtraukšanu.
Papildus ietekmei uz asins recēšanu heparīnam ir arī daži citi efekti: tas samazina lipīdu līmeni asinīs, jo tiek aktivizēta lipoproteīna lipāze (šis enzīms hidrolizē triglicerīdus), kā arī nomāc gludo muskuļu šūnu proliferāciju.
Lietojot perorāli, heparīns slikti uzsūcas, tāpēc to ievada intravenozi, dažreiz subkutāni. Ievadot intravenozi, efekts rodas nekavējoties un ilgst 2-6 stundas Ievadot subkutāni, heparīns sāk darboties pēc 1-2 stundām, darbības ilgums ir 8-12 stundas (izrakstīts 2-3 reizes dienā). Heparīns asinīs saistās ar daudziem proteīniem, tostarp tiem, kas to neitralizē (trombocītu faktors 4 un daži citi). Augsts šo olbaltumvielu līmenis asinīs var izraisīt relatīvu rezistenci pret zālēm. Turklāt heparīns saistās ar makrofāgiem un endotēlija šūnām, un notiek tā degradācija (depolimerizācija). Heparīns arī metabolizējas aknās un izdalās caur nierēm.
Heparīnu lieto dziļo vēnu trombozes un plaušu embolijas profilaksei un ārstēšanai, nestabilas stenokardijas un miokarda infarkta gadījumā, perifēro artēriju trombozes profilaksei, sirds vārstuļu nomaiņai un ekstrakorporālajai cirkulācijai. Heparīnu dozē darbības vienībās (AU).
Biežākās heparīna terapijas komplikācijas ir asiņošana, ko var izraisīt trombocītu funkcijas kavēšana vai to skaita samazināšanās (trombocitopēnija). Šķiet, ka heparīna saistīšanās ar fon Vilebranda faktoru izskaidro tā inhibējošo ietekmi uz trombocītu adhēziju un agregāciju. Šādos gadījumos heparīna lietošana tiek pārtraukta, un nopietnas asiņošanas gadījumā intravenozi tiek ievadīts arī protamīna sulfāts, kas neitralizē heparīnu, veidojot nešķīstošu kompleksu.
Trombocitopēnija rodas 7.–14. ārstēšanas dienā aptuveni 1–5% pacientu, kuri saņem heparīnu. To izraisa antivielu (IgG) parādīšanās, kas vērstas pret heparīna-trombocītu faktora 4 kompleksu. Šis komplekss saistās ar trombocītu membrānu, neitralizējot heparīnu ar 4. faktoru — trombocītu izcelsmes glikoproteīnu, kas izdalās trombocītu agregācijas rezultātā. Mazāk nekā 1% pacientu ar trombocitopēniju novēro trombozi endotēlija bojājumu dēļ
šūnas un trombocītu aktivizēšana ar antivielām pret heparīna-faktora 4 kompleksu. Šis stāvoklis prasa pārtraukt heparīna lietošanu un nozīmēt antikoagulantus, kas neizraisa trombocitopēniju: danaparoīdu** un lepirudīnu**.
Ilgstoši lietojot heparīnu (vairāk nekā 3 mēnešus), var attīstīties osteoporoze. Tas ir īpaši svarīgi ņemt vērā, parakstot heparīnu grūtniecības laikā. Hiperkaliēmija, kas saistīta ar aldosterona sintēzes inhibīciju virsnieru dziedzeros, ir diezgan reta heparīna terapijas komplikācija.
Zemas molekulmasas (frakcionēti) heparīni sastāv no heparīna fragmentiem ar molekulmasu no 1000 līdz 10 000 D (vidēji 4000-5000 D). Tos iegūst, frakcionējot, hidrolizējot vai depolimerizējot parasto (nefrakcionētu) heparīnu. Šīs zāles, piemēram, heparīns, iedarbojas uz koagulācijas faktoriem, izmantojot antitrombīnu III, bet atšķiras no heparīna ar šādām īpašībām:
Tie kavē Xa faktora aktivitāti lielākā mērā nekā faktora IIa (3-4 reizes);
Viņiem ir lielāka biopieejamība, ja tos ievada subkutāni (zemas molekulmasas heparīni - aptuveni 90%, standarta heparīns - 20%);
Tie iedarbojas uz ilgāku laiku, kas ļauj tos ievadīt 1-2 reizes dienā;
Viņiem ir mazāka afinitāte pret trombocītu faktoru 4, tāpēc tie mazāk izraisa trombocitopēniju nekā standarta heparīns;
Retāk izraisa osteoporozi.
Iekšzemes praksē izmanto šādus zemas molekulmasas heparīnu preparātus: en o x a parin sodium (Clexane *), nadroparin kalcija (Fraxiparin *), d alte parin sodium (Fragmin *), reviparin sodium (klivarin*). Šīs zāles pēc sastāva ir neviendabīgas (satur dažādas heparīna frakcijas), tāpēc tās nedaudz atšķiras viena no otras pēc fizikāli ķīmiskajām, farmakokinētiskajām īpašībām un aktivitātes.
Zemas molekulmasas heparīnus lieto dziļo vēnu trombozes profilaksei un ārstēšanai (īpaši pēc operācijām), plaušu embolijas profilaksei, kā arī nestabilas stenokardijas un miokarda infarkta gadījumā. Profilaksei indicēti zemas molekulmasas heparīna preparāti
tiki un trombozes terapija dzemdniecības praksē. Ievada tikai subkutāni. Deva ir norādīta ME (starptautiskajās vienībās).
Zemas molekulmasas heparīni, tāpat kā nefrakcionēti heparīna preparāti, var izraisīt asiņošanu. Pirmajās ārstēšanas dienās iespējama mērena trombocitopēnija. Zemas molekulmasas heparīni dažos gadījumos palielina aknu enzīmu aktivitāti un var izraisīt alerģiskas reakcijas. Protamīna sulfāts pilnībā nenovērš zemas molekulmasas heparīnu iedarbību.
Pēdējā laikā klīniskajā praksē parādījās medikaments fo n d a p a - nātrija rinukss - sintētisks pentasaharīds, kas, saistoties ar antitrombīnu III, paātrina Xa faktora inaktivāciju. Zāles ražo nātrija sāls veidā un lieto vēnu trombozes un plaušu embolijas profilaksei ortopēdiskajā ķirurģijā.
Heparinoīdi- sulfēti glikozaminoglikāni, strukturāli līdzīgi heparīniem. Tāpat kā heparīns, tie pastiprina antitrombīna III inhibējošo iedarbību uz asins koagulācijas faktoriem. Daudzās svarīgās īpašībās tie atšķiras no heparīna un zemas molekulmasas heparīniem, tāpēc tos klasificē īpašā grupā. Danaparoid* un sulodeksīds pieder šai grupai. Šīs zāles iegūst no cūku zarnu gļotādas.
Danaparoid** (organons**) satur heparāna sulfāta, dermatāna sulfāta un hondroitīna sulfāta maisījumu. Danaparoid p inhibē Xa faktoru vairāk nekā protrombīns. Zāles ievada subkutāni vēnu trombozes profilaksei un ārstēšanai. Danaparoid p nesaistās ar trombocītu faktoru 4 un neizraisa trombocitopēniju. Tāpēc tas ir indicēts gadījumos, kad heparīna terapiju sarežģī trombocitopēnija.
Sulodeksīds (Wessel Due F*) sastāv no heparāna sulfāta un dermatāna sulfāta maisījuma. Sulodeksīds lielā mērā samazina Xa faktora aktivitāti, maz ietekmējot protrombīnu. Zāles palielina fibrinolītisko aktivitāti, tām ir aizsargājoša iedarbība uz asinsvadu endotēliju, un tām ir hipolipidēmiskas īpašības. Sulodeksīds ir indicēts perifēro asinsvadu slimībām ar paaugstinātu trombozes risku. Ir zāļu zāļu formas parenterālai (intravenozai un intramuskulārai) ievadīšanai un perorālai ievadīšanai.
Antitrombīns IIInepieciešami heparīna, zemas molekulmasas heparīnu un heparinoīdu antikoagulantam iedarbībai.
Iedzimta antitrombīna III deficīta gadījumā tā zāles lieto un ievada intravenozi. Ilgstoši lietojot heparīnu, palielinās antitrombīna III patēriņš, tāpēc tā koncentrācija asinīs ievērojami samazinās. Tas samazina heparīna terapijas efektivitāti. Šādos gadījumos tiek ievadīts arī antitrombīns III.
Hirudīns- proteīns ar molekulmasu 7 kDa, pirmo reizi atklāts ārstniecisko dēles siekalu dziedzeros Hirudo medicalis. Hirudīns, tāpat kā heparīns, ir antikoagulants, kas darbojas tieši asinīs, bet atšķirībā no heparīna, hirudīns tieši inhibē trombīnu: tas selektīvi saistās ar to un inaktivē to bez antitrombīna III līdzdalības. Inhibīcija ir neatgriezeniska. Atšķirībā no heparīna, hirudīnam ir spēja inhibēt ar asins recekli saistīto trombīnu un tādējādi aizkavēt asins recekļa augšanu. Hirudīns nesadarbojas ar trombocītu faktoru 4 un tāpēc neizraisa trombocitopēniju.
Klīniskajai lietošanai tika iegūts rekombinants hirudīna preparāts - le p i r u d i n * (refludan *). Ieteicams lietot, lai novērstu iespējamās trombemboliskās komplikācijas heparīna izraisītas trombocitopēnijas gadījumā. Lepirudīnu* ievada intravenozi. Lietošanas laikā var rasties asiņošana. Hirudīna preparātiem nav specifiska antidota.
Alfa drotrekogīns (Zigris*) ir rekombinants aktivēta proteīna C preparāts. Tas inhibē trombīna veidošanos, izraisot VIIIa un Va asinsreces faktoru proteolītisko inaktivāciju. Turklāt drotrekogīns palielina asins plazmas fibrinolītisko aktivitāti, samazinot asinīs cirkulējošā plazminogēna aktivatora inhibitora 1. tipa daudzumu Pretiekaisuma aktivitātes klātbūtne medikamentā ir saistīta ar tā inhibējošo iedarbību uz audzēja nekrozes faktora alfa izdalīšanos. no monocītiem. Visas šīs drotrekogīna īpašības nosaka tā efektivitāti septiskā šoka ārstēšanā (šī stāvokļa galvenie simptomi ir iekaisums un pastiprināta asins recēšana). Tāpat kā citi antikoagulanti, zāles var izraisīt hemorāģiskas komplikācijas.
Netiešie antikoagulanti
Šīs zāles, atšķirībā no heparīna, tieši neietekmē asinsreces faktorus. Tie kavē sin-
no K vitamīna atkarīgo asins plazmas olbaltumvielu sintēze aknās - II faktors (protrombīns), VII, IX un X faktori (sk. 27.-5. att.). K vitamīns ir nepieciešams funkcionāli vērtīgu faktoru veidošanai, jo darbojas kā koenzīms glutamīnskābes atlieku γ-karboksilēšanas reakcijā. Reducētā K vitamīna forma, hidrohinons, uzrāda koenzīma aktivitāti. Karboksilēšanas laikā K vitamīns-hidrohinons tiek oksidēts, veidojot neaktīvu K vitamīna epoksīdu. Netiešie antikoagulanti novērš neaktīvā K vitamīna epoksīda pārvēršanu (samazināšanu) par aktīvo K vitamīna hidrohinonu, ko veic epoksīda reduktāze un DT-diaforāze, inhibējot šos enzīmus. Tāpēc tie tiek klasificēti kā K vitamīna antagonisti (27.-6. att.).

Rīsi. 27-6.K vitamīna un netiešo antikoagulantu darbības mehānisms
Netiešie antikoagulanti uzreiz nesamazina koagulācijas faktoru koncentrāciju asinīs. Viņu darbībai raksturīgs latentais periods. Tādējādi acenokumarola antikoagulanta iedarbība sasniedz maksimālo vērtību pēc 48 stundām vai ilgāk. Šī lēnā iedarbības attīstība ir izskaidrojama ar to, ka, lietojot šīs zāles, vēl kādu laiku asinīs cirkulē pilnvērtīgi koagulācijas faktori (iedarbības rašanās ātrumu nosaka laiks, kurā koagulācijas faktori protrombīna komplekss tiek noārdīts). Netiešo antikoagulantu iedarbība ilgst apmēram 2-4 dienas, zāles spēj uzkrāties.

Netiešie antikoagulanti tiek izmantoti ilgstošai trombozes un trombembolijas profilaksei un ārstēšanai (dziļo vēnu tromboze, plaušu embolija, trombemboliskas komplikācijas priekškambaru fibrilācijas gadījumā, miokarda infarkts, sirds vārstuļu nomaiņa), ķirurģijā, lai novērstu trombu veidošanos pēcoperācijas periodā. Ienāca iekšā. Ārstēšana tiek veikta, obligāti kontrolējot protrombīna līmeni asins plazmā, nosakot protrombīna laiku - indikatoru, kura vērtība ir atkarīga no protrombīna satura asinīs un IX un X faktoriem.
Visbiežāk sastopamās komplikācijas, lietojot netiešos antikoagulantus, ir asiņošana. Asiņošanas risks palielinās, vienlaikus lietojot aspirīnu * un citus prettrombocītu līdzekļus. Lai apturētu netiešo antikoagulantu izraisītu asiņošanu, jāievada K1 vitamīna preparāti un protrombīna kompleksa koncentrāts (satur II, VII, IX un X faktorus). Iespējamas arī citas blakusparādības: alerģiskas reakcijas, caureja, aknu darbības traucējumi, ādas nekroze. Netiešie antikoagulanti grūtniecības laikā ir kontrindicēti: tie iekļūst placentā un var radīt teratogēnu efektu (traucē skeleta veidošanos, jo
kavē osteokalcīna, no K vitamīna atkarīgā kaulu proteīna, veidošanos). Fenindions (fenilīns*) var izraisīt hematopoēzes inhibīciju.
27.2.2. Asins recēšanas līdzekļi
Zāles, kas palielina asins recēšanu, tiek izmantotas, lai apturētu asiņošanu, tāpēc tās klasificē kā hemostatiskos līdzekļus (hemostatiskos līdzekļus) vai prethemorāģiskos līdzekļus. Šajā grupā ietilpst asins recēšanas faktoru veidošanai nepieciešamās vielas (K vitamīna preparāti) un paši asinsreces faktoru preparāti.
K vitamīna preparāti
K vitamīns pastāv divos veidos - K 1 vitamīns (filohinons), kas atrodams augos, un K 2 vitamīns - mikroorganismu (īpaši cilvēka zarnu mikrofloras) sintezētu savienojumu (menahinonu) grupa. K 1 un K 2 vitamīni ir taukos šķīstoši savienojumi, 2-metil-1,4-naftohinona atvasinājumi, kas atšķiras ar sānu oglekļa ķēdes garumu un raksturu. K j vitamīns tiek iegūts sintētiski, tā preparāts pazīstams kā fitomenadions. Ir sintezēts ūdenī šķīstošs K vitamīna prekursors 2-metil-1,4-naftohinons (menadions), kam piemīt provitamīna aktivitāte. Šo savienojumu nosauca par K3 vitamīnu. K 3 vitamīna atvasinājums - menadiona nātrija bisulfīts - tiek izmantots medicīnas praksē ar nosaukumu b un k a - sol *.
K vitamīns ir nepieciešams protrombīna (II faktora) un VII, IX un X asinsreces faktoru, kā arī proteīnu C un S sintēzei aknās. Zināms, ka K vitamīns piedalās kaulu audu proteīna osteokalcīna sintēzē.
Visu K vitamīna atkarīgo proteīnu struktūrai ir kopīga iezīme: šie proteīni satur γ-karboksiglutamīnskābes atlikumus, kas saista Ca 2+ jonus. K vitamīns-hidrohinons darbojas kā koenzīms glutamīnskābes atlikumu γ-karboksilēšanas reakcijā (sk. 27.-6. att.). Ar K vitamīna deficītu parādās neaktīvi asinsreces faktoru prekursori, kas nespēj saistīt Ca 2+. K vitamīna trūkums organismā visātrāk izraisa hemokoagulācijas traucējumus. Tāpēc galvenais
un agrākās K vitamīna deficīta izpausmes ir asiņošana un asiņošana.
K vitamīna preparātus lieto, lai novērstu un apturētu asiņošanu un citas hemorāģiskas komplikācijas, ko izraisa K vitamīna trūkums organismā, piemēram, jaundzimušo hemorāģiskais sindroms. K vitamīna deficītu jaundzimušajiem var izraisīt gan nepietiekama K 1 vitamīna uzņemšana, gan zarnu mikrofloras trūkums, kas sintezē K 2 vitamīnu. Lai novērstu šādas komplikācijas, jaundzimušajiem pirmajās dzīves stundās ieteicams profilaktiski ievadīt K 1 vitamīnu.
K vitamīna preparāti ir indicēti samazinātai K vitamīna uzsūkšanās zarnās dēļ traucētas žults sekrēcijas dēļ obstruktīvas dzeltes gadījumā (žults ir nepieciešama taukos šķīstošā K vitamīna uzsūkšanai) vai ar malabsorbcijas sindromu (sprue, enterokolīts, Krona slimība u.c. .)
K 1 vitamīna preparāti ir efektīvi pret asiņošanu, ko izraisa netiešie antikoagulanti. Tos ievada perorāli un intravenozi lēni.
K vitamīna preparāti var izraisīt alerģiskas reakcijas (izsitumus, niezi, eritēmu, bronhu spazmas). Ievadot intravenozi, pastāv anafilaktoīdu reakciju risks. Lietojot K 3 vitamīna preparātus (Vikasol*) jaundzimušajiem, pastāv hemolītiskās anēmijas un hiperbilirubinēmijas attīstības risks.
Asinsreces faktoru preparāti
Nepieciešamība pēc šādām zālēm rodas, ja trūkst viena vai vairāku asinsreces faktoru.
Antihemofīlais VIII asinsreces faktors (hemofils M*, imunāts* utt.) ir VIII faktora sausais koncentrāts. Zāles ir iegūtas no donora asins plazmas, kas ir pakļauta dubultai vīrusa inaktivācijai, un ir standartizētas atbilstoši VIII faktora saturam. Tie ir aktīvāki un drošāki par krioprecipitātu *.
Krioprecipitāts* ir asins plazmas proteīnu koncentrāts, kas ietver VIII faktoru, fon Vilebranda faktoru, fibronektīnu, kā arī mazākā mērā citus asinsreces faktorus un nelielu daudzumu fibrinogēna.
Zāles tiek ievadītas intravenozi iedzimta (hemofilija A) un iegūta VIII faktora deficīta gadījumā. krioprecipitāts*,
turklāt to lieto fon Vilebranda slimības (iedzimts fon Vilebranda faktora deficīts) un afibrinogēnijas aizstājterapijai. Ievadot, ir iespējamas nevēlamas blakusparādības tahikardijas, arteriālas hipotensijas, elpas trūkuma, alerģisku reakciju (nātrene, drudzis, anafilaktiskais šoks), kā arī sarkano asins šūnu hemolīzes veidā.
Visiem recēšanas faktoru preparātiem, kas iegūti no asins plazmas, ir būtisks trūkums - iespēja pārnēsāt vīrusu infekcijas (HIV, hepatītu). Šobrīd ir iegūti VIII faktora un fon Vilebranda faktora rekombinantie preparāti, kuru lietošana samazina inficēšanās risku.
Papildus koagulācijas faktora zālēm vieglām hemofilijas A formām un fon Vilebranda slimības formām izmanto arginīna vazopresīna analogu desmopresīnu. Desmopresīns palielina fon Vilebranda faktora saturu asins plazmā, veicinot tā izdalīšanos no endotēlija šūnām un palielina faktora aktivitāti
VIII. Zāles ievada parenterāli.
Asins koagulācijas faktors IX (agemfils B*, imunīns*, oktanīns*) ir attīrīta cilvēka plazmas frakcija, kas bagātināta ar IX faktoru. Lieto pie iedzimta (hemofilija B) un iegūta IX faktora deficīta, kā arī pie netiešo antikoagulantu pārdozēšanas. Blakusparādības ir tādas pašas kā VIII faktora zālēm.
Alfa aktivētais eptakogs (novoseven *) ir rekombinants VIIa asinsreces faktors. Lieto VII faktora un citu koagulācijas faktoru (V, II,
IX, X).
Lokāli, lai apturētu asiņošanu no mazajiem kapilāriem un parenhīmas orgāniem, tiek izmantots medikaments trombīns (iegūst no donora asins plazmas), kā arī hemostatiskie sūkļi (kolagēns, želatīns).
Dzemdes, plaušu, nieru, zarnu un citu asiņošanu apturēšanai izmanto ārstniecības augu preparātus: nātru lapas, pelašķu zālīti, piparmētru lakstaugu, vīgriezes zālīti, irbenes mizu, arnikas ziedus, reibinošo lāgotiņu. Ārstniecības augus lieto uzlējumu, tinktūru un ekstraktu veidā iekšēji un lokāli.
27.3. ZĀLES, KAS IETEKMĒ FIBRINOLĪZI
Kad veidojas asins recekļi, tiek aktivizēta fibrinolītiskā sistēma, kas nodrošina fibrīna izšķīšanu (līzi) un asins recekļa iznīcināšanu. Tas noved pie normālas asinsrites atjaunošanas.
Fibrinolīzes procesā neaktīvais plazminogēns tiek pārveidots par plazmīnu (fibrinolizīnu), piedaloties plazminogēna aktivatoriem. Plazmīns hidrolizē fibrīnu, veidojot šķīstošus peptīdus. Plazmīnam nav specifiskuma, kā arī tas izraisa fibrinogēna un dažu citu asinsreces faktoru iznīcināšanu, kas palielina asiņošanas risku. Asinīs cirkulējošo plazmīnu ātri inaktivē α 2 -antiplazmīns un citi inhibitori, un tāpēc tam parasti nav sistēmiskas fibrinogenolītiskas iedarbības. Tomēr noteiktos patoloģiskos apstākļos vai fibrinolītisko līdzekļu lietošanas gadījumā ir iespējama pārmērīga plazminogēna aktivācija, kas var izraisīt asiņošanu.
27.3.1. Fibrinolītiskie (trombolītiskie) līdzekļi
Fibrinolītiskos līdzekļus izmanto, lai izšķīdinātu asins recekļus koronārās trombozes (akūta miokarda infarkta), dziļo vēnu trombozes, akūtas perifēro artēriju trombozes un plaušu embolijas gadījumā.
Kā fibrinolītiskos līdzekļus izmanto zāles, kas aktivizē plazminogēnu: streptokināzes zāles, audu plazminogēna aktivatora zāles, urokināzes zāles.
Streptokināzes zāles
Streptokināze (kabikināze *) ir ļoti attīrīts olbaltumvielu preparāts, kas iegūts no β-hemolītiskā streptokoka kultūras. Streptokināze iegūst proteolītisko aktivitāti tikai kombinācijā ar plazminogēnu. Ievadot streptokināzi, veidojas ekvimolārs streptokināzes-plazminogēna komplekss, kas pārvērš plazminogēnu par plazmīnu. Streptokināze iedarbojas uz plazminogēnu gan asins receklī, gan asins plazmā (27.-7. att.).
Streptokināzi ievada intravenozi akūta miokarda infarkta gadījumā, ko izraisa koronāro asinsvadu tromboze (vairums
efektīvas pirmās 3-6 stundas), dziļo vēnu trombozes, plaušu embolijas un tīklenes asinsvadu trombozes gadījumā. Streptokināzi ievada ME (starptautiskajās vienībās).
Biežas komplikācijas, lietojot streptokināzi, ir asiņošana, kas var būt saistīta gan ar asinīs cirkulējošā plazminogēna aktivāciju (iegūtais plazmīns iznīcina fibrinogēnu, kā rezultātā samazinās trombocītu agregācija), gan ar fizioloģisko asins recekļu izšķīšanu. Iespējama slikta dūša, vemšana un arteriāla hipotensija. Pateicoties antigēnu īpašību klātbūtnei, streptokināze var izraisīt alerģiskas reakcijas, tostarp anafilaktisku šoku. To bīstamība palielinās, atkārtoti lietojot zāles. Asinīs cirkulējošās antivielas var inaktivēt streptokināzi un samazināt terapijas efektivitāti.
Anistreplāze** (emināze**) ir streptokināzes komplekss ar acilētu lizīna plazminogēnu. Acilgrupa plazminogēna molekulā aizver katalītisko vietu, kas novērš plazminogēna aktivāciju. Zāles ir priekšzāles un iegūst spēju pārvērst plazminogēnu plazmīnā tikai pēc acilgrupas šķelšanās. Deacilācijas ātrums un līdz ar to arī aktīvās zāles veidošanās laiks ir atkarīgs no acilgrupas rakstura un var svārstīties no 40 minūtēm līdz vairākām stundām. Anistreplase** ievada intravenozi. Pēc vienas injekcijas fibrinolītiskais efekts saglabājas 4-6 stundas. Lietošanas indikācijas un blakusparādības ir tādas pašas kā streptokināzei.
Audu plazminogēna aktivatora un urokināzes preparāti
Audu plazminogēna aktivators un urokināze ir galvenie fizioloģiskie plazminogēna aktivatori.
Audu plazminogēna aktivatoru ražo endotēlija šūnas. Tas izraisa daļēju plazminogēna proteolīzi, kā rezultātā tas tiek pārveidots par plazmīnu. Audu aktivatora atšķirīga iezīme ir tā augstā afinitāte pret fibrīnu, kas simtiem reižu paātrina tā ietekmi uz plazminogēnu. Rezultātā audu aktivators ar lielāku ātrumu aktivizē tās plazminogēna molekulas, kas adsorbējas uz fibrīna pavedieniem. Tādējādi audu plazminogēna aktivatora darbību ierobežo trombu fibrīns. Nokļūstot asinsritē,

Rīsi. 27-7.Fibrinolītisko līdzekļu darbības mehānisms: tPA - audu plazminogēna aktivators; FDP - fibrinogēna sadalīšanās produkti; EK - endotēlija šūna; ? - aktivizēšana; Θ - līze
audu aktivators saistās ar specifisku inhibitoru, tāpēc tas maz ietekmē asinīs cirkulējošo plazminogēnu un mazākā mērā samazina fibrinogēna līmeni.
Klīniskajai lietošanai iegūti audu plazminogēna aktivatora rekombinantie preparāti: alteplāze (actilyse *) un tenekteplāze (metalise *). Zāles ievada intravenozi akūta miokarda infarkta, ko izraisa koronāro asinsvadu tromboze (iedarbojas pirmajās 6-12 stundās), plaušu embolijas gadījumā. Neskatoties uz to, ka alteplāzei ir maza ietekme uz plazminogēnu, kas cirkulē asinīs, tās lietošanas laikā bieži rodas hemorāģiskas komplikācijas. Tam nav antigēnu īpašību. Tenekteplāzei ir paaugstināta trombu fibrīna specifiskums.
Urokināzi ražo nieru šūnas, un tā ir atrodama urīnā. Nierēs veidojas vienas ķēdes urokināze (prourokināze), kas plazmīna ietekmē pārvēršas aktīvajā formā - dubultķēdes urokināze. Divkāršās ķēdes urokināzei ir tieša aktivizējoša iedarbība uz plazminogēnu (kompleksa veidošana ar plazminogēnu nav nepieciešama). Divkāršās ķēdes urokināzes preparātu iegūst no cilvēka embrija nieru šūnu kultūras. Lieto pie akūta miokarda infarkta, vēnu un artēriju trombozes, plaušu embolijas. Ievadīts intravenozi. Dozēts ME. Salīdzinot ar audu plazminogēna aktivatoru, urokināze lielākā mērā iedarbojas uz asinīs cirkulējošo plazminogēnu, kā rezultātā asinīs izveidojies plazmīns izraisa fibrinogēna sadalīšanos (sk. 27.-7. att.). Tajā pašā laikā samazinās trombocītu agregācija un veidojas fibrinogēna sadalīšanās produkti, kuriem ir antikoagulanta aktivitāte. Galvenās blakusparādības ir asiņošana. Nav antigēnu īpašību.
Tika iegūts vienas ķēdes urokināzes (prourokināzes) rekombinants preparāts - c a p u p l a z a *, kas uzrāda lielāku specifiskumu trombu fibrīnam nekā urokināzei.
27.3.2. Antifibrinolītiskie līdzekļi
Antifibrinolītiskos līdzekļus lieto, lai apturētu asiņošanu, ko izraisa palielināta fibrinolītiskās sistēmas aktivitāte traumu, ķirurģisku iejaukšanos, dzemdību laikā,
aknu slimības, prostatīts, menorāģija, kā arī fibrinolītisko zāļu pārdozēšana. Šiem nolūkiem tiek izmantotas zāles, kas inhibē plazminogēna aktivāciju vai ir plazmīna inhibitori.
Aminokaproīnskābe saistās ar plazminogēnu un novērš tā pārvēršanos par plazmīnu. Turklāt tas traucē plazmīna ietekmi uz fibrīnu. Zāles lieto iekšķīgi un intravenozi. Iespējamās blakusparādības: arteriāla hipotensija, bradikardija, aritmijas, reibonis, slikta dūša, caureja. Aminometilbenzoskābei (Ambene*, Pamba*) ir līdzīga iedarbība.
Traneksamskābe (traneksāms*, ciklokaprons*) kavē plazminogēna aktivāciju. Zāles lieto iekšķīgi un intravenozi. Tas ir efektīvāks par aminokaproīnskābi un ilgst ilgāk. Blakusparādības ir dispepsijas simptomi (anoreksija, slikta dūša, vemšana, caureja), reibonis, miegainība; Iespējamas alerģiskas ādas reakcijas.
Aprotinīns (Gordox*, Contrical*, Trasylol*, Ingitril*) inhibē plazmīnu un citus proteolītiskos enzīmus. Zāles ievada intravenozi. Blakusparādības: arteriāla hipotensija, tahikardija, slikta dūša, vemšana, alerģiskas reakcijas.
Trombocīti, mazākās asins šūnas (salīdzinot ar leikocītiem un sarkanajiem asinsķermenīšiem), veic vissvarīgāko funkciju – aizsargā organismu no asins zuduma. Trombocītu agregācija ir šūnu salipšanas process, asins recekļu veidošanās sākuma stadija.
Otrais posms ir trombocītu piestiprināšana pie bojātā trauka sienas. Fibrīna pavedieni, citi elementi un jaunas pielipušās šūnas tiek uzklātas uz trombocītu masas. Tādējādi trombs aug līdz tādam izmēram, kas spēj bloķēt trauka diametru un apturēt asiņošanu. Dažreiz cilvēka dzīve ir atkarīga no procesa ātruma.
Trombocītu agregācijas loma asins recēšanas procesā
Asins sarecēšana ir atkarīga no daudziem faktoriem. Vienai no tām, trombocītu agregācijai, veselā organismā ir aizsargājošs adaptīvs raksturs. Šūnas salīp kopā tikai asiņojošā traukā. Šajā gadījumā procesam ir pozitīva loma.
Bet ir zināmi patoloģiski stāvokļi, kuros asins recekļu veidošanās nav vēlama, jo tas izraisa svarīgu orgānu uztura traucējumus. Piemēram, ar miokarda infarktu, insultu, vadošo artēriju trombozi. Trombocītu agregācijas aktivitāte ir saistīta ar patoloģiskām izmaiņām. Pret to jācīnās ar dažādu medikamentu palīdzību.
Ir praktiski nepieciešams kvantitatīvi noteikt labo un slikto trombocītu agregāciju. Lai to izdarītu, jums ir jāizmanto norma un jānošķir novirzes.
Kā noteikt normu un patoloģiju?
Vai asins analīzes var parādīt konkrētas personas trombocītu agregācijas spēju? Galu galā, lai veiktu pētījumu, asinis tiek ņemtas no vēnas, un no šī brīža ķermeņa “pasūtījumi” nedarbojas uz asins šūnām. Šāda veida analīzi sauc par "in vitro", kas ir burtisks tulkojums no latīņu valodas "uz stikla, mēģenē". Zinātnieki vienmēr cenšas izpētīt reakciju apstākļos, kas ir tuvu cilvēka ķermenim. Tikai šādā veidā iegūtos datus var uzskatīt par ticamiem un izmantot diagnostikā.
Trombocītu spējas nosaka inducētā agregācija. Tas nozīmē, ka kā induktora viela tiek izmantotas vielas, kuras ķīmiskajā sastāvā nav svešas organismam un var izraisīt asins recekļu veidošanos. Kā induktori tiek izmantoti asinsvadu sieniņu komponenti: adenozīna difosfāts (ADP), ristocetīns (ristomicīns), kolagēns, serotonīns, arahidonskābe, adrenalīns.
Spontānu agregāciju nosaka bez induktoriem.
Kvantitatīvās noteikšanas metodes ir balstītas uz gaismas viļņu izvadīšanu cauri ar trombocītiem bagātinātu asins plazmu. Agregācijas aktivitātes pakāpi pēta pēc plazmas gaismas blīvuma starpības pirms koagulācijas sākuma un pēc maksimālā rezultāta iegūšanas. Tiek noteikts arī agregācijas ātrums pirmajā minūtē, viļņu raksturs un forma.
Ātrums ir atkarīgs no induktora vielas un tās koncentrācijas.
Trombocītu agregāciju ar ADP parasti izraksta un novērtē kombinācijā ar kolagēnu, ristomicīnu un adrenalīnu.
Analīzes ar ADP norma ir no 30,7 līdz 77,7%. Trombocītu agregācijas apjoms ar adrenalīnu svārstās no 35 līdz 92,5%. Pētījumā ar kolagēnu normālās vērtības tiek uzskatītas par no 46,4 līdz 93,1%.
Noteikumi, kā sagatavoties analīzei
Lai veiktu asins analīzi par agregācijas spēju, jums jāsaprot, ka pārbaude būs neprecīza, ja tiks pārkāpti sagatavošanas noteikumi. Asinīs būs vielas, kas ietekmē rezultātu.
- Nedēļu pirms asins nodošanas jāpārtrauc visu aspirīna zāļu, dipiridamola, indometacīna, sulfapiridazīna un antidepresantu lietošana. Šo zāļu lietošana kavē (nomāc) trombu veidošanos. Ja nevarat pārtraukt tā lietošanu, jums par to jāinformē laboratorijas tehniķis.
- Jūs nedrīkstat ēst vismaz 12 stundas, jo īpaši tavus rezultātus ietekmē taukaini ēdieni.
- Pacientam jābūt pēc iespējas mierīgākam un nedrīkst veikt fizisku darbu.
- Dienu iepriekš izslēdziet no ēdiena kafiju, alkoholu, ķiplokus un nesmēķējiet.
- Analīze netiek veikta, ja ir aktīvs iekaisuma process.
Zem mikroskopa ir redzami salipuši trombocīti
Asins analīzi trombocītu agregācijas noteikšanai nosaka ārsts, ja nepieciešama ārstēšana ar antikoagulantiem, kontrolējot to efektivitāti, izvēloties optimālo devu, lai diagnosticētu pastiprinātu asiņošanu.
Rezultātu atšifrēšana
Iemesli pētījumu veikšanai ar trim standarta induktoriem vienlaikus un, ja nepieciešams, jaunu pievienošanai, ir dominējošais viena no koagulācijas faktoru aktivizācijas mehānisms. Identificētajai izmainītajai normai, piemēram, ar ADP, ja nav dinamikas ar citiem induktoriem, ir diagnostiska nozīme. Rezultātus novērtē ārsts.
Trombocītu agregācijas samazināšanos var izraisīt:
- veiksmīga prettrombocītu terapijas izmantošana;
- slimību grupa, ko sauc par trombocitopātijām.

Agregācijas analīzes aparāti
Trombocitopātijas loma
Trombocitopātijas var būt iedzimtas vai iegūtas citu slimību rezultātā. Statistika saka, ka līdz 10% planētas iedzīvotāju cieš no šīs patoloģijas. Tie visi ir saistīti ar trombocītu darbības traucējumiem noteiktu vielu uzkrāšanās laikā.
Tā rezultātā nenotiek koagulācija un asins recekļu veidošanās, kas izraisa pastiprinātu asiņošanu mazās brūcēs un sasitumus (iekšēja asiņošana).
Slimības parādās jau bērnībā ar smaganu asiņošanu, biežu deguna asiņošanu, daudziem sasitumiem uz bērna ķermeņa, locītavu pietūkumu sasitumu dēļ. Pubertātes laikā meitenēm sākas ilgstošas un smagas menstruācijas. Asiņošana izraisa anēmijas (anēmijas) attīstību.
Zemu agregācijas spēju trombocitopātijā var aktivizēt vīrusu un baktēriju infekcijas, medikamenti un fizioterapeitiskās procedūras.

Deguna asiņošanu 80% gadījumu izraisa trombocitopātija un tikai 20% - LOR orgānu slimības.
Sekundārās trombocitopātijas
Simptomātiskas (sekundāras) trombocitopātijas veidojas hroniskas leikēmijas, mielomas,. Šis stāvoklis ir raksturīgs nieru mazspējas (urēmijas) beigu stadijai, pavājinātai vairogdziedzera darbībai.
Ķirurgi saskaras ar trombocitopātijām, ja ķirurģiskas iejaukšanās laikā ir pastiprināta asiņošana.
Trombocītu agregācijas palielināšanās tiek novērota ar:
- plaši izplatīta asinsvadu ateroskleroze;
- hipertensija;
- iekšējo orgānu infarkts;
- vēdera artēriju tromboze;
- insults;
- cukura diabēts
Agregācijas izmaiņas grūtniecības laikā
Trombocītu agregācija grūtniecības laikā var atšķirties no normālām vērtībām.
Agregācija tiek samazināta nepietiekamas trombocītu ražošanas vai to kvalitatīvā sastāva pārkāpuma dēļ. Tas izpaužas kā asiņošana un zilumi. Dzemdību laikā jārēķinās ar masīvas asiņošanas iespējamību.
Agregācija tiek palielināta visbiežāk toksikozes laikā, jo vemšanas un caurejas rezultātā rodas šķidruma zudums. Koncentrācijas palielināšanās asinīs izraisa palielinātu trombu veidošanos. Tas var izraisīt agrīnu abortu. Mērena hiperagregācija tiek uzskatīta par normālu grūtniecības laikā un ir saistīta ar placentas asinsrites attīstību.
- spontāna aborta gadījumā;
- neauglības ārstēšana;
- pirms kontracepcijas līdzekļu lietošanas un tās laikā;
- pirms plānotās grūtniecības.
Trombocītu agregācijas īpašību analīze ļauj identificēt riskus, paredzēt bīstamas komplikācijas slimību laikā un operatīvi veikt profilaktisko terapiju.
Trombocīti ir asins šūnas, kurām nav krāsas. Tie veic svarīgu funkciju organismā, pasargājot to no asins zuduma. Šis process ir trombocītu agregācija asinīs, tam ir savi standarta rādītāji.
Lai saprastu, kas tas ir, jums ir nepieciešams priekšstats par asins recekļa veidošanos, esošajiem standartiem un novirzēm no normālām vērtībām.
Apraksts un loma cilvēka organismā
Pēc audu traumas trombocīti piestiprinās pie bojātā trauka sienām. Tā rezultātā šūnas salīp kopā. Laika gaitā iegūtajai masai pievieno fibrīna pavedienus, jaunas līmētās šūnas un citus elementus.
Uz šī fona aug asins receklis, kas sasniedz lielus izmērus, kas var izraisīt kuģa bloķēšanu un asiņošanas apturēšanu. Šāda procesa ātrums ir ļoti svarīgs, jo no tā dažreiz ir atkarīga cilvēka dzīvības saglabāšana.

Asins recēšanu ietekmē liels skaits faktoru. Viens no tiem ir apkopošana. Ja nav patoloģisku stāvokļu, tas veic aizsargājošu adaptīvo funkciju.
Agregācijas pazīmes sastāv no šūnu līmēšanas tikai bojātajā traukā. Šajā gadījumā process tiek uzskatīts par pozitīvu.
.jpg)
Tomēr ir situācijas, kad tromboze ir nevēlama. Piemēram, ja tiek diagnosticēts insults vai miokarda infarkts.
Tas izskaidrojams ar to, ka asins recekļu veidošanās novērš normālu nepieciešamo vielu plūsmu uz dzīvībai svarīgiem orgāniem.
Šajā gadījumā trombocīti ieņem patoloģisko procesu pusi. Atkāpes no normas var tikt galā tikai ar medikamentu palīdzību.
Lai noteiktu normālu no neparastiem rādītājiem, ir nepieciešams veikt pozitīvās un negatīvās agregācijas kvantitatīvo analīzi.
Veidi
Medicīnas praksē ir noteikta summēšanas klasifikācija pēc veida. Tie ietver:

- Mērens apkopojums. Tas tiek diagnosticēts galvenokārt grūtniecības laikā. Stāvokli var izraisīt placentas cirkulācija.
- Spontāna agregācija. Atklāšanai nav nepieciešams induktors. Lai noteiktu agregācijas aktivitāti, asinis ielej mēģenē, kuru ievieto speciālā ierīcē, kur tās uzkarsē līdz 37 grādiem.
- Inducēta agregācija. Lai veiktu pētījumu, plazmai pievieno induktorus. Šajā gadījumā agregācija notiek ar ADP, kolagēnu, ristomicīnu un adrenalīnu. Šo metodi izmanto gadījumos, kad nepieciešams diagnosticēt noteiktas asins šķidruma patoloģijas.
- Paaugstināta agregācija veicina asins recekļu veidošanos. Šī patoloģiskā stāvokļa raksturīgie simptomi ir nejutīgums un pietūkums.
- Samazināta agregācija visbiežāk tiek konstatēta asinsrites sistēmas darbības traucējumu gadījumos. Trombocītu skaita samazināšanās izraisa dažādas asiņošanas. Tas notiek daiļā dzimuma pārstāvjiem menstruālā cikla laikā.
Gan palielināta, gan samazināta agregācija ir bīstama cilvēka veselībai. Tādēļ regulāri jākontrolē trombocītu līmenis asinīs.
Simptomi novirzēm no rādītājiem
Hiperagregāciju pavada paaugstināta asins viskozitāte un tās plūsmas ātruma samazināšanās, kas negatīvi ietekmē visas cilvēka sistēmas un orgānus.
Tomēr ir patoloģiski stāvokļi, kad izteikta agregācija ir normāla parādība, kas savukārt netiek uzskatīta par iemeslu atteikties no pastāvīgas koagulācijas parametru izpētes.
Šādas slimības ietver:
- paaugstināts asinsspiediens;
- cukura diabēts;
- vēzis;
- asinsvadu patoloģijas.
Savlaicīga hiperagregācijas atklāšana un palīdzības trūkums var izraisīt sirdslēkmes, insulta un vēnu trombozes attīstību.
Agregācijas rādītāju samazināšanos pavada ilgstoša asiņošana, tai skaitā iekšēja asiņošana, kas izpaužas kā hematomu veidošanās.
Kāda ir norma
Trombocītu līmeņa normas pieaugušajam un bērnam būs nedaudz atšķirīgas. Rādītāju optimālās vērtības ir parādītas tabulā zemāk.
Ja mēs runājam par normālām summēšanas vērtībām, tad tie būs 25-75 procenti. Šajā gadījumā trombocīti turas kopā bez novirzēm un nerada draudus cilvēka ķermenim.
Kādi pētījumi tiek veikti?
Trombocītu agregācijas analizators ir pilnīga asins aina. Tomēr ir arī citi pētījumi, kas sniedz precīzākus rezultātus. Galvenās metodes ietver šādus testus:
.jpg)
- saskaņā ar Lī-Vaitu;
- koagulogramma.
To būtība slēpjas faktā, ka asinīm tiek pievienotas īpašas vielas, kas kavē agregāciju.
Šīs sastāvdaļas ir līdzīgas cilvēka organismā esošajām vielām, kas izraisa asins recekļu veidošanos. Šādas sastāvdaļas sauc par induktoriem.
Gatavošanās analīzei
Pirms analīzes veikšanas jums ir jāveic noteikta sagatavošanās. Lai rezultāti būtu pēc iespējas precīzāki, asins šķidrums nedrīkst saturēt vielas, kas to varētu negatīvi ietekmēt.
Sagatavošanas pasākumi:
- Nedēļu pirms analīzes daži aspirīna medikamenti tiek izslēgti, jo to lietošana nomāc trombu veidošanos. Ja šīs zāles nav iespējams atcelt, par to jāinformē laboratorijas tehniķis, kas veic pētījumu.
- Jums jāpārtrauc ēst 12 stundas. Produkti, īpaši tie ar augstu tauku saturu, arī negatīvi ietekmē rezultātus.
- Izvairieties no fiziska un emocionāla stresa.
- Dienas laikā nelietojiet alkoholiskos dzērienus, kafiju, ķiplokus un nesmēķējiet.
Analīze tiek atlikta, ja ir aktīvs iekaisuma process.
Veicot
Asins paraugu ņemšana tiek veikta no rīta, no pulksten 7 līdz 10. Pētījumu var veikt tikai tukšā dūšā. Ir atļauts dzert negāzētu ūdeni.
Lai veiktu hemotestu, asins šķidrums tiek ņemts no vēnas. Šiem nolūkiem tiek izmantota vienreizējās lietošanas šļirce. Pēc tam materiālu ievieto agregometrā, kas satur 4% nātrija citrāta šķīdumu. Pēc tam trauku vairākas reizes apgriež. Pēc tam asiņu caurule tiek nosūtīta uz laboratoriju turpmākai pārbaudei.
Rezultātu atšifrēšana
Ņemot vērā pētījuma laikā izmantoto vielu, analīze tiek atšifrēta. Lai to izdarītu, iegūtos rādītājus salīdzina ar parastajām vērtībām, kas ir norādītas zemāk.
Ja tiek novērots pieaugums salīdzinājumā ar normu, tiek diagnosticēta hiperagregācija. Tas var rasties tādos patoloģiskos apstākļos kā:
.jpg)
- leikēmija;
- kuņģa-zarnu trakta vai nieru patoloģijas;
- ateroskleroze;
- cukura diabēts;
- augsts asinsspiediens;
- sepse;
- limfogranulomatoze.
Ja novirzes ir uz leju, tiek diagnosticēta hipoagregācija. To var izraisīt asins patoloģijas vai ārstēšana ar prettrombocītu līdzekļiem.
Procenti parāda plazmas gaismas caurlaidības līmeni pēc tam, kad tai ir pievienota induktora viela. Ja trombocītu skaits ir zems, šis skaitlis ir 100 procenti, un, ja tas ir augsts, tas ir nulle.
Agregācijas pazīmes grūtniecēm
Grūtniecības laikā ir pieļaujamas novirzes no normas, kas šajā periodā svārstās no 30 līdz 60 procentiem.
Dezagregāciju var novērot, ja ir trombocītu trūkums, kā arī, ja ir izmaiņas to kvalitatīvajā sastāvā, kas izpaužas ar asiņošanu un zilumiem.
Paaugstināta agregācija rodas toksikozes laikā, kad pacientam vemšanas vai caurejas rezultātā rodas liels šķidruma zudums. Koncentrācijas palielināšanās asinīs izraisa pastiprinātu asins recekļu veidošanos. Tas apdraud agrīnu abortu.
Kā jūs varat normalizēt vērtības?
Ja tiek diagnosticēti asinsreces traucējumi, nekavējoties jāveic pasākumi, lai novērstu patoloģisko stāvokli. Agregācijas palielināšanās var izraisīt trombozi, un samazināšanās var izraisīt smagu un bīstamu asiņošanu.
Hiperagregācijas attīstības sākumposmā speciālisti izraksta zāles, kas var šķidrināt asinis. Regulārais aspirīns var tikt galā ar uzdevumu.
Pamatojoties uz papildu pārbaudes rezultātiem, bieži tiek noteikts:
.jpg)
- pretsāpju līdzekļi;
- novokaīna blokāde;
- zāles, kas veicina vazodilatāciju;
- antikoagulanti, kas novērš ātru recēšanu.
Dažreiz tradicionālās metodes ir ne mazāk efektīvas. Ir vērts atcerēties, ka šāda ārstēšana ir jāsaskaņo ar ārstējošo ārstu.
Starp pārbaudītajām receptēm ir šādas:
- Vienu ēdamkaroti saldā āboliņa ielej 200 ml vārīta ūdens un ļauj ievilkties 30 minūtes. Sagatavoto maisījumu lietojiet dienā vairākās devās. Terapijas kurss ir viens mēnesis.
- Uzvāriet pusotru litru verdoša ūdens vienādos daudzumos (tējkarote) ingvera un zaļās tējas. Pievieno šķipsniņu kanēļa. Atstāj uz ceturtdaļu stundas un ņem visu dienu.
- Katru dienu dzeriet svaigi spiestu apelsīnu sulu. Var sajaukt vienādās daļās ar ķirbi.
Ir svarīgi arī uzturēt pareizu uzturu. Diētā jāiekļauj:
- citrusaugļi;
- ingvers;
- ķiploki;
- sarkanie un zaļie dārzeņi;
- jūras veltes.
Ja jums ir slikta asins recēšana, jūs nedrīkstat lietot zāles. kas atšķaida asins šķidrumu. Ja procesa gaita ir ieguvusi progresīvu formu, tad terapeitiskie pasākumi tiek veikti tikai stacionāros apstākļos.
Ir parakstītas šādas zāles:

- Emosints;
- aminokapronskābe un traneksāmskābe;
- ATP injekcija;
Uzturā jāiekļauj griķu biezputra, olas, bietes un burkāni, granātāboli, liellopu aknas un sarkanā gaļa.
Lai uzturētu asinis normālā stāvoklī, ir stingri jāievēro dzeršanas režīms. Par normu dienā tiek uzskatīts vismaz pusotrs litrs tīra ūdens. Pārtikai jābūt svaigai un sabalansētai.
Uztura noteikumu ievērošana ir daudzu cilvēka ķermeņa slimību profilakse. Tikpat svarīga loma ir arī fiziskajām aktivitātēm. Tie palīdz ne tikai stiprināt ķermeni, bet arī normalizēt visus iekšējos procesus.
Savlaicīgi diagnosticējot summēšanas rādītāju novirzes, var novērst daudzas slimības un komplikācijas. Regulāri jāuzrauga trombocītu agregācijas līmenis.
Trombocīti ir mazas asins šūnas, kas ir atbildīgas par asins recēšanu. Tie palīdz apturēt asins zudumu asiņošanas gadījumā.
Kad rodas brūce, trombocīti pārvietojas uz ievainoto vietu. Šeit tie ir piestiprināti pie bojātā trauka sienas, kā rezultātā asiņošana apstājas. Šo procesu sauc par trombocītu agregāciju.
Trombocītu agregācija ir process, kurā asins šūnas saķeras viena ar otru un nostiprina tās uz ievainotā trauka sienas. Tas aptur asiņošanu. Taču šāds process var būt arī bīstams organismam. Šajā gadījumā veidojas asins receklis, kas noteiktos apstākļos var izraisīt sirdslēkmi un insultu. Tas var notikt, ja trombocīti ir pārāk aktīvi un agregācija notiek pārāk ātri.
Turklāt lēnais process arī nesola neko labu organismam. Šajā gadījumā lēnas trombocītu adhēzijas dēļ var rasties slikta asins recēšana. Šī patoloģija izraisa anēmiju. Ja asins recēšana ir slikta, ir grūti apturēt asiņošanu, kas var izraisīt veselības problēmas un pat nāvi. Lai tas nenotiktu, ir jāuzrauga trombocītu līmenis asinīs un to spēja salipt kopā.
Trombocītu agregācijas process grūtniecības laikā
 Ir ārkārtīgi svarīgi, lai grūtniecības laikā trombocītu agregācija noritētu normāli. Ja process notiek pārāk lēni, tad dzemdību laikā vai pēcdzemdību periodā var rasties asiņošana no dzemdes, kas var izraisīt sievietes nāvi. Turklāt, ja grūtniecības laikā trombocītu agregācija notiek ātri, var veidoties asins recekļi, kas grūtniecības laikā var izraisīt tās pārtraukšanu jebkurā stadijā.
Ir ārkārtīgi svarīgi, lai grūtniecības laikā trombocītu agregācija noritētu normāli. Ja process notiek pārāk lēni, tad dzemdību laikā vai pēcdzemdību periodā var rasties asiņošana no dzemdes, kas var izraisīt sievietes nāvi. Turklāt, ja grūtniecības laikā trombocītu agregācija notiek ātri, var veidoties asins recekļi, kas grūtniecības laikā var izraisīt tās pārtraukšanu jebkurā stadijā.
Jūs varat izvairīties no šīs situācijas, ja plānojat grūtniecību un rūpēsieties par savu veselību iepriekš. Jau pirms ieņemšanas ir jānoskaidro, kādā stāvoklī atrodas trombocīti, un, ja nepieciešams, jāveic pasākumi situācijas labošanai. Ja grūtniecība nebija plānota, tad no agregācijas patoloģijas var izvairīties, reģistrējoties agrīnā stadijā. Tad ārsts izrakstīs nepieciešamās pārbaudes un palīdzēs atbrīvoties no trombocītu patoloģiskā stāvokļa, ja tāds tiks atklāts.
Normāls trombocītu skaits asinīs
Lai uzzinātu trombocītu līmeni, jums ir nepieciešams priekšstats par to normālo līmeni.
Ja runājam par summēšanas koeficientu, tad tas ir 25-75%. Šajā gadījumā trombocītu līmēšanas process norit labi un nerada nekādu apdraudējumu veselībai.
Ja tiek novērotas novirzes no normas, tiek noteikta atbilstoša ārstēšana, kas palīdzēs labot situāciju.Asins analīze trombocītu agregācijai
Asins analīze, ko sauc par inducētu agregāciju, palīdz izpētīt trombocītu stāvokli. Šajā gadījumā asinis tiek ņemtas no pacienta vēnas un sajauktas ar īpašām vielām. Šādu līdzekļu sastāvs ir līdzīgs to ķermeņa šūnu sastāvam, kas piedalās agregācijas procesā. Par induktoriem visbiežāk tiek izmantotas šādas vielas:
- adenozīna difosfāts (ADP);
- kolagēns;
- serotonīns;
- ristocetīns;
- adrenalīns;
- arahidonskābe.
Visbiežāk veiktā procedūra ir trombocītu agregācija ar ADP. Lai veiktu pētījumu, tiek ņemta īpaša ierīce. To sauc par trombocītu agregācijas analizatoru. Ar tās palīdzību gaismas viļņi tiek izvadīti cauri asinīm, pirms tās sāk sarecēt un pēc šī procesa pabeigšanas. Pēc tam tiek novērtēts rezultāts.
Gatavošanās testiem
 Lai rezultāts būtu pēc iespējas precīzāks, jums jāievēro šādi asins analīzes noteikumi:
Lai rezultāts būtu pēc iespējas precīzāks, jums jāievēro šādi asins analīzes noteikumi:
- Pētījums tiek veikts tukšā dūšā. Šajā gadījumā jums jāpārtrauc ēšana 12 stundas pirms testa. Šajā gadījumā varat dzert tīru negāzētu ūdeni.
- 7 dienas pirms testa jums jāpārtrauc zāļu lietošana ar noteiktiem medikamentiem. Ja tas nav iespējams, jums par to jāinformē ārsts, kurš veic analīzi.
- Dažas dienas pirms analīzes jums vajadzētu izvairīties no stresa situācijām un fiziskām aktivitātēm.
- 24 stundas iepriekš jāpārtrauc kafijas lietošana, smēķēšana, alkohola un ķiploku lietošana.
- Pētījumus nevar veikt, ja organismā notiek iekaisuma process.
Indikācijas analīzei
 Jūs varat laiku pa laikam veikt trombocītu agregācijas testu pēc savas iniciatīvas.
Jūs varat laiku pa laikam veikt trombocītu agregācijas testu pēc savas iniciatīvas. Inducētās agregācijas analīzes rezultāta interpretācija
Rādītāju interpretācija ir atkarīga no līdzekļiem, ar kādiem pētījums tika veikts. Lai to izdarītu, dati tiek salīdzināti ar normu.
Ja rezultāti novirzās no normas uz augšu, tad tiek diagnosticēta pastiprināta trombocītu agregācija. Šis nosacījums rodas, ja: 
- augsts asinsspiediens;
- ateroskleroze;
- leikēmija;
- cukura diabēts;
- kuņģa-zarnu trakta vai nieru onkoloģiskās slimības;
- limfogranulomatoze;
- sepse;
- ķirurģiska liesas noņemšana.
Paaugstināta trombocītu agregācija var izraisīt sirdslēkmi, insultu, trombozi un nāvi, jo asins receklis bloķē asinsvadu.
Ja rezultāti novirzās no normas uz samazināšanos, tad tiek diagnosticēta samazināta trombozes agregācija. Tas ir saistīts ar:
- asins slimības;
- trombocitopātija;
- antitrombocītu līdzekļu lietošana.
Samazinoties agregācijai, trauki kļūst trausli. Turklāt asiņošanas apturēšanas process ir grūts, kas var izraisīt nāvi.
Līdzekļi, kas samazina agregācijas procesu
Daži līdzekļi kavē agregācijas procesu. Šīs zāles ietver prettrombocītu līdzekļus. Trombocītu agregācijas inhibitori ietver tādas zāles kā acetilsalicilskābe, ibustrīns, mikristīns un citi. Šādas zāles ir paredzētas noteiktu slimību ārstēšanai. Tomēr, ja agregācijas process krasi novirzās no normas, inhibitoru zāles jāaizstāj ar citiem līdzekļiem, kas neizraisa šādas sekas. Ja tas nav iespējams, ārsts var izrakstīt īpašas zāles, kas veicina agregāciju.
Gan palielināta, gan samazināta agregācija var izraisīt briesmīgas sekas. Tāpēc šādas situācijas nevar ignorēt. Šādos gadījumos jums jākonsultējas ar ārstu, lai izrakstītu atbilstošu ārstēšanu.